-
下列方程式不正确的是
A.用稀H2SO4吸收氨气:NH3+H+=NH4+
B.用CaO吸收汽车尾气中的NOx:CaO+ NO+NO2==Ca(NO2)2
C.向海带灰的浸出液中(酸性)加入双氧水提取I2:2I-+H2O2+2H+==I2+2H2O
D.足量铁溶于稀硝酸,溶液变成浅绿色:Fe+4H++NO3-=Fe3++NO↑+2H2O
高三化学选择题中等难度题查看答案及解析
-
(16分)汽车尾气中CO、NOx 以及燃煤废弃中的SO2都是大气污染物,对它们的治理具有重要意义。吸收SO2和NO,获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):
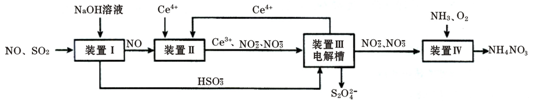
(1)装置Ⅰ中,NaOH溶液吸收SO2也可生成Na2SO3和NaHSO3的混合溶液
①写出NaOH溶液吸收SO2生成等物质的量的Na2SO3和NaHSO3混合溶液时总反应的离子方程式 。
②已知混合液pH随
:n(
)变化关系如下表:
91:9
1:1
9:91
8.2
7.2
6.2
当混合液中
时,c(Na+) c(HSO3-)+ 2c(SO32-)(填“>”“=”或“<”)
(2)装置Ⅱ中,酸性条件下,NO被Ce4+ 氧化的产物主要是NO3- 、NO2- ,写出只生成NO2-的离子方程式 ;
(3)装置Ⅲ的作用之一是再生Ce4+,其原理如下图所示。
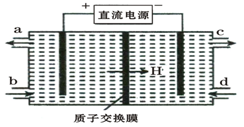
①生成的Ce4+从电解槽的 (填字母序号)口流出;
②生成S2O42 - 的电极反应式为 ;
(4)已知进入装置Ⅳ的溶液中,NO2- 的浓度为a g·L- 1 ,要使1m3该溶液中的NO2- 完全转化为NO3-,至少需向装置Ⅳ中通入标准状况下的O2 L。(用含a代数式表示)
高三化学填空题困难题查看答案及解析
-
NH3在催化剂存在时能还原NOx为N2和H2O,这是目前国外硝酸厂进行尾气治理所普遍采用的一种方法.下图是某校化学兴趣小组设计的模拟氨气还原NO的装置.
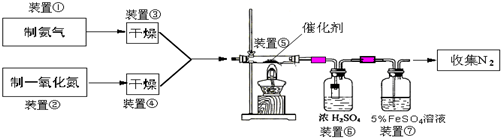
回答下列问题:
(1)若制取氨气用A装置,则发生反应的化学方程式为______ CaCl2+2NH3↑+2H2O高三化学解答题中等难度题查看答案及解析
-
下列指定反应的离子方程式正确的是
A. 用强碱溶液吸收工业制取硝酸尾气:NO + NO2+2OH-=2NO3-+H2O
B. 向硝酸银溶液中滴加氨水至过量:Ag+ + NH3·H2O=AgOH↓+ NH4+
C. 用MnO2与浓盐酸反应制Cl2: MnO2+4H++4Cl-
Mn2+ +Cl2↑+ 2H2O
D. 在强碱性溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3C1O-+2 Fe(OH)3+4OH-=2 FeO42-+3Cl-+5H2O
高三化学选择题中等难度题查看答案及解析
-
(20分)NH3和NOx在催化剂作用下可转变为N2和H2O,这是目前硝酸厂尾气治理所普遍采用的一种方法,为了提高NO的转化率实际操作中用过量的氨气。某研究小组拟验证NO能被氨气还原并计算其转化率。(已知:浓硫酸在常温下不氧化NO气体)。
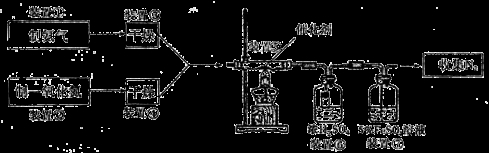
(1)装置③可以选的干燥剂为:_________(选填序号,下同);
a.浓硫酸 b.碱石灰 c.无水氯化钙
(2)若实验室只提供浓氨水和生石灰两种试剂,你会选择下图_____装置来制取氨气;下图装置C中盛放固体药品的仪器名称是_____。
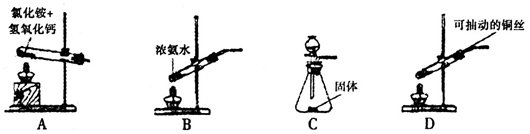
(3)写出装置⑤中反应的化学方程式_______;该反应中的氧化剂是______。
(4)实验室在用装置D制取较纯NO过程中,先在试管中加入2~3粒石灰石,注入适量稀硝酸,反应一段时间后,再塞上带有细铜丝的胶塞进行后续反应,加入石灰石的作用__________。
(5)实验完成后,检验装置⑥中NH4+的存在需要浓NaOH溶液和__________试纸。
(6)已知NO与FeSO4溶液反应形成棕色可溶性的[Fe(NO)]SO4,装置⑥中,小段玻璃管的作用是_____;装置⑦的作用是除去NO和检验氨气是否除尽,若氨气未除尽观察到的实验现象是_____。
高三化学实验题极难题查看答案及解析
-
NH3和NOx在催化剂作用下可转变为N2和H2O,这是目前硝酸厂尾气治理所普遍采用的一种方法,为了提高NO的转化率实际操作中用过量的氨气。某研究小组拟验证NO能被氨气还原并计算其转化率。(已知:浓硫酸在常温下不氧化NO气体)。

(1)装置③可以选的干燥剂为:_________(选填序号,下同);
a.浓硫酸 b.碱石灰 c.无水氯化钙
(2)若实验室只提供浓氨水和生石灰两种试剂,你会选择下图_________装置来制取氨气;所选装置中盛放生石灰的仪器名称是_____________。

(3)写出装置⑤中反应的化学方程式____________________;该反应中的氧化剂是____________。
(4)实验室在用装置D制取较纯NO过程中,先在试管中加入2~3粒石灰石,注入适量稀硝酸,反应一段时间后,再塞上带有细铜丝的胶塞进行后续反应,加入石灰石的作用__________________。
(5)实验完成后,检验装置⑥中NH4+的存在需要浓NaOH溶液和__________试纸。
(6)已知NO与FeSO4溶液反应形成棕色可溶性的[Fe(NO)]SO4,装置⑥中,没有将进气导管直接插入浓硫酸中,而是接了一小段玻璃管,小段玻璃管的作用是_____________________;装置⑦的作用是除去NO和检验氨气是否除尽,若氨气未除尽观察到⑦中的实验现象是_____________________。
(7)化学是一门以实验为基础的科学,下列叙述正确的是________(填写序号).
①将0.2mol•L-1FeCl3溶液滴加到沸水中,然后继续加热并不断搅拌可制得氢氧化铁胶体.
②检验氧化铁中的氧化亚铁,先用硫酸溶液溶解,然后加入盐酸酸化的高锰酸钾溶液。
③用NaOH固体配制100g 10%的氢氧化钠溶液时,用到的玻璃仪器主要有玻璃棒、烧杯、量筒和胶头滴管。
④托盘天平、容量瓶、量筒、滴定管等定量仪器均标有0刻度线。
⑤除去CO2中HCl,可将混合气体通过盛有饱和Na2CO3溶液的洗气瓶。
⑥纯净的氢气在氯气中安静地燃烧,产生苍白色火焰,瓶口伴有白雾。
⑦加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有
。
高三化学实验题极难题查看答案及解析
-
Ⅰ.汽车尾气中含有NO、CO等有害物质,其中NOx会引起光化学烟雾等环境问题。
NH3-SCR技术是去除NOx最为有效的技术之一:在催化剂条件下,以NH3或尿素将尾气中NOx还原为N2从而降低污染。
(1)汽车燃料中一般不含氮元素,汽缸中生成NO的原因 _________________(用化学方程式表示,该反应为为可逆反应);汽车启动后,汽缸内温度越高,单位时间内NO排放量越大,试分析其原因 _____________________________。
(2)①NH3去除尾气中的NOx,当v(NO):v(NO2)=1:1时称为“快速SCR 反应”,该反应化学方程式为______________________________________ ;
②合成NH3所用原料气H2,可用天然气为原料制得,有关反应能量变化如下所示。
CO(g)+
O2 (g)== CO2 (g) △H1=-282.0 KJ/mol
H2(g)+
O2 (g)=== H2O (g) △H2=-241.8 KJ/mol
CH4(g)+ 2O2 (g)== CO2 (g)+ 2H2O (g) △H3=-836.3 KJ/mol
则用CH4(g)和H2O(g)反应制得H2(g)和CO(g)的热化学方程式为___________。
(3)通过NOx传感器可监测NOx的含量,其工作原理如图所示,则:
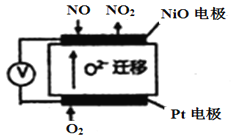
①Pt电极上发生的是 ______________反应(填“氧化”或“还原”);
②NiO电极上的电极反应式为______________________________________;
(4)研究发现,将煤炭在O2/CO2的气氛下燃烧,能够降低燃煤时NO的排放,主要反应为:2NO(g)+2CO(g)=N2(g)+2CO2(g)。在一定温度下,于2L的恒容密闭容器中充入0.1molNO和0.3molCO发生该反应,测得不同时间容器内的压强(p)与起始压强(p0)的比值(p/p0)如下表。
时间/t
0min
2min
5min
10min
13min
15min
比值(p/p0)
1
0.97
0.925
0.90
0.90
0.90
0~5min内,该反应的平均反应速率V(NO)=___________________;
(5)将上述反应的CO2与NH3为原料合成尿素,能够实现节能减排:①2NH3(g)+CO2(g)=NH2CO2NH4(s);②NH2CO2NH4(s)
CO(NH2)2(s)+H2O(g)
对于上述反应②在密闭容器中将过量NH2CO2NH4固体于300K下分解,平衡时P[H2O(g)]为aPa,若反应温度不变,将体系的体积增加50%,至达新平衡的过程中P[H2O(g)]的取值范围是__________________ (用含a的式子表示)。
高三化学综合题中等难度题查看答案及解析
-
汽车尾气的主要成分有CO、SO2、NO、NO2等。
(1)利用氨水可以将SO2、氮氧化物吸收,原理如下图所示。
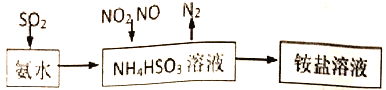
①25℃时,在pH=5的 NH4HSO3溶液中,c(SO32-)+c(NH3·H2O)-c(H2SO3)=__________mol/L(填确值)
②请写出NO2和NO按体积比1:1被吸收时反应的离子方程式_____________________。
(2)科研工作者目前正在尝试以二氧化钛(TiO2)催化分解汽车尾气的研究。
①已知:2NO(g)+O2(g)=2NO2(g) △H1=-113.0kJ·mol-1
3NO2(g)+H2O(g)=2HNO3(g)+NO(g) △H2=-138.0 kJ·mol-1
TiO2催化尾气降解原理可表示为:2COg)+O2(g)
2CO2(g) △H3
则2H2O(g)+4NO(g)+3O2(g)
4HNO3(g) △H4=______________________。
②在O2、H2O(g)浓度一定条件下,模拟CO、NO的降解,得到其降解率(即转化率)如图1所示。请解释T1后NO降解率下降的可能原因______________________。
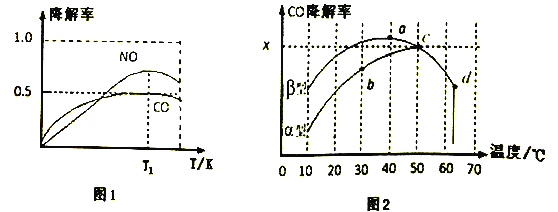
(3)沥青混凝土也可降解CO。如图2为在不同颗粒间隙的沥青混凝土(α、β型)在不同温度下,反应相同时间,测得CO降解率变化。结合如图回答下列问题:
①已知在50℃时在α型沥青混凝土容器中,平衡时O2浓度为0.01mol·L-1,求此温度下CO降解反应的平衡常数____________________________________________。(用含x的代数式表示)
②科研团队以β型沥青混凝土颗粒为载体,将TiO2改为催化效果更好的TiO2纳米管,在10℃~60℃范围内进行实验,请在如图中用线段与“
”阴影描绘出CO降解率随温度变化的曲线可能出现的最大区域范围(在图中画出)。____________
(4)TiO2纳米管的制备是在弱酸性水溶液中以金属钛为阳极进行电解,写出阳极的电极反应式____________________________________________。
高三化学综合题中等难度题查看答案及解析
-
(10分)汽车尾气是城市空气的主要污染物,如何减少汽车尾气(CO、NOx等)的污染是重要的科学研究课题。
(1) 已知:N2(g) + O2(g)
2NO(g) ΔH1
N2(g) + 3H2(g)
2NH3(g) ΔH2
2H2(g) + O2(g)
2H2O(g) ΔH3
则4NO(g) + 4NH3(g) + O2(g)
4N2(g) + 6H2O(g) ΔH =____________(用ΔH1、ΔH2、ΔH3表达)
(2) 在密闭容器中,一定条件下,进行如下反应:2NO(g)+2CO(g)
N2(g)+2CO2(g),下列说法不能说明该反应达到平衡的是__________ (填字母)
A.NO的生成速率与NO的消耗速率相等
B.v(CO)=v(CO2)
C.体系的压强保持不变
D.各物质的浓度保持不变
(3) 可用活性炭还原法处理氮氧化物。有关反应的化学方程式为:
C(s) + 2NO(g)
N2(g) + CO2(g) ΔH >0
某研究小组向密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol·L-1
时间/min
NO
N2
CO2
0
0.100
0
0
10
0.058
0.021
0.021
20
0.040
0.030
0.030
30
0.040
0.030
0.030
40
0.032
0.034
0.017
① 写出该反应的平衡常数表达式:K= 。
② 30 min后,改变某一条件,平衡发生了移动,则改变的条件是 ;若升高温度,NO浓度将 (填“增大”、“不变”或“减小”)。
高三化学填空题困难题查看答案及解析
-
(10分)汽车尾气是城市空气的主要污染物,如何减少汽车尾气(CO、NOx等)的污染是重要的科学研究课题。
(1)已知:N2(g) + O2(g)
2NO(g) ΔH1
N2(g) + 3H2(g)
2NH3(g) ΔH2
2H2(g) + O2(g)
2H2O(g) ΔH3
则4NO(g) + 4NH3(g) + O2(g)
4N2(g) + 6H2O(g) ΔH =____________(用ΔH1、ΔH2、ΔH3表达)
(2)在密闭容器中,一定条件下,进行如下反应:2NO(g)+2CO(g)
N2(g)+2CO2(g),下列说法不能说明该反应达到平衡的是__________ (填字母)
A.NO的生成速率与NO的消耗速率相等
B.v(CO)=v(CO2)
C.体系的压强保持不变
D.各物质的浓度保持不变
(3)可用活性炭还原法处理氮氧化物。有关反应的化学方程式为:
C(s) + 2NO(g)
N2(g) + CO2(g) ΔH >0
某研究小组向密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol·L-1
时间/min
NO
N2
CO2
0
0.100
0
0
10
0.058
0.021
0.021
20
0.040
0.030
0.030
30
0.040
0.030
0.030
40
0.032
0.034
0.017
①写出该反应的平衡常数表达式:K= 。
②30 min后,改变某一条件,平衡发生了移动,则改变的条件是 ;
若升高温度,NO浓度将 (填“增大”、“不变”或“减小”)。
高三化学填空题极难题查看答案及解析