-
分析下面两个案例并回答有关问题。
(1) 某城镇生产、生活的分布情况如图所示,河流中W、X、Y、Z处某次水样抽测结果如表所示。
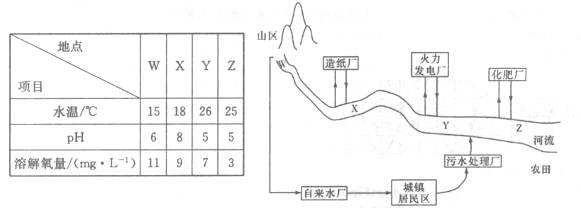
①导致X、Y处水样pH变化的原因可能是 (3分)
②Z处鱼类大量减少,产牛这种现象的原因可能是 (3分),
(2) 某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2Qi,还含有SiO2等杂质)、煤矿、石灰石和黏土。拟在该地区建设大型炼铁厂。
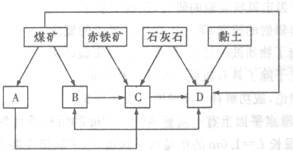
①随着铁矿的开发和炼矿的鼓厲要在该地区相应建立焦化厂、发电厂、水泥厂等,形成规模的工业体系。据此确定上图中相应工厂的名称A 、B 焦化厂、C 、D (每空1分)>
②以赤铁矿为原料,写出髙炉炼铁中得到生铁和产生炉渣的化学方程式
________________(2 分),
③从“三废”利用、环境保护等角度考虑,该地区和企业在生产中应采取的一些措施有(举出2种措施即可) (3分),
-
分析下面两个案例并回答有关问题。
(1)某城镇生产、生活的分布情况如图所示,河流中W、X、Y、Z处某次水样抽测结果如表所示。
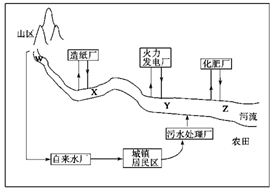
| 地点 项目 | W | X | Y | Z |
| 水温/℃ | 15 | 18 | 26 | 25 |
| pH | 6 | 8 | 5 | 5 |
| 溶解氧量/(mg·L-1) | 11 | 9 | 7 | 3 |
①导致X、Y处水样pH变化的原因可能是_______________________________
②Z处鱼类大量减少,产生这种现象的原因可能是_______________________
(2)某地区已探明蕴藏着丰富的赤铁矿(主要成分为Fe2O3,还含有SiO2等杂质)、煤矿、石灰石和黏土。拟在该地区建设大型炼铁厂。

①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成有规模的工业体系。据此确定上图中相应工厂的名称:
A________、B________、C________、D________;
②以赤铁矿为原料,写出高炉炼铁中得到生铁和产生炉渣的化学方程式_____;
③从“三废”利用、环境保护等角度考虑,该地区和企业在生产中应采取的一些措施有(举出2种措施即可)______________________________________________________________
-
分析下面两个案例并回答有关问题。
(1)某城镇生产、生活的分布情况如右图所示,河流中W、X、Y、Z处某次水样抽测结果如表所示。

| 项目 地点 | W | X | Y | Z |
| 水温/℃ | 15 | 18 | 26 | 25 |
| pH | 6 | 8 | 5 | 5 |
| 溶解氧量/(mg·L-1) | 11 | 9 | 7 | 3 |
①导致X、Y处水样pH变化的原因可能是 ;
②Z处鱼类大量减少,产生这种现象的原因可能是 。
(2)某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O3,还含有SiO2等杂质)、煤矿、石灰石和黏土。拟在该地区建设大型炼铁厂。
①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成规模的工业体系。据此确定右图中相应工厂的名称A 、B 、C 、D ;
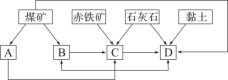
②以赤铁矿为原料,写出高炉炼铁中得到生铁和产生炉渣的化学方程式 ;
③从“三废”利用、环境保护等角度考虑,该地区和企业在生产中应采取的一些措施有(举出2种措施即可) 。
-
[化学一选修2化学与技术]分析下面两个案例并回答有关问题.
(1)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤.压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2 7%,O2 11%,N282%):
压强/MPa
SO2转化率
温度/℃ |
0.1 |
0.5 |
1 |
10 |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
①利用表中数据,如何推断出SO2的催化氧化反应是一个放热反应?______
②选择适应的催化剂,是否可以提高SO2的转化率?______(填“是”或“否”)是否可以增大该反应所放出的热量?______(填“是”或“否”).
③已知:2SO2(g)+O2(g) 2SO3(g),△H=-196.6k J/mol,计算每生产1万吨98%硫酸所需要SO3质量为______t,由SO2生产这些SO3时放出的热量为______kJ.
2SO3(g),△H=-196.6k J/mol,计算每生产1万吨98%硫酸所需要SO3质量为______t,由SO2生产这些SO3时放出的热量为______kJ.
(2)某地区已探明蕴藏有丰富的赤铁矿(主要成分为Fe2O3,还含有SiO2等杂质)、煤矿、石灰石和黏土,拟在该地区建设大型炼铁厂.
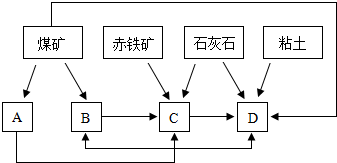
①随着铁矿的开发和炼铁厂的建立,需要在该地区相应建立焦化厂、发电厂、水泥厂等,形成规模的工业体系.据此确定上图中相应工厂的名称B______、D______.
②以赤铁矿为原料,写出高炉炼铁中得到生铁以及产生炉渣的化学方程式______ 2Fe+3CO2 、CaCO3+SiO2  CaSiO3+CO2
CaSiO3+CO2
-
铁及其化合物在人类的生活生产中有着重要的作用,Fe2+、Fe3+是影响水质的一个重要因素。回答下列问题:
I:测量某河水样本中铁的含量
(1)水样中Fe2+的含量越大,溶解氧的含量就越低,用离子方程式解释原因___________。
(2)测定Fe2+取5mL c mo/L的KMnO4标准液,稀释至100mL。取10.00mL河水水样,加入稀硫酸后,用稀释后的KMnO4溶液进行滴定,用去KMnO4溶液V1mL。
①用___________(填滴定管的名称)盛放KMnO4标准液。
②滴定达到终点的标志是___________。
(3)测定Fe3+:取10.00mL水样,转移至盛有过量锌粒的烧杯中充分反应。加入过量稀硫酸,用表面皿盖住烧杯并加热10分钟。冷却后用(2)中稀释后的KMnO4溶液滴定,消耗KMnO4溶液V2mL。
①锌粒的作用是___________。
②河水中Fe3+的浓度是___________mol/L(用含字母的代数式表示)。
Ⅱ:氢氧化亚铁[Fe(OH)2]在常温常压下为白色固体。
(4)当溶液中的离子浓度<1×10-5mol·L-1时,可以认为该离子已沉淀完全。已知常温Fe(OH)2的Ksp为8.0×10-16。现调节含Fe2+的某河水样品pH=9,用简要计算过程说明Fe2+是否已经达到沉淀完全:___________。
(5)一种用Na2SO4溶液做电解液,电解制取Fe(OH)2的实验装置如图所示。通电后,溶液中产生白色沉淀,且较长时间不变色。

①必须使用铁电极的是___________(填“A"或“B”)极。
②B电极的电极反应式为___________。
-
氮及其化合物在人们的日常生活、生产和环保事业中属于“明星物质”。回答下列问题:
(1)氨气是农业肥料和化工生产的重要原料,其电子式为____。
(2)叠氮化钠(NaN3)在药物制备、合成影像、化学分析、汽车制造等行业有着广泛的用途,但该物质极易爆炸,且有副毒。可用NaClO溶液对含有叠氮化钠的溶液进行处理,生成一种无污染的气体单质,反应的化学方程式为______________。
(3)“固氮”是农业科学家研究的永恒主题。在某特殊催化剂和光照条件下,N2与水反应可生成NH3。
已知:
(i)4NH3(g)+3O2(g) 2N2(g) +6H2O(g) △H1=-1266 kJ/mol;
2N2(g) +6H2O(g) △H1=-1266 kJ/mol;
(ii)H2O(g)=H2O(l) △H2= -44.0kJ/mol。
则2N2(g) +6H2O(l) 4NH3(g)+3O2(g) △H3=______kJ/mol。
4NH3(g)+3O2(g) △H3=______kJ/mol。
(4)目前“人工固氮”最成功的应用就是工业合成氨:
N2(g) +3H2(g) 2NH3(g) △H=-92.4kJ/mol。将1.00molN2和3.00molH2充入到容积为3L的恒容密闭容器中,发生上述反应。
2NH3(g) △H=-92.4kJ/mol。将1.00molN2和3.00molH2充入到容积为3L的恒容密闭容器中,发生上述反应。
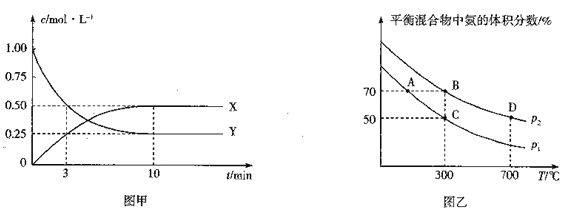
①图甲是测得X、Y 的浓度随时间变化的曲线.其中Y 为_____(写化学式),反应达到平衡时的平均反应速率v(N2) =_________。
②在不同温度和压强下,平衡体系中NH3的体积分数与温度、压强关系如图乙,则压强p1_____p2(填“>”“<”“=”或“不确定”,下同),B、D 两点的平衡常数KB____KD,B 点N2 的转化率=_________(保留3位有效数字)。
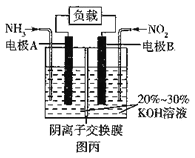
(5)“绿水青山就是金山银山”,利用原电池原理(6NO2 +8NH3=7N2+12H2O)可以处理氮的氧化物和NH3 尾气,装置原理图如图丙:
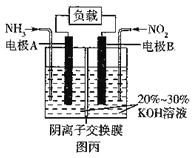
负极反应式为__________,当有标准状况下4.48 L NO2被处理时,转移电子的物质的量为_____mol。
-
氮及其化合物在人们的日常生活、生产和环保事业中属于“明星物质”。回答下列问题:
(1)氨气是农业肥料和化工生产的重要原料,其电子式为____。
(2)叠氮化钠(NaN3)在药物制备、合成影像、化学分析、汽车制造等行业有着广泛的用途,但该物质极易爆炸,且有副毒。可用NaClO溶液对含有叠氮化钠的溶液进行处理,生成一种无污染的气体单质,反应的化学方程式为______________。
(3)“固氮”是农业科学家研究的永恒主题。在某特殊催化剂和光照条件下,N2与水反应可生成NH3。
已知:
(i)4NH3(g)+3O2(g) 2N2(g) +6H2O(g) △H1=-1266 kJ/mol;
2N2(g) +6H2O(g) △H1=-1266 kJ/mol;
(ii)H2O(g)=H2O(l) △H2= -44.0kJ/mol。
则2N2(g) +6H2O(l) 4NH3(g)+3O2(g) △H3=______kJ/mol。
4NH3(g)+3O2(g) △H3=______kJ/mol。
(4)目前“人工固氮”最成功的应用就是工业合成氨:
N2(g) +3H2(g) 2NH3(g) △H=-92.4kJ/mol。将1.00molN2和3.00molH2充入到容积为3L的恒容密闭容器中,发生上述反应。
2NH3(g) △H=-92.4kJ/mol。将1.00molN2和3.00molH2充入到容积为3L的恒容密闭容器中,发生上述反应。
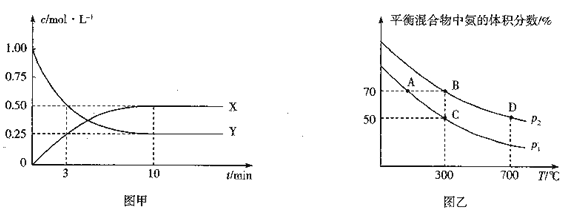
①图甲是测得X、Y 的浓度随时间变化的曲线.其中Y 为_____(写化学式),反应达到平衡时的平均反应速率v(N2) =_________。
②在不同温度和压强下,平衡体系中NH3的体积分数与温度、压强关系如图乙,则压强p1_____p2(填“>”“<”“=”或“不确定”,下同),B、D 两点的平衡常数KB____KD,B 点N2 的转化率=_________(保留3位有效数字)。
(5)“绿水青山就是金山银山”,利用原电池原理(6NO2 +8NH3=7N2+12H2O)可以处理氮的氧化物和NH3 尾气,装置原理图如图丙:
负极反应式为__________,当有标准状况下4.48 L NO2被处理时,转移电子的物质的量为_____mol。
-
下列对于与生产、生活有关的化学问题的分析正确的是( )
A.对“地沟油”进行分馏可得到汽油
B.向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量
C.误食可溶性重金属盐后,应采取的有效应急措施是喝大量的豆浆或牛奶
D.PM 2.5、二氧化碳都属于空气质量日报的内容
-
下列对于生产、生活有关的化学问题的分析正确的是
A.对“地沟油”进行分馏可得到汽油
B.向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量
C.PM 2.5、二氧化碳都属于空气质量日报的内容
D.误食可溶性重金属盐后,应采取的有效应急措施是喝大量的豆浆或牛奶
-
下列对生产、生活有关化学问题的分析正确的是
A.医疗上进行胃部造影前,患者服用的“钡餐”是BaCO3等不溶于水的物质
B.铝合金的大量使用归功于人们能用焦炭等还原剂从氧化铝中获取铝
C.“百炼成钢”的化学含义是使用氧化剂提高生铁中碳的含量
D.液氯罐中的液氯泄漏时,可将其移入水塘中,并向水塘中加入生石灰











