-
氮化锶(Sr3N2)在工业上有广泛应用。已知氮化锶遇水剧烈反应产生氢氧化锶和氨气。
锶和镁位于同主族且锶比镁活泼, 锶与氮气在加热条件下反应产生氮化锶。某学习小组拟设计两套方案制备氮化锶:
方案Ⅰ:根据下列装置制备氮化锶。
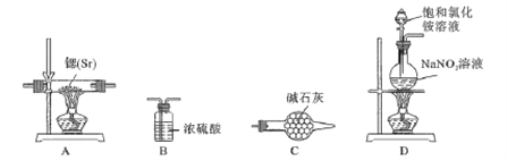
已知:实验室用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气。
回答下列问题:
(1)气流从左至右,选择装置并排序为___________(填字母表示)。
(2)写出实验室制备N2的化学方程式____________
(3)实验时先点燃_____处酒精灯(填“A”或“D”),一段时间后,点燃另一只酒精灯。
(4)氮化锶遇水发生反应的化学方程式为____________
方案Ⅱ:某氮气样品可能含有少量的CO、CO2、O2等气体杂质,某同学设计如下装置制备氮化锶(各装置盛装足量试剂)。已知:醋酸二氨合亚铜CH3COO[Cu(NH3)2]溶液能定量吸收CO,但易被O2氧化,失去吸牧CO能力;连苯三酚鹹性溶液能定量吸收O2.
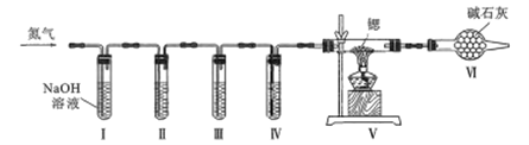
(5)试管Ⅱ盛装的试剂是__________填代号)。
a.连苯三酚碱性溶液 b.醋酸二氨合亚铜溶液 C.浓巯酸 d.赤热铜粉
装置Ⅵ的作用是_______________
(6)测定产品纯度:取wg产品,向其中加入适量的水。将产生的气体全部通人到依硫酸中,依硫酸增重mg,则产品纯度为__(用代数式表示)。有同学认为上述方法使测得产品纯度偏高,其原因是___________
-
氮化锶(Sr3N2)在工业上广泛用于生产荧光粉。已知:锶与镁位于同主族:锶与氮气在加热条件下可生成氮化锶,氮化锶遇水剧烈反应。
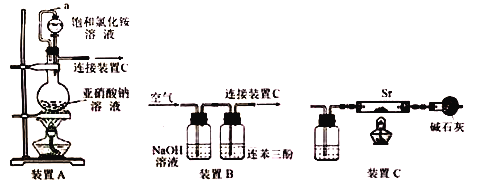
I.利用装置A和C制备Sr3N2
(1)实验装置中玻璃管之间需用橡皮管连接,其连接方法是先将___________,然后稍稍用力即可将玻璃管插入橡皮管。
(2)写出由装置A制备N2的化学反应方程式___________。
(3)装置A中a导管的作用是________。利用该套装置时,有同学提出应先点燃置A的酒精灯一段时间后,再点燃装置C的酒精灯,你同意其观点吗?_______(“同意”或“不同意”)。理由是___________。
Ⅱ.利用装置B和C制备Sr3N2。利用装置B从空气中提纯N2(已知:氧气可被连苯三酚溶液定量吸收)
(4)写出装置B的NaOH溶液中发生反应的离子方程式___________。
(5)装置C中广口瓶盛放的试剂是___________。
Ⅲ.测定Sr3N2产品的纯度
(6)取10.0g该产品,向其中加入适量的水,将生成的气体全部通入浓硫酸中,利用浓硫酸增重质量计算得到产品的纯度,该方法测得产品的纯度偏高,其原因是_______。经改进后测得浓硫酸增重1.02g,则产品的纯度为___________。
-
氮化锶(Sr3N2)在工业上广泛用于生产荧光粉。已知:锶与镁位于同主族:锶与氮气在加热条件下可生成氮化锶,氮化锶遇水剧烈反应。
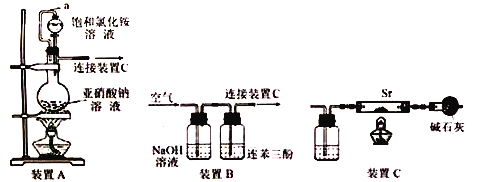
I.利用装置A和C制备Sr3N2
(1)实验装置中玻璃管之间需用橡皮管连接,其连接方法是先将___________,然后稍稍用力即可将玻璃管插入橡皮管。
(2)写出由装置A制备N2的化学反应方程式___________。
(3)装置A中a导管的作用是________。利用该套装置时,有同学提出应先点燃置A的酒精灯一段时间后,再点燃装置C的酒精灯,你同意其观点吗?_______(“同意”或“不同意”)。理由是___________。
Ⅱ.利用装置B和C制备Sr3N2。利用装置B从空气中提纯N2(已知:氧气可被连苯三酚溶液定量吸收)
(4)写出装置B的NaOH溶液中发生反应的离子方程式___________。
(5)装置C中广口瓶盛放的试剂是___________。
Ⅲ.测定Sr3N2产品的纯度
(6)取10.0g该产品,向其中加入适量的水,将生成的气体全部通入浓硫酸中,利用浓硫酸增重质量计算得到产品的纯度,该方法测得产品的纯度偏高,其原因是_______。经改进后测得浓硫酸增重1.02g,则产品的纯度为___________。
-
氮化锶(Sr3N2)在工业上广泛用于生产荧光粉。已知:锶与镁位于同主族;锶与氮气在加热条件下可生成氮化锶,氮化锶遇水剧烈反应。
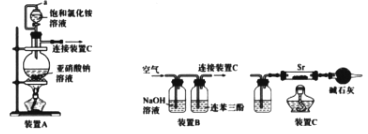
I.利用装置A和C制备Sr3N2
(1)写出由装置A制备N2的化学方程式_______。
(2)装置A中a导管的作用是_______。利用该套装置时,应先点燃装置A的酒精灯一段时间后,再点燃装置C的酒精灯,理由是__________。
II.利用装置B和C制备Sr3N2。利用装置B从空气中提纯N2(已知:氧气可被连苯三酚溶液定量吸收)
(3)写出装置B的NaOH溶液中发生反应的离子方程式_________。
(4)装置C中广口瓶盛放的试剂是_________。
III.测定Sr3N2产品的纯度
(5)取ag该产品,向其中加入适量的水,将生成的气体全部通入浓硫酸中,利用浓硫酸增重质量计算得到产品的纯度,该方法测得产品的纯度偏高,其原因是____。经改进后测得浓硫酸增重bg,则产品的纯度为_____(用相关字母的代数式表示)。
-
已知氨气跟氧化铜反应可以制备氮气,有关化学方程式:
2NH3+3CuO  3Cu+3H2O+N2↑
3Cu+3H2O+N2↑
纯氮气跟镁在高温下反应可得到氮化镁,但氮化镁遇水即剧烈反应生成氢氧化镁和氨气.
(1)下面是某化学课外小组的同学提出的实验室制备氨气的几种方案
A.NH4Cl溶液与澄清石灰水共热 B.浓氨水逐滴加到生石灰中
C.在一定条件下,N2与H2化合 D.加热分解NH4Cl固体
你认为其中最合理的方案是______(填字母);
(2)该小组同学设计的制备氮化镁的方案有以下两个.分别见实验方案的装置图.实验前系统内的空气均已设法排尽.
方案一
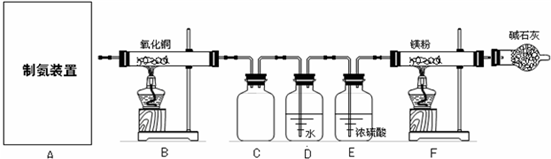
①按(1)中所选合理的制氨方案,在框内画出制氨的反应装置图;
②该实验完成后,能否得到纯净的氮化镁______(填“能”或“不能”);
③装置C的作用是______;D装置的作用是______.
方案二
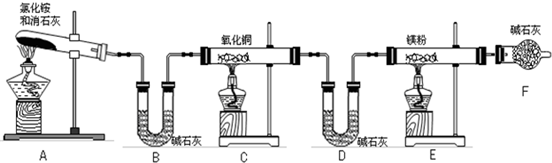
已知:6NH3+3Mg 3Mg(NH2)2+3H2↑
3Mg(NH2)2+3H2↑
①写出A装置中发生反应的化学方程式______.②该方案中存在的主要问题是______.
-
氨气及含氮化合物在化工生产和国防工业中具有广泛应用。请回答:
(1)已知:(i)氢气的燃烧热为286.0 kJ• mol-1
(ii)4NH3(g)+3O2(g) 2N2(g)+6H2O △H=-1530.6kJ•mol-1。
2N2(g)+6H2O △H=-1530.6kJ•mol-1。
①合成氨反应的热化学方程式为__________________________________。
②对于反应(ii),正、逆反应活化能的大小关系为:E正_______E逆 (填>、=或<)。
(2)恒温恒容条件下,起始按物质的量之比为1 : 1向密闭容器中充入N2(g)和H2(g),发生合成氨的反应。达平衡后,N2(g)的体积分数为_________;然后只降低温度,N2(g)的体积分数会______(填选项字母)。
A.增大 B.减小 C.不变 D.不能判断
(3)T℃ 时,CO2(g)和 NH3(g)合成尿素的原理为 2NH3(g)+ CO2(g) CO(NH2)2(s)+H2O(l)。在2 L恒容密闭容器中,通入1.2 mol NH3(g)和0.6 mol CO2(g),2 min时反应恰好达到平衡,测得c(NH3)=0.2mol • L-1
CO(NH2)2(s)+H2O(l)。在2 L恒容密闭容器中,通入1.2 mol NH3(g)和0.6 mol CO2(g),2 min时反应恰好达到平衡,测得c(NH3)=0.2mol • L-1
①0-2 min内,用NH3表示的反应速率v(NH3)=___________;反应的平衡常数K=__________。
②若其他条件不变,2 min时将容器体积迅速压缩到1 L,在3 min时重新达到平衡,请在图1中画出2〜3 min内c(NH3)随时间(t)变化的曲线关系图:__________。
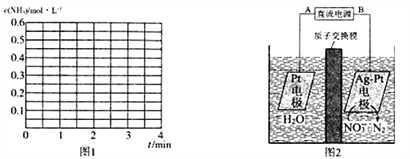
(4)电化学降解法可用于治理水中硝酸盐的污染,电化学降解NO3-的原理如图2所示:
①电源正极为___________(填“A”或“B”),阴极反应式为________________________________。
②若电解过程中转移了 1 mol e-,则膜两侧电解液的质量变化差值(Δm正-Δm右)为________g。
-
氨气及含氮化合物在化工生产和国防工业中具有广泛应用。请回答:
(1)已知:(i)氢气的燃烧热为286.0 kJ·mol-1
(ii)4NH3(g)+3O2(g) 2N2(g)+6H2O (l) ΔH=- 1530.6 kJ·mol-1。
2N2(g)+6H2O (l) ΔH=- 1530.6 kJ·mol-1。
合成氨反应的热化学方程式为_____________________________。
(2)恒温恒容条件下,起始按物质的量之比为1∶1向密闭容器中充入N2(g)和H2(g),发生合成氨的反应。达平衡后,N2(g)的体积分数为_______________;然后只降低温度,N2(g)的体积分数会_________(填选项字母)。
A.增大 B.减小 C.不变 D.不能判断
(3)T℃时,CO2(g)和NH3(g)合成尿素的原理为2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(1)。在2 L恒容密闭容器中,通入1.2 mol NH3(g)和0.6 mol CO2(g),2 min时反应恰好达到平衡,测得c(NH3)=0.2 mol·L-1。
CO(NH2)2(s)+H2O(1)。在2 L恒容密闭容器中,通入1.2 mol NH3(g)和0.6 mol CO2(g),2 min时反应恰好达到平衡,测得c(NH3)=0.2 mol·L-1。
①0~2min内,用NH3表示的反应速率υ(NH3)=___________;反应的平衡常数K=____________。
②若其他条件不变,2 min时将容器体积迅速压缩到1L,在3 min时重新达到平衡,请在图1中画出2~3 min内c(NH3)随时间(t)变化的曲线关系图。
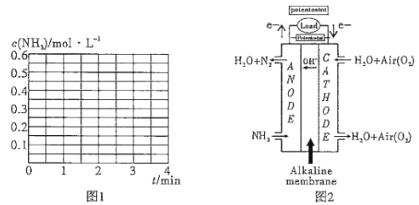
(4)碱性氨气燃料电池的装置如图2 所示,写出负极的电极反应式____________________。当电路中每通过3.6 mol e-,则需要标况下空气的体积________________L。
-
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。
完成下列计算:
(1)叠氮化钠(NaN3)受撞击分解产生钠和氮气,故可应用于汽车安全气囊。若78克叠氮化钠完全分解,产生标准状况下氮气___________________L 。
(2)钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。计算溶液中氢氧化钠的物质的量浓度______________________(忽略液体体积变化)。
(3)氢氧化钠溶液处理铝土矿并过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应: 2NaAl(OH)4+CO2→2Al(OH)3↓+Na2CO3+H2O。己知通入二氧化碳112 L(标准状况下),生成的Al(OH)3和Na2CO3的物质的量之比为4:5。若向该溶液中通入的二氧化碳为224L(标准状况下),计算生成的 Al(OH)3和Na2CO3的物质的量的最大值。
(4)为测定某硫酸吸收含氨气废气后,所得铵盐中氮元素的质量分数,现将不同质量的铵盐固体分别加入到50.00mL相同浓度的氢氧化钠溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。部分测定结果如下表:
| 铵盐的质量/g | 10.00 | 20.00 | 30.00 | 50.00 |
| 浓硫酸增加的质量/g | m | m | 1.29 | 0 |
试回答:
该铵盐的成分为_______________________________。
该铵盐中氮元素的质量分数为:_______________________________(须列式计算)。
-
氮化锂(Li3N)常作固体电解质和催化剂,遇水蒸气剧烈反应生成氢氧化锂和氨气。某实验小组用一瓶氮气样品制备纯净的氮化锂的装置如图所示。
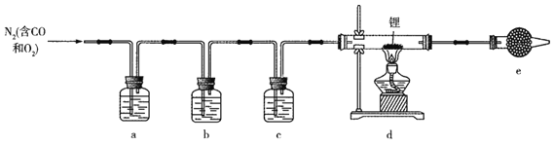
已知:连苯三酚碱性溶液能定量吸收少量O2,氯化亚铜盐酸溶液能定量吸收少量CO生成Cu(CO)Cl·H2O且易被O2氧化;在加热条件下,CO2与锂发生剧烈反应。下列说法正确的是
A. 干燥管e中试剂为无水CuSO4,用于检验氮气中的水蒸气
B. 为了减少气体用量,先点燃酒精灯再通入氮气
C. a、c中试剂分别为连苯三酚碱性溶液、浓硫酸
D. a装置可以换成盛装赤热铜粉的硬质玻璃管
-
氮元素的氢化物和氧化物在工业生产和防建设中都有广泛的应用.请回答下列问题:
(1)氨气可由N2和H2反应制取,N2(g)+3H2(g)⇌2NH3(g)反应过程的能量变化如图所示:已知1molN2分子中的化学键断裂时需要吸收942kJ的能量;1molH2分子中的化学键断裂时需要吸收436kJ的能量;形成1molN﹣H键时释放390.8kJ的能量.
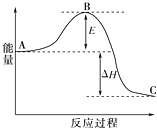
①图中E的大小对该反应热有无影响?____________________________.该反应需要用铁触媒作催化剂,加铁触媒会使图中B点升高还是降低?______________________,理由_________________.
②图中△H=___kJ/mol.
③如果反应速率v(H2)为0.15mol/(L•min),则v(N2)=_____________mol/(L•min),v(NH3)=_________________________________________.
(2)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气.
已知:N2(g)+2O2(g)=N2O4(l) △H=﹣19.5kJ•mol﹣1
N2H4(l)+O2(g)=N2(g)+2H2O(g)△H=﹣534.2kJ•mol﹣1
请写出肼和 N2O4反应的热化学反应方程式_______________________ .










