-
铝土矿为自然界中铝的重要存在形式,通常含有50﹪左右的Al2O3,以及SiO2、Fe2O3和MgO等成分。上述4种氧化物中,属于两性氧化物的是
A. Al2O3 B. SiO2 C. Fe2O3 D. MgO
高二化学选择题中等难度题查看答案及解析
-
某铝土矿的主要成分为Al2O3·xH2O,还含有Fe2O3和SiO2杂质。称取17.5g铝土矿样品,加入200mL1.65mol/L稀H2SO4,恰好完全反应,过滤得到滤渣0.3g,然后在滤液中加入足量NaOH溶液,得到沉淀2.14g。(提示:SiO2杂不与稀硫酸反应)
(1)写出本题涉及到的任意两个反应的化学方程式或离子方程式___。
(2)该样品中,Fe2O3的物质的量___。
(3)铝土矿样品中Al2O3的质量___。
(4)试计算样品中Al2O3·xH2O的x值___。(要求计算过程)
高二化学计算题中等难度题查看答案及解析
-
蓝宝石的主要成分为ⅢA族元素的氧化物,该氧化物为
A.Al2O3 B.SiO2
C.Fe2O3 D.MgO
高二化学单选题简单题查看答案及解析
-
从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取Al2O3的两种工艺流程如下:
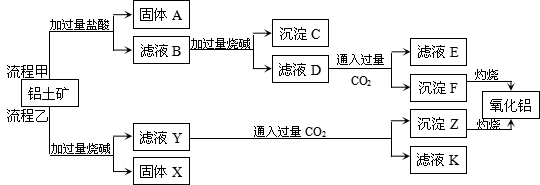
请回答下列问题:
(1)流程甲加入盐酸后生成Fe3+的离子方程式为 ;
(2)铝土矿中固体A 是 (填化学式),写出沉淀F转化为氧化铝的化学方程式 ;
(3)流程乙中,烧碱与Al2O3反应的离子方程式为 ;
(4)固体X 是 (填化学式)
高二化学推断题困难题查看答案及解析
-
工业上以铝土矿(主要成分是A12O3,含杂质Fe2O3和SiO2)为原料生产铝,其生产流程如下:
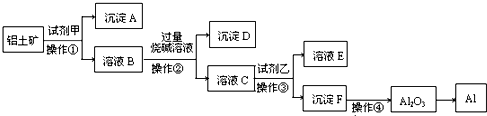
(1)工业上由Al2O3 冶炼金属Al所采用的方法是______(填字母).
a.电解法 b.加热分解 c.加入还原剂
(2)若在实验室中完成上述流程,操作①~④中属于过滤的是______(填序号).
(3)加入试剂甲后发生反应的离子方程式是______.
(4)在溶液B中加入过量烧碱溶液的目的是______.高二化学解答题中等难度题查看答案及解析
-
工业上以铝土矿(主要成分是A12O3,含杂质Fe2O3和SiO2)为原料生产铝,其生产流程如下:
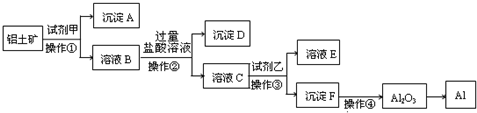
请回答:
(1)工业上Al2O3 冶炼Al所采用的方法是________,化学方程式________
(2)加入试剂甲后发生反应的离子方程式有两个,一是________,二是________.
(3)在溶液B中加入过量盐酸溶液的目的是________.
(4)加入试剂乙后发生反应的离子方程式________.
(5)铝与氢氧化钠溶液反应的离子方程式为________.高二化学填空题中等难度题查看答案及解析
-
能与铝粉混合组成铝热剂的氧化物是( )
A.SiO2 B.MgO C.Al2O3 D.Fe2O3
高二化学选择题简单题查看答案及解析
-
.铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中.工业上用铝土矿制备铝的某种化合物的工艺流程如下.

(1)在滤液A中加入漂白液,生成红褐色沉淀,滤液A、B显酸性.
①滤液A中加入漂白液,发生氧化还原反应生成红褐色沉淀,用离子方程式表示为:
②使滤液B中的铝元素以沉淀析出,可选用的最好试剂为 (填代号).
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
(2)由滤液B制备少量无水AlCl3
①由滤液B制备氯化铝晶体(将AlCl36H2O)涉及的操作为: 、冷却结晶、 (填操作名称)、洗涤.
②将AlCl36H2O溶于浓硫酸进行蒸馏,也能得到一定量的无水AlCl3,此原理是利用浓硫酸下列性质中的 (填序号).
①氧化性 ②吸水性 ③难挥发性 ④脱水性
(3)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为 (填代号).

高二化学实验题简单题查看答案及解析
-
单质铝应用极为广泛,从铝土矿中提取铝主要分以下三个阶段,根据要求回答相关问题
(1)铝土矿的提纯:铝土矿主要成分是Al2O3(含有Fe2O3、SiO2等杂质),提纯流程如下图所示:
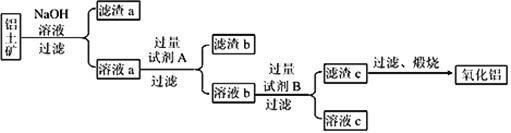
①在用NaOH溶液母液浸提过程中需研碎、湿磨,其目的是______________________________。
②向溶液a中通入过量CO2,所得不溶物煅烧后也可得Al2O3,该方法的缺点是___________________________________________________。
(2)制备无水氯化铝
其反应为:2Al2O3+6Cl2
4AlCl3+O2
③为促进该反应的进行,实际生产中需加入焦炭,其原理是_____________________________。
(3)电解制取铝
目前可低温电解AlCl3熔盐得到金属铝纯的无水氯化铝熔点190℃,沸点180℃,其导电性如图:
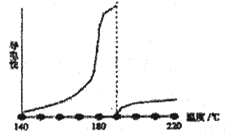
①从图中可知,AlCl3熔融液导电能力___________________________。
②但若在AlCl3中加入NaCl,使形成共融物,将AlCl3制成离子型液体,导电能力增强,熔融液中存在的阴离子是Cl-、AlCl4-、Al2Cl7-,请写AlCl3加入NaCl后形成离子型液体的两个离子方程式:AlCl3+ Cl-=AlCl4-、及平衡________________________________。
③电解时,阳极主要是AlCl4-放电,其电极反应为__________________________________。
④为保证电解进行,熔融液主要离子是AlCl4-、Al2Cl7-,则n(AlCl3)∶n(NaCl)应大于________。
高二化学综合题困难题查看答案及解析
-
Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备。工艺流程如下:
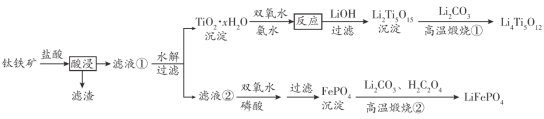
“酸浸”后,钛主要以
形式存在,若“滤液②”中c(Mg2+)=0.02 mol ·L-1,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1.0×10-5mol·L-1,此时是否有Mg3(PO4)2沉淀生成? 已知FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-2 _____________(列式计算)。
高二化学计算题中等难度题查看答案及解析