-
恒温(1100℃)恒容密闭容器中发生反应:Na2SO4(s)+4H2(g)→Na2S(s)+4H2O(g)。下列说法正确的是( )
A. 该反应的平衡常数表达式K=c(H2O)/c(H2)
B. 若容器内气体的密度或压强保持不变,均说明该反应已达到平衡状态
C. 若Na2SO4足量,改变起始充入H2的浓度,达平衡时H2的转化率不变
D. 若初始时投入2.84gNa2SO4与一定量H2,反应达平衡时容器内固体共有2.264g,则Na2SO4的转化率为45%
高三化学选择题中等难度题查看答案及解析
-
1000℃时,硫酸钠与氢气发生下列反应:Na2SO4(s) + 4H2(g)
Na2S(s) + 4H2O(g) 。
(1)该反应的平衡常数表达式为____________________。
已知K1000℃<K1200℃,则该反应是________反应(填“吸热”或“放热”)。
(2)该温度下,在2L盛有1.42 g Na2SO4的密闭容器中通入H2气体,5分钟后测得固体质量为1.10 g。则5分钟内H2的平均反应速率为_________________。
(3)能说明该反应已达到平衡状态的是______(填序号)。
a.容器内压强保持不变 b.容器内气体密度保持不变
c.c(H2) = c(H2O) d.υ正(H2) =υ逆(H2O)
(4)向平衡体系中加入焦炭,下列图像正确的是___________(填序号)。
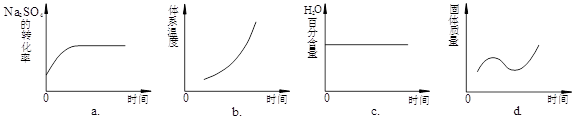
(5)用有关离子方程式说明上述反应产物水溶液的酸碱性______________________________,欲使该溶液中S2—浓度增大,平衡逆向移动,可加入的物质是____________________。
高三化学填空题简单题查看答案及解析
-
1000℃时,硫酸钠与氢气发生下列反应:Na2SO4(s) + 4H2(g)
Na2S(s) + 4H2O(g) 。
(1)该反应的平衡常数表达式为____________________。
已知K1000℃<K1200℃,则该反应是________反应(填“吸热”或“放热”)。
(2)该温度下,在2L盛有1.42 g Na2SO4的密闭容器中通入H2气体,5分钟后测得固体质量为1.10 g。则5分钟内H2的平均反应速率为_________________。
(3)能说明该反应已达到平衡状态的是______(填序号)。
a. 容器内压强保持不变 b. 容器内气体密度保持不变
c. c(H2) = c(H2O) d. υ正(H2) =υ逆(H2O)
(4)向平衡体系中加入焦炭,下列图像正确的是___________(填序号)。
(5)用有关离子方程式说明上述反应产物水溶液的酸碱性______________________________,欲使该溶液中S2—浓度增大,平衡逆向移动,可加入的物质是____________________。
高三化学填空题困难题查看答案及解析
-
1100℃时,在体积为5L的密闭容器中,发生可逆反应:Na2SO4(s)+4H2(g)
Na2S(s)+4H2O(g)并达到平衡,请完成下列各题:
(1)上述反应中涉及的非金属元素原子的半径从大到小的顺序为_____________,非金属性最强的元素原子的电子排布式_________________,其电子的自旋方向共有________种。
(2)该反应中O、S属于同主族元素,比较它们的单质的氧化性_____________________(用化学方程式表示),写出Na2O的电子式______,比较Na2O和Na2S的熔点高低:Na2O___Na2S。
(3)上述平衡的平衡常数表达式K=______________________。降低温度,K值减小,则正反应为_______(填“吸热”或“放热”)反应。
(4)能判断反应达到平衡状态的依据是_____________(填序号)。
A.混合气体的压强不变 B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.各气体的浓度相等
(5)若初始时加入的Na2SO4为2.84g,10分钟后达到平衡时Na2SO4的转化率为45%,V(H2)=__________________。平衡后,向容器中充入1molH2,平衡向_________________(填“正反应方向”、“逆反应方向”或“不移动”),重新达到平衡后,与原平衡相比,H2的体积百分含量_____________(填“增大”、“减小”或“不变”)
高三化学综合题中等难度题查看答案及解析
-
I.1100OC时,在恒容密闭容器中,发生可逆反应:
Na2SO4(s)+4H2(g)
Na2S(s)+4H2O(g)
并达到平衡,请完成下列各题:
(1)达到平衡时的平衡常数表达式K=_______________。降低温度,K值减小,则正反应为____________(填“吸热”或“放热”)反应。
(2)向该容器中分别加入以下物质,对平衡的影响如何?
A.正向移动 B.逆向移动 C.不发生移动
①加入少量Na2
SO4,则平衡:__________(填所选字母)
②加入少量灼热的Fe3O4 ,则平衡:_________(填所选字母)
II.将CH4设计成燃料电池,其利用率更高,装置示意如右图

(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积VL。
①0<V≤44.8L时,电池总反应方程式为________________;
②44.8L<V≤89.6L时,负极电极反应为_________________;
③V=67.2L时,溶液中阴离子浓度大小关系为____________;
高三化学填空题困难题查看答案及解析
-
1000℃时,在恒容密封容器中发生下列反应:Na2SO4(s)+4H2(g)
Na2S(s)+4H2O(g)。
(1)该温度下,在2L盛有1.42 g Na2SO4的密闭容器中通入H2气体,5分钟后测得固体质量为1.10 g。
则5分钟内H2的平均反应速率为________。
(2)能说明该反应已达到平衡状态的是____(填序号)。
a.容器内压强保持不变 b.容器内气体密度保持不变
c.c(H2)=c(H2O) d.v正(H2)=v逆(H2O)
(3)向该容器中分别加入以下物质,对平衡的影响如何?,(填“正向移动”,“逆向移动”或“不发生移动”)
①加入少量Na2SO4固体,则平衡:________②加入少量灼热的碳粉,则平衡:__________
(4)若将反应后的物质溶于水,用有关离子方程式说明上述反应产物水溶液的酸碱性____________,欲使该溶液中S2-浓度增大,平衡逆向移动,可加入的物质是________。
高三化学填空题中等难度题查看答案及解析
-
将H2和CO以
=2的方式充入1 L的恒容密闭容器中,一定条件下发生反应:4H2(g)+2CO(g)
CH3OCH3(g)+H2O(g),测得CO的平衡转化率随温度、压强变化关系如图所示。下列说法正确的是
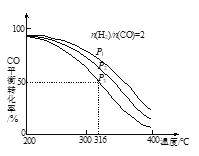
A.该反应的△H<0
B.压强大小:P1<P2<P3
C.在316℃时,该反应的平衡常数为0.25
D.若在P3和316℃时,起始时
=3,则达到平衡时,CO转化率大于50%
高三化学多选题中等难度题查看答案及解析
-
某班级同学查阅资料,对Na2S有了一定的认识,并提出了以下几个问题,请回答:
(1)1000℃时,在密闭容器中加入一定量的Na2SO4固体使其发生以下反应达到平衡:
Na2SO4(s)+4H2(g)
Na2S(s)+4H2O(g) ΔH>0若反应在恒温恒容状态下进行,回答以下问题:
向容器中分别加入以下物质,判断对平衡有无影响,有影响的填写出平衡移动的方向。
①加入Na2SO4 。②加入焦炭 。
(2)向Na2S的浓溶液中逐滴加入稀盐酸,直到不再生成H2S气体为止,则在此过程中,溶液的c(HS-)变化趋势可能是 。
a.逐渐减小 b.逐渐增大
c.先逐渐增大,而后减小 d.先逐渐减小,而后增大
(3)Na2S溶液与下列溶液混合,不能发生反应的是 。
①H2S ②SO2 ③Na2SO3 ④酸性KMnO4溶液 ⑤CuSO4 ⑥氯水
(4)写出Na2S和AlCl3溶液反应的离子方程式 。
高三化学填空题中等难度题查看答案及解析
-
在甲、乙、丙三个不同密闭容器中,按不同方式投料,起始浓度和起始容积相同,一定条件下发生反应:
。相关数据如表所示:下列说法正确的是( )
容器
甲
乙
丙
相关条件
恒温恒容
绝热恒容
恒温恒压
反应物投料n
、
平衡时容器体积
反应的平衡常数K
平衡时
的浓度
平衡时
的反应速率
A.
B.
C.
D.
高三化学单选题困难题查看答案及解析
-
在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g) Fe(s)+CO2(g) △H=a kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是
A. 若生成1 mol Fe,则吸收的热量小于a kJ
B. 若升高温度,正反应速率加快,逆反应速率减慢,则化学平衡正向移动
C. 若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态
D. 达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L
高三化学选择题中等难度题查看答案及解析