-
(11分)实验室制备1,2—二溴乙烷的反应原理如下:CH3CH2OH  CH2=CH2,CH2=CH2+Br2
CH2=CH2,CH2=CH2+Br2  BrCH2CH2Br。用少量的溴和足量的乙醇制备l,2—二溴乙烷的装置如下图所示:
BrCH2CH2Br。用少量的溴和足量的乙醇制备l,2—二溴乙烷的装置如下图所示:
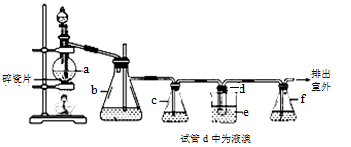
有关数据列表如下:
| 乙醇 | 1,2—二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在装置c中应加入 (选填序号),其目的是吸收反应中可能生成的酸性气体。
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是 。
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的 (填“上”或“下”)层。
(4)若产物中有少量未反应的Br2,最好用 (填正确选项前的序号)洗涤除去。
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),其主要目的是 ;但不用冰水进行过度冷却,原因是: 。
(6)以1,2—二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2—二溴乙烷通过( ① )反应制得( ② ),②通过( ③ )反应制得氯乙烯,由氯乙烯制得聚氯乙烯。
①______________(填反应类型)
②________________(填该物质的电子式)
③______________(填反应类型)
写出第一步的化学方程式_________________。
-
实验室制备 1,2 —二溴乙烷的反应原理如下:①CH3CH2OH在浓硫酸170℃条件下生成CH2=CH2②CH2=CH2与Br2反应生成BrCH2CH2Br。现用少量溴和50gCH3CH2OH制备1,2 —二溴乙烷。回答下列问题:
(1)制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_______。
A 加快反应速度 B 引发反应 C 防止乙醇挥发 D 减少副产物乙醚生成
(2)判断该制备反应已经结束的最简单方法是___________________。
(3)将 1,2 —二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在_____层。
(4)若产物中有少量副产物乙醚,可用____________的方法除去。
(5)若最终得到纯净1,2 —二溴乙烷94g,本实验的产率是__________。
-
实验室制备1,2-二溴乙烷的反应原理如下:
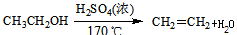 ,CH2=CH2+Br2→ BrCH2CH2Br
,CH2=CH2+Br2→ BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸存在下在140 ℃脱水生成乙醚。用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
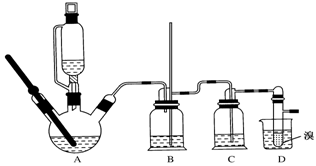
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状 态 | 无 色液 体 | 无 色液 体 | 无 色液 体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170 ℃左右,其最主要目的是___________ ;
(2)在装置C中应加入___________,其目的是吸收反应中可能生成的酸性气体 (填正确选项前的字母); a.水 b.浓硫酸 c.饱和碳酸氢钠溶液 d.氢氧化钠溶液
(3)判断该制备反应已经结束的最简单方法是 ;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在________层(填“上”“下”); 其同系物C4H8Br2有 种同分异构体。
(5)若产物中有少量未反应的Br2,最好用________洗涤除去;(填正确选项前的字母)
a.水 b.碘化钠溶液 c.氢氧化钠溶液 d.乙醇
-
实验室制备1,2二溴乙烷的反应原理如下:CH3CH2OH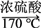 CH2=CH2+H2O,CH2=CH2+Br2―→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
CH2=CH2+H2O,CH2=CH2+Br2―→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
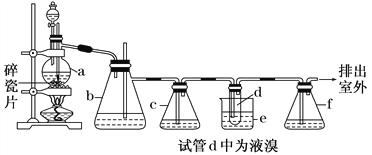
有关数据列表如下:
| 乙醇 | 1,2二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在装置c中应加入________(选填序号),其目的是吸收反应中可能生成的酸性气体。
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)装置b的作用是___________。
(3)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的________(填“上”或“下”)层。
(4)若产物中有少量未反应的Br2,最好用________(填正确选项前的序号)洗涤除去。
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),但不用冰水进行过度冷却,原因是___________________________。
(6)以1,2二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2二溴乙烷通过反应①制得A,A通过反应②制得氯乙烯,由氯乙烯制得聚氯乙烯。
①________________(填反应类型) ②________________(填反应类型)
A________________(填该物质的电子式)
写出第一步反应①的化学方程式_______________________________。
-
实验室制备 1,2-二溴乙烷的反应原理如下:
CH3CH2OH→CH2=CH2
CH2=CH2+B2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在 l40℃脱水生成乙醚。 用少量的溴和足量的乙醇制备 1,2—二溴乙烷的装置如下图所示:

有关数据列表如下:

回答下列问题:
(1) 在此制各实验中,要尽可能迅速地把反应温度提高到 170℃左右,其最主要目的是 ;(填正确选项前的字母)
A.引发反应 B.加快反应速度
C.防止乙醇挥发 D.减少副产物乙醚生成
(2) 在装置 C 中应加入 ,其目的是吸收反应中可能生成的酸性气体: (填正确选项前的字母)
A.水 B.浓硫酸
C.氢氧化钠溶液 D.饱和碳酸氢钠溶液
(3) 判断该制各反应已经结束的最简单方法是 ;
(4) 将 1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在 层(填“上”、“下”);
(5) 若产物中有少量未反应的 Br2,最好用 洗涤除去;(填正确选项前的字母)
A.水 B.氢氧化钠溶液
C.碘化钠溶液 D.乙醇
(6) 若产物中有少量副产物乙醚,可用 的方法除去;
(7) 反应过程中应用冷水冷却装置 D,其主要目的是 ; 但又不能过度冷却 (如用冰水),其原因是 。
-
实验室制备 1,2二溴乙烷的反应原理如下:
CH3CH2OH CH2=CH2+H2O CH2=CH2+Br2―→BrCH2CH2Br
CH2=CH2+H2O CH2=CH2+Br2―→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。用少量溴和足量的乙醇 制备1,2-二溴乙烷的装置如下图所示:
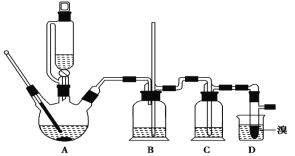
有关数据列表如下:
| 乙醇 | 1 ,2-二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0 .79 | 2.2 | 0 .71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_________。(填正确选项前的字母)
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置 C 中应加入________,其目的是吸收反应中可能生成的酸性气体。(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断 1,2-二溴乙烷制备反应已经结束的最简单方法是_________________________。
(4)将 1,2 二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在__________________层(填“上”、“下”)。
(5)若产物中有少量未反应的 Br2,最好用___________洗涤除去。(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用_____的方法除去。
-
实验室制备1,2二溴乙烷的反应原理如下:
CH3CH2OH CH2===CH2
CH2===CH2
CH2===CH2+Br2→BrCH2CH2B r
r
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140 ℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
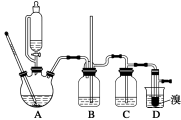
有关数据列表如下:
| 乙醇 | 1,2二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170 ℃左右,其最主要目的是________;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入________,其目的是吸收反应中可能生成的酸性气体;(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是_________________;
(4)将1,2二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在______层(填“上”或“下”);
(5)若产物中有少量未反应的Br2,最好用________洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用__________的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是___________;但又不能过度冷却(如用冰水),其原因是_____________________。
-
实验室制备 1,2-二溴乙烷的反应原理如下:
CH3CH2OH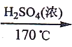 CH2=CH2+H2O
CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在 l40℃脱水生成乙醚。用少量的溴和足量的乙醇制备 1,2-二溴乙烷的装置如下图所示:
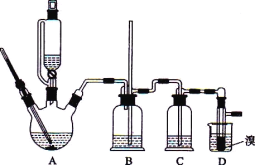
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g∙cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到 170℃ 左右,其最主要目的是_____;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入_____,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)若产物中有少量未反应的 Br2,最好用_____洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(4)判断该制各反应已经结束的最简单方法是_____;
(5)若产物中有少量副产物乙醚,可用_____的方法除去;
(6)反应过程中应用冷水冷却装置D,其主要目的是____;但又不能过度冷却(如用冰水),其原因是_____
-
实验室制备1,2—二溴乙烷的反应原理如下:CH3CH2OH  CH2=CH2+H2O,CH2=CH2+Br2
CH2=CH2+H2O,CH2=CH2+Br2 BrCH2CH2Br。用少量的溴和足量的乙醇制备l,2—二溴乙烷的装置如图所示,有关数据如下表:
BrCH2CH2Br。用少量的溴和足量的乙醇制备l,2—二溴乙烷的装置如图所示,有关数据如下表:

| 乙醇 | 1,2—二溴乙烷 | 乙醚 |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g·cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
⑴在装置c中应加入______(选填序号),其目的是吸收反应中可能生成的酸性气体。
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
⑵将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的________层。(填“上”或“下”)
⑶判断d管中制备二溴乙烷反应已结束的最简单方法是_________________________。
⑷若产物中有少量未反应的Br2,最好用________(填正确选项前的序号)洗涤除去。
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
⑸以1,2—二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2—二溴乙烷通过(①)反应制得(②),②通过(③)反应制得氯乙烯,由氯乙烯制得聚氯乙烯。
①______________(填反应类型),其化学方程式__________________。
②______________(填反应类型)。
-
实验室可用少量的溴和足量的乙醇制备1,2—二溴乙烷,反应原理为:CH3CH2OH CH2=CH2↑+H2O;CH2=CH2+Br2→BrCH2CH2Br。制备装置如图所示:
CH2=CH2↑+H2O;CH2=CH2+Br2→BrCH2CH2Br。制备装置如图所示:
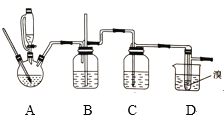
下列说法中不正确的是( )
A.使用恒压低液漏斗的目的是防止有机物挥发,使漏斗内液体顺利滴下
B.实验中为了防止有机物大量挥发,应缓慢升高反应温度至170℃
C.装置C中应加入氢氧化钠溶液,以吸收反应中可能生成的酸性气体
D.实验过程中应用冷水冷却装置D,以避免溴的大量挥发
CH2=CH2,CH2=CH2+Br2
BrCH2CH2Br。用少量的溴和足量的乙醇制备l,2—二溴乙烷的装置如下图所示:

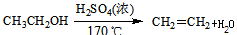 ,CH2=CH2+Br2→ BrCH2CH2Br
,CH2=CH2+Br2→ BrCH2CH2Br
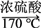 CH2=CH2+H2O,CH2=CH2+Br2―→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:
CH2=CH2+H2O,CH2=CH2+Br2―→BrCH2CH2Br。用少量的溴和足量的乙醇制备1,2二溴乙烷的装置如下图所示:




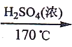 CH2=CH2+H2O
CH2=CH2+H2O

