-
硫酸铵是常见的化肥,是强酸弱碱盐,室温下,可用酸碱滴定法测定其氮元素的含量,但由于NH4+的酸性太弱(Ka=5.6×10-10),直接用NaOH标准溶液滴定有困难,生产和实验室中广泛采用甲醛法测定铵盐中的含氮量。甲醛法是基于甲醛与一定量铵盐作用,生成酸(H+)和六次甲基四铵盐(Ka=7.1×10-6)反应如下:4NH4++ 6HCHO=(CH2)6N4H++ 6H2O+ 3H+,生成物可用酚酞为指示剂,用NaOH标准溶液滴定[在室温下(25℃),通常Ka表示弱酸的电离平衡常数,Kb表示弱碱的电离平衡常数]。硫酸铵含氮量的测定步骤如下:
①准确称取1.800g (NH4)2SO4于烧杯中。
②用适量蒸馏水溶解,然后定量地移至250mL容量瓶中,并用蒸馏水稀释至刻度,摇匀备用。
③用移液管移取试液25mL于锥形瓶中,加入8mL 1:1的甲醛溶液,再加入1~2滴酚酞指示剂摇匀,静置一分钟后,用0.100 mol/L NaOH标准溶液滴定至溶液呈浅红色持续半分钟不褪色,即为终点。
④记录读数,平行做2~3次,NaOH标准溶液滴定消耗的平均体积为27.00mL。
根据实验回答下列问题:
(1)硫酸铵水溶液呈酸性的原因是__________________________________。(用离子方程式说明)
(2)步骤①称取硫酸铵固体样品是否能使用托盘天平______________(填“是”或“否”)。
(3)步骤③加入的甲醛溶液使用前需要加入一定量的NaOH,原因是________________________。
(4)NH4NO3中氮的百分含量是否能用该方法测定______________(填“是”或“否”)。原因是
_________________________________。
(5)据题目给出的信息计算样品中氮的百分含量为_________________ ____。
(6)若室温下,C mol/L氨水的电离平衡常数为Kb,则该氨水的电离度a=_________ ____。(用C
和Kb表示),由此在恒定温度下,你能得出的结论为_________________ ____。
高三化学实验题困难题查看答案及解析
-
(17分)中学化学常见的滴定法包括中和滴定法、氧化还原反应滴定法等。
(1)探究小组甲用酸性KMnO4溶液滴定某补血剂[主要成分硫酸亚铁晶体(FeSO4•7H2O)]中铁元素的含量。
①下列滴定装置中(夹持部分略去),最合理的是: (填字母序号)。
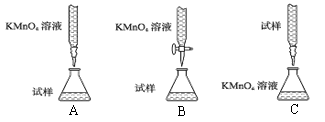
②实验前,首先要准确配制一定物质的量浓度的酸性KMnO4溶液250mL,配制时需要的仪器除托盘天平、玻璃棒、烧杯、胶头滴管、量筒外,还需要 (填仪器名称)。
③该小组拟在同浓度的FeSO4溶液中,探究酸性KMnO4溶液浓度对Fe2+被氧化时反应速率的影响。限选试剂与仪器:0.10mol∙L-1FeSO4、0.02mol∙L-1酸性KMnO4、蒸馏水、锥形瓶、试管、胶头滴管、量筒、秒表。参照下表格式,完成实验表格(列出所选试剂体积和数据;数据用字母表示)。
物理量
实验序号
V[0.10mol∙L-1FeSO4]
/mL
KMnO4溶液褪色所需时间t/s
1
a
t1
2
a
t2
(2)常温下,探究小组乙将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液的pH随加入盐酸体积的变化曲线如右图所示。
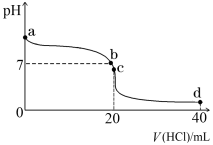
①a点处假设溶液的pH=10,则该点处由水电离产生的c(OH-)= 。
②b点处溶液中c (Cl-) c (NH4+)(填“>”、“<”或“=”)。
③取c点时的饱和溶液并向其加入水玻璃(硅酸钠水溶液),振荡、静置。写出实验现象并用必要的文字和相关离子方程式给予解释: 。
④d点所示溶液中离子浓度由大到小的排序是 。
高三化学实验题困难题查看答案及解析
-
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。为测定补血剂中铁元素的含量,某化学兴趣小组设计了两套实验方案。
方案一 滴定法:用酸性KMnO4溶液滴定,测定铁元素的含量
(1)写出该滴定反应的离子方程式_______________________。
(2)某同学设计的下列滴定方式中,最合理的是________(夹持部分略去)(填字母序号)
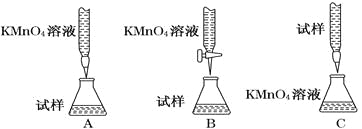
(3)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、药匙、烧杯、胶头滴管外,还需___________(填仪器名称)。
在溶液配制过程中,下列操作会导致配制结果偏低的是___________(填写代号)。
a. 定容时,俯视容量瓶刻度线
b. 容量瓶在使用前内有少量蒸馏水
c. 转移溶液后的烧杯、玻璃棒未洗涤
d. 定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(4)上述实验中KMnO4溶液需要酸化,用于酸化的酸是________。
a.浓盐酸 b.稀硫酸 c.稀硝酸 d.浓硫酸
方案二 称量法:操作流程如下:
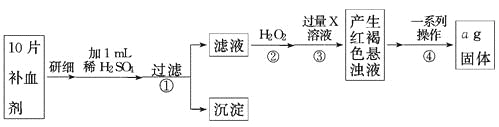
(5)写出步骤②中H2O2氧化Fe2+的离子方程式_______________。
步骤②中除用H2O2外还可以使用的物质是___________
步骤②是否可以省略________,理由是_______________。
(6)步骤④一系列操作依次是:过滤、洗涤、____________、冷却、称量。
(7)假设实验无损耗,则每片补血剂含铁元素的质量________g(用含a的代数式表示)。
高三化学实验题中等难度题查看答案及解析
-
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。为测定补血剂中铁元素的含量,某化学兴趣小组设计了两套实验方案:
方案一 滴定法 用酸性KMnO4溶液滴定测定铁元素的含量。
反应原理:5Fe2++MnO4—+8H+===5Fe3++Mn2++4H2O
(1)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需________(填仪器名称)。
(2)上述实验中KMnO4溶液需要酸化,用于酸化的酸是________。
A.稀硫酸 B.浓硝酸 C.稀硝酸 D.稀盐酸
(3)某同学设计的下列滴定方式中,最合理的是________(夹持部分略去)(填字母序号)。
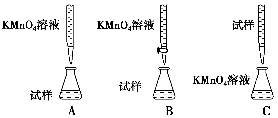
方案二 重量法 操作流程如下:

(4)步骤②中除用H2O2外还可以使用的物质是__________________________。
(5)步骤②是否可以省略________,理由是________________________________
_______________________________________。
(6)步骤④中一系列操作依次是:过滤、洗涤、________、冷却、称量。
(7)假设实验无损耗,则每片补血剂含铁元素的质量________g(用含a的代数式表示)。
高三化学实验题困难题查看答案及解析
-
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。为测定补血剂中铁元素的含量,某化学兴趣小组设计了两套实验方案
方案一 滴定法:用酸性KMnO4溶液滴定,测定铁元素的含量
(1)写出该滴定反应的离子方程式 。
(2)某同学设计的下列滴定方式中,最合理的是___________(夹持部分略去)(填字母序号)
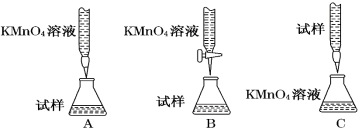
(3)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250 mL,配制时需要的仪器除天平、药匙、烧杯、胶头滴管、玻璃棒外,还需 (填仪器名称)。在溶液配制过程中,下列操作会导致配制结果偏低的是___________(填写代号)。
a.定容时,俯视容量瓶刻度线
b.容量瓶在使用前内有少量蒸馏水
c.转移溶液后的烧杯、玻璃棒未洗涤
d.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(4)上述实验中KMnO4溶液需要酸化,用于酸化的酸是________。
A.浓盐酸 B.稀硫酸 C.稀硝酸 D.浓硫酸
方案二 称量法:操作流程如下:

(5)写出步骤②中H2O2氧化Fe2+ 的离子方程式 。步骤②中除用H2O2外还可以使用的物质是 ,步骤②是否可以省略 ,理由是 。
(6)步骤④一系列操作依次是:过滤、洗涤、 、冷却、称量。
(7)假设实验无损耗,则每片补血剂含铁元素的质量 g(用含a的代数式表示)。
高三化学实验题极难题查看答案及解析
-
配制某补血剂主要成分是硫酸亚铁晶体(FeSO4·7H2O),为测定该补血剂中铁元素的含量,某化学兴趣小组设计用滴定法(用酸性KMnO4溶液滴定),主要步骤如下:①取一定量补血剂样品,溶解除去不溶物(不损耗铁元素),并配制成250mL待测溶液;②量取25.00mL待测溶液于锥形瓶中;③用酸化的0.0100mol/LKMn04溶液滴定至终点,记录消耗KMnO4溶液体积,重复一到两次实验。(已知:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O)
(1)配制250mL待测溶液时需要的玻璃仪器除烧杯、胶头滴管外,还需_________(填仪器名称);滴定时,左手控制滴定管的活塞,右手摇动锥形瓶,眼睹注视__________;当看到_________时,达滴定终点;
(2)滴定操作中,锥形瓶残留少量蒸馏水,则测定结果_____________(填“偏高”“偏低”或“无影响”下同);达到滴定终点时,尖嘴处尚有一滴液滴未滴下,则测定的结果_____________。
高三化学实验题困难题查看答案及解析
-
配制某补血剂主要成分是硫酸亚铁晶体(FeSO4•7H2O),为测定该补血剂中铁元素的含量,某化学兴趣小组设计了两套实验方案.
方案一:滴定法(用酸性KMnO4溶液滴定),主要步骤如下:
①取一定量补血剂样品,溶解除去不溶物(不损耗铁元素),并配制成250mL待测溶液;
②量取25.00mL待测溶液于锥形瓶中;
③用酸化的0.0100mol/LKMnO4溶液滴定至终点,记录消耗KMnO4溶液体积,重复一到两次实验.
(已知:5Fe 2++MnO4﹣+8H+→5Fe 3++Mn2++4H2O).
(1)250mL待测溶液时需要的玻璃仪器除烧杯、胶头滴管外,还需 (填仪器名称);滴定时,左手控制滴定管的活塞,右手摇动锥形瓶,眼睛注视 ;当看到 时,达滴定终点.
(2)上述实验中的KMnO4溶液需要酸化,若分别用下列酸进行酸化,对测定结果的影响是:硝酸 ,硫酸 ,盐酸 .(填“偏大”、“偏小”或“无影响”)
(3)方案二:重量法(将FeSO4转化为Fe2O3,测定质量),操作流程如下:
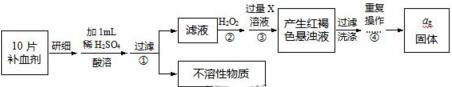
步骤①加入1ml稀硫酸的目的是 .
(4)步骤②是否可以省略 ,理由是 .
(5)步骤④中重复操作加热、冷却、称量,直到 为止.
(6)假设实验中铁元素无损耗,则每片补血剂含铁元素的质量 g(用含a的代数式表示).
高三化学实验题困难题查看答案及解析
-
下列陈述I、II均正确且有因果关系的是
陈述I
陈述II
1
常温下铁与浓硫酸不反应
可用铁槽车密封运送浓硫酸
2
NaHCO3溶于水完全电离
NaHCO3是强电解质
3
NH4Cl为强酸弱碱盐
用加热法除去NaCl中的NH4Cl
4
H2O2、SO2能使酸性KMnO4溶液褪色
H2O2表现还原性,SO2表现漂白性
A.1 B.2 C.3 D.4
高三化学选择题简单题查看答案及解析
-
下列陈述Ⅰ、Ⅱ均正确且有因果关系的是
选项
陈述Ⅰ
陈述Ⅱ
A
常温下铁与浓硫酸不反应
可用铁槽车密封运送浓硫酸
B
NaHCO3溶于水完全电离
NaHCO3是强电解质
C
NH4Cl为强酸弱碱盐
用加热法除去NaCl中的NH4Cl
D
H2O2、SO2都能使酸性KMnO4溶液褪色
H2O2表现还原性、SO2表现漂白性
高三化学选择题中等难度题查看答案及解析
-
下列陈述I、Ⅱ均正确且有因果关系的是
选项 陈述I 陈述Ⅱ
A 常温下铁与浓硫酸不反应 可用铁槽车密封运送浓硫酸
B NaHCO3溶于水完全电离 NaHCO3是强电解质
C NH4Cl为强酸弱碱盐 用加热法除去NaCl中的NH4Cl
D H2O2、SO2都能使酸性KMnO4溶液褪色 H2O2表现还原性,SO2表现漂白性
高三化学选择题中等难度题查看答案及解析