某研究性学习小组同学设计了如下图制取氯气(药品:MnO2和浓盐酸)并验证其性质的实验装置。
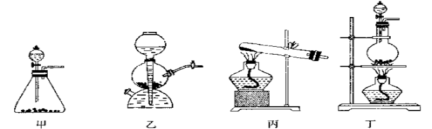
请回答下列问题:(1)该实验中A部分的装置是 (填写装置的序号)
(2)A中发生反应一段时间后,B中的现象是 ;
整套实验装置存在的明显缺陷是 。
(3)写出D装置中发生反应的离子方程式: 。
(4)请你帮该小组同学设计一个实验,证明洗气瓶C中的已被氧化(简述实验步骤): 。
高一化学实验题中等难度题
某研究性学习小组同学设计了如下图制取氯气(药品:MnO2和浓盐酸)并验证其性质的实验装置。

请回答下列问题:(1)该实验中A部分的装置是 (填写装置的序号)

(2)A中发生反应一段时间后,B中的现象是 ;
整套实验装置存在的明显缺陷是 。
(3)写出D装置中发生反应的离子方程式: 。
(4)请你帮该小组同学设计一个实验,证明洗气瓶C中的已被氧化(简述实验步骤): 。
高一化学实验题中等难度题
某研究性学习小组同学设计了如下图制取氯气(药品:MnO2和浓盐酸)并验证其性质的实验装置。

请回答下列问题:(1)该实验中A部分的装置是 (填写装置的序号)

(2)A中发生反应一段时间后,B中的现象是 ;
整套实验装置存在的明显缺陷是 。
(3)写出D装置中发生反应的离子方程式: 。
(4)请你帮该小组同学设计一个实验,证明洗气瓶C中的已被氧化(简述实验步骤): 。
高一化学实验题中等难度题查看答案及解析
氯气是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药、染料和药品,为研究氯气,某研究性学习小组利用下列装置制取并验证氯气部分化学性质,请回答下列问题:
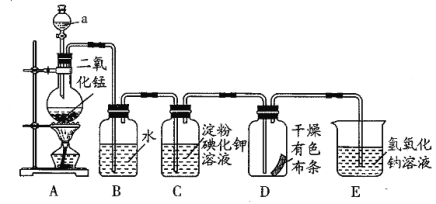
(1)装置A中,仪器a的名称为___,该装置中发生反应的化学方程式:___;34.8gMnO2完全反应生成Cl2体积为___(标准状况下)。
(2)当Cl2气流通过一段时间后,装置B中溶液的pH___(填“>”“<”或“=”)7,写出Cl2与水反应的离子方程式:___。
(3)当有少量Cl2气流通过后,观察到装置C中的溶液变为___色,反应的离子方程式为___。
(4)当Cl2气流持续通过时,装置D中干燥的有色布条能否褪色?为什么?___。
(5)装置E的作用是___。
高一化学实验题中等难度题查看答案及解析
为了探究和验证氯气的性质,某研究性学习小组以MnO2和浓盐酸为主要原料,设计了如图所示装置(其中a是连有注射器针头的橡皮管,针头已插入并穿过橡皮塞)进行了研究。
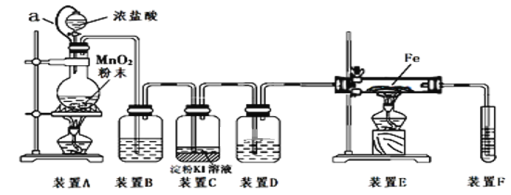
(资料:氯气与铁反应制取氯化铁要在无水条件下进行)
试回答下列问题:
(l)装置A中发生反应的化学方程式为_____________________。
(2)装置B中的试剂为_________,装置D作用是________。
(3)装置C中发生反应的离子方程式为_____________________________。
(4)反应开始后,装置E发生反应的化学方程式为____________________________。
(5)装置F中发生反应的化学方程式为________________________。
高一化学实验题中等难度题查看答案及解析
某研究性学习小组的同学利用MnO2和浓盐酸反应来制取干燥的氯气并验证其有无漂白性,所用装置(数量可满足需要,不含制气装置)如下,下列说法正确的是( )
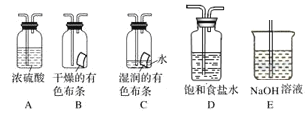
A. 装置E中发生反应的离子方程式为:Cl2+OH-=Cl-+ClO-+H2O
B. 按气流流动的先后顺序,装置连接顺序依次为DABAE
C. 装置E的主要用途是制备NaClO
D. 装置D的作用是除去氯气中的HCl并提供水蒸气以验证HClO具有漂白性
高一化学单选题中等难度题查看答案及解析
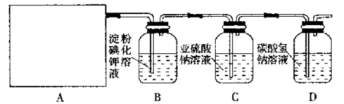
某研究性学习小组查阅资料得知,漂白粉与硫酸溶液加热反应可制取氯气,他们设计如下实验用于制取氯气并验证其性质。
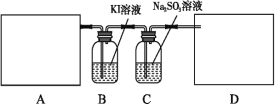
试回答:
(1)该实验中A部分的装置是___________ (填写字母)。A部分的装置中发生反应的化学方程式为:___________。
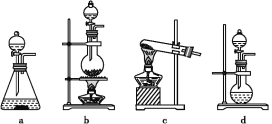
(2)B中的发生反应的离子方程式为____________。
(3)用离子方程式表示C中亚硫酸钠被氧化的主要原因:___________。请你帮助他们设计一个实验,证明洗气瓶C中的亚硫酸钠已被氧化(简述实验步骤)__________。
(4)请根据题意画出D处的实验装置图,并注明盛放的物质___________。
高一化学实验题中等难度题查看答案及解析
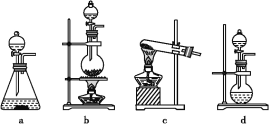
某研究性学习小组查阅资料得知,漂白粉与硫酸溶液加热反应可制取氯气,他们设计如下实验用于制取氯气并验证其性质。
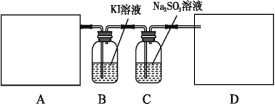
试回答:
(1)该实验中A部分的装置是___________ (填写字母)。A部分的装置中发生反应的化学方程式为:___________。
(2)B中的发生反应的离子方程式为____________。
(3)用离子方程式表示C中亚硫酸钠被氧化的主要原因:___________。请你帮助他们设计一个实验,证明洗气瓶C中的亚硫酸钠已被氧化(简述实验步骤)__________。
(4)请根据题意画出D处的实验装置图,并注明盛放的物质___________。
高一化学实验题中等难度题查看答案及解析
某化学学习小组为制取氯气并验证氯气的化学性质,设计了如下实验装置,请按要求回答问题。已知各试剂瓶装的试剂为:B(H2S的水溶液)、C(KI淀粉溶液)、D(FeBr2溶液)、E(混有SO2的BaCl2溶液)、F(水)、H(紫色石蕊溶液)
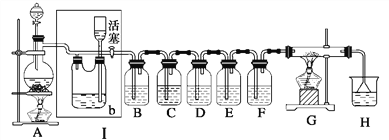
(1)A是氯气发生装置,其化学反应方程式是________________________________。
(2)Ⅰ中b瓶内加入的液体最好是________。
(3)B中产生淡黄色的单质硫沉淀,请写出反应的化学方程式:______________________
(4)C中的实验现象为______________________
(5)D中的实验现象为______________________
(6)E中产生白色沉淀,共发生了两个反应,请写出发生的氧化还原反应的离子方程式:____________________________________
(7)G装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为二氧化碳和氯化氢。请写出G中发生反应的化学方程式:_____________________________________。
(8)H中的实验现象为____________________________________________,其原因是___________________________________________________________。
【答案】 MnO2+4HCl(浓)MnCl2+2H2O+Cl2↑ 饱和食盐水 H2S+Cl2=S↓+2HCl 溶液变蓝 溶液由浅绿色变为橙黄色(或溶液由浅绿色变为黄色,最后变为橙黄色) SO2+Cl2+2H2O=SO42—+2Cl—+4H+ C+2H2O+2Cl2
CO2+4HCl 紫色石蕊试液的颜色由紫色变为红色,再变为无色 氯气与水反应生成的HCl使紫色石蕊试液变红色,生成的次氯酸有漂白性,使红色褪去
【解析】本题考查实验方案设计与评价,(1)实验室制备Cl2,常用MnO2和浓盐酸的反应,反应方程式为MnO2+4HCl(浓)MnCl2+2H2O+Cl2↑;(2)制备的氯气中混有HCl和水蒸气,HCl可能对后续实验产生干扰,因此必须除去,除去Cl2中HCl,常用饱和食盐水,即b中盛放的是饱和食盐水;(3)氯气的氧化性强于S,因此发生离子反应方程式为Cl2+H2S=S↓+2HCl;(4)氯气的氧化性强于I2,因此发生Cl2+2I-=2Cl-+I2,淀粉与碘单质显蓝色,因此实验现象是溶液变蓝;(5)还原性:Fe2+>Br-,因此通入氯气先发生:Cl2+2Fe2+=2Fe3++2Cl-,Cl2+2Br-=2Cl-+Br2,现象是溶液由浅绿色变为黄色,最后变为橙黄色;(6)E中产生白色沉淀,发生的离子反应方程式为Cl2+SO2+H2O=4H++SO42-+2Cl-,Ba2++SO42-=BaSO4↓,前者属于氧化还原反应,后者不属于氧化还原反应;(7)根据题意,G中发生化学反应方程式为C+2H2O+2Cl2
CO2+4HCl;(8)氯气与水反应生成的HCl使紫色石蕊试液变红色,生成的次氯酸有漂白性,使红色褪去,因此现象是紫色石蕊试液的颜色由紫色变为红色,再变为无色。
【题型】实验题
【结束】
22
常见物质A~K之间存在如下图所示的转化关系,其中D、E为单质,请回答下列问题(图中有些反应的产物和反应的条件没有全部标出)。
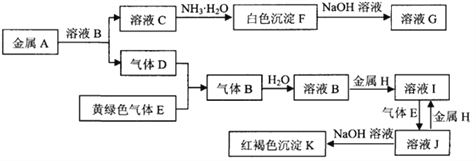
(1)写出下列物质中溶质的名称:B是 __________,G是____________
(2)反应“F→G”的化学方程式是_____________________________________________
(3)反应“J→I”的离子方程式是_____________________________________________
(4)溶液I中混有溶液J,除去J的方法是:________________________________________________________________
(5)检验溶液I中阳离子的方法是:__________________________
高一化学推断题中等难度题查看答案及解析
某化学学习小组为制取氯气并验证氯气的化学性质,设计了如下实验装置,请按要求回答问题。已知各试剂瓶装的试剂为:B(H2S的水溶液)、C(KI淀粉溶液)、D(FeBr2溶液)、E(混有SO2的BaCl2溶液)、F(水)、H(紫色石蕊溶液)

(1)A是氯气发生装置,其化学反应方程式是________________________________。
(2)Ⅰ中b瓶内加入的液体最好是________。
(3)B中产生淡黄色的单质硫沉淀,请写出反应的化学方程式:______________________
(4)C中的实验现象为______________________
(5)D中的实验现象为______________________
(6)E中产生白色沉淀,共发生了两个反应,请写出发生的氧化还原反应的离子方程式:____________________________________
(7)G装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为二氧化碳和氯化氢。请写出G中发生反应的化学方程式:_____________________________________。
(8)H中的实验现象为____________________________________________,其原因是___________________________________________________________。
高一化学实验题中等难度题查看答案及解析
某实验小组用MnO2与浓盐酸混合加热制Cl2,并将 制得的氯气与潮湿的Ca(OH)2 固体反应制取少量漂白粉.实验装置如下图:回答下列问题
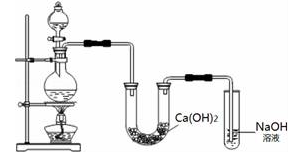
(1)装置的分液漏斗所盛的药品是(写名称) ; 漂白粉的有效成分是(写化学式) .
(2)装置的试管中发生的主要反应的化学方程式是 .
(3)用KClO3代替MnO2与浓盐酸混合,在常温下也能产生Cl2,试写出该反应的化学方程式 .
高一化学实验题中等难度题查看答案及解析
某化学兴趣小组欲在实验室探究氯气的性质及模拟工业制取漂白粉,设计了如下装置进行实验(实验室制取氯气的反应为MnO2 + 4 HCI(浓)MnCl2 + C12↑+ 2 H2O):
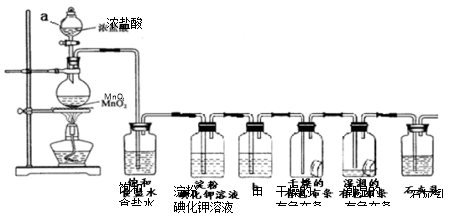
请按要求回答下列问题:
(1)淀粉碘化钾溶液中观察到的现象是_________,反应的离子方程式____________。
(2)若干燥的有色布条不褪色,湿润的有色布条褪色,则甲中盛放________(填名称)。
(3)C12与石灰乳反应制取漂白粉的化学方程式为___________________。
(4)该兴趣小组用8.7g MnO2与足量的浓盐酸制备氯气,则理论上最多可制得标准状况下的Cl2______________L。
高一化学实验题中等难度题查看答案及解析