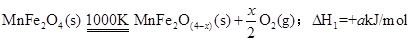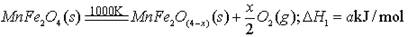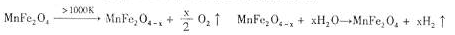-
[化学选修2:化学与技术]工业上为了使原料和能量得到充分的利用,常常采用循环操作.
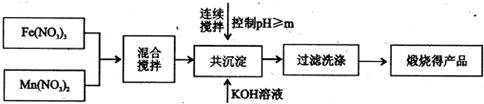
Ⅰ、利用热化学循环制氢能缓解能源矛盾.最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢.MnFe2O4的制备:
已知Fe3+、Mn2+沉淀的pH如表所示.
| 开始沉淀 | 完全沉淀 |
| Fe3+ | 2.7 | 4.2 |
| Mn2+ | 8.3 | 10.4 |
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比应为______.
(2)控制pH的操作中m的值为______.
Ⅱ、用MnFe2O4热化学循环制取氢气:MnFe2O4(s) MnFe2O(4-x)(s)+
MnFe2O(4-x)(s)+ 8O2(g);△H1=akJ/mol,
8O2(g);△H1=akJ/mol,
MnFe2O(4-x)(s)+xH2O(l)═MnFe2O4(s)+xH2(g);△H2=bkJ/mol,
(3)由上可知,H2燃烧的热化学方程式是______.
(4)该热化学循环制取氢气的优点是______(填字母编号).
A.过程简单、无污染 B.物料可循环使用 C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl通过如图的循环流程制取太阳能材料高纯硅.
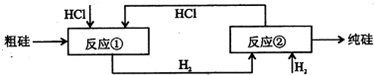
反应①Si(粗)+3HCl(g) SiHCI3(l)+H2(g)
SiHCI3(l)+H2(g)
反应②:SiHCl3(l)+H2(g) Si(纯)+3HCl(g)
Si(纯)+3HCl(g)
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%.则在下一轮次的生产中,需补充投入HCl和H2的体积比是______.
-
【化学选修2:化学与技术】(15分)
工业上为了使原料和能量得到充分的利用,常常采用循环操作。
I、利用热化学循环制氢能缓解能源矛盾。最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢。MnFe2O4的制备:
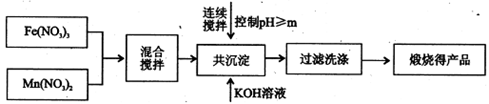
已知Fe3+、Mn2+沉淀的pH如右表所示。
| 开始沉淀 | 完全沉淀 |
| Fe3+ | 2.7 | 4.2 |
| Mn2+ | 8.3 | 10.4 |
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比应为________。
(2)控制pH的操作中m的值为________。
II、用MnFe2O4热化学循环制取氢气:
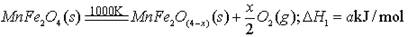

(3)由上可知,H2燃烧的热化学方程式是________。
(4)该热化学循环制取氢气的优点是________(填字母编号)。
A.过程简单、无污染 B.物料可循环使用
C.氧气和氢气在不同步骤生成,安全且易分离
III、工业上可用H2、HCl通过下图的循环流程制取太阳能材料高纯硅。
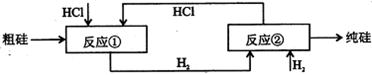
反应①
反应②:
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%。则在下一轮次的生产中,需补充投入HCl和H2的体积比是________。
-
(15分)工业上为了使原料和能量得到充分的利用,常常采用循环操作。
Ⅰ、利用热化学循环制氢能缓解能源矛盾。最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢。
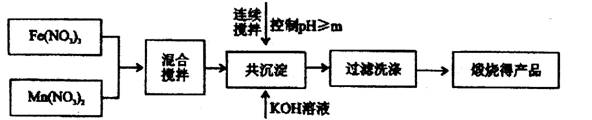
MnFe2O4的制备:
| 开始沉淀 | 完全沉淀 |
| Fe3+ | 2.7 | 3.7 |
| Mn2+ | 8.3 | 10.4 |
已知Fe3+、Mn2+沉淀的pH如右表所示。
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质
的量之比应为 __________。
(2)控制pH的操作中m的值为 。
Ⅱ、用MnFe2O4热化学循环制取氢气:
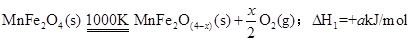

(3)由上可知,表示H2燃烧热的热化学方程式是__________________________ 。
(4)该热化学循环制取氢气的优点是_______________(填字母编号)。
A.过程简单、无污染
B.物料可循环使用
C.氧气和氢气在不同步骤生成,安全且易分离
Ⅲ、工业上可用H2、HCl在一定条件下通过下图的循环流程制取太阳能材料高纯硅。
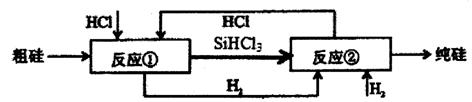
(5)上图中,假设在每一轮次的投料生产中,硅元素没有损失,反应①中HCl的利用率和反应②中H2的利用率均为75%。则在下一轮次的生产中,需补充投入HCl和H2的体积比是___________________。
-
随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐。最近的研究发现,复合氧化物铁酸锰(MnFe2O4)也可以用于热化学循环分解水制氢,MnFe2O4的制备流程如下:
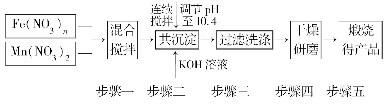
(1)原料Fe(NO3)n中n=________,投入原料Fe(NO3)n和Mn(NO3)2的物质的量之比应为________。
(2)步骤二中“连续搅拌”的目的是__________________________________________
步骤三中洗涤干净的标准是________________________________________________
(3)利用MnFe2O4热化学循环制氢的反应可表示为:
MnFe2O4 MnFe2O4-x+O2↑;
MnFe2O4-x+O2↑;
MnFe2O4-x+xH2O MnFe2O4+xH2↑
MnFe2O4+xH2↑
请认真分析上述两个反应并回答下列问题:
①若MnFe2O4-x中x=0.8,则MnFe2O4-x中Fe2+占全部铁元素的百分率为________。
②该热化学循环制氢法的优点有_____________________、________________________ (答两点即可)。
该热化学循环法制氢尚有不足之处,进一步改进的研究方向是___________________________________________________________。
-
随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐.最近的研究发现,复合氧化物铁酸锰(MnFe2O4)也可以用于热化学循环分解水制氢,MnFe2O4的制备流程如下:

(1)原料Fe(NO3)n中n=______,投入原料Fe(NO3)n和Mn(NO3)2的物质的量之比为______.
(2)步骤二中连续搅拌的目的是:______,步骤三中洗涤干净的标准是______.
(3)利用MnFe2O4热化学循环制氢的反应可表示为:
MnFe2O4 MnFe2O4-x+
MnFe2O4-x+ O2↑,MnFe2O4-x+xH2O→MnFe2O4+xH2↑
O2↑,MnFe2O4-x+xH2O→MnFe2O4+xH2↑
请认真回答下列问题:
①若MnFe2O4-x中x=0.8,则MnFe2O4-x中Fe2+占全部铁元素的百分率为:______
②该化学循环制氢的优点是:______
③该化学循环法制氢尚有不足之处,进一步改进的研究方向是:______.
-
随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐。最近的研究发现,复合氧化物铁酸锰(MnFe2O4)也可以用于热化学循环分解水制氢,MnFe2O4的制备流程如下:
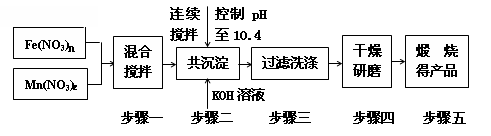
(1)原料Fe(NO3)n中n=______,投入原料Fe(NO3)n和Mn(NO3)2的物质的量之比应为______。
(2)步骤二中“连续搅拌”的目的是_________________________________________;
步骤三中洗涤干净的标准是________________________________________。
(3)利用MnFe2O4热化学循环制氢的反应可表示为:
MnFe2O4  MnFe2O4-x +
MnFe2O4-x +  O2↑MnFe2O4-x + xH2O→MnFe2O4 + xH2↑,
O2↑MnFe2O4-x + xH2O→MnFe2O4 + xH2↑,
请认真分析上述两个反应并回答下列问题:
①若MnFe2O4-x中x=0.8,则MnFe2O4-x中Fe2+占全部铁元素的百分率为_______。
②该化学循环制氢的优点有(答两点即可)
_____________________________________________________________________。
③该热化学循环法制氢尚有不足之处,进一步改进的研究方向是_________。
-
[化学一选修2:化学与技术](15分)随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐。最近的研究发现,复合氧化物铁酸锰(MnFe2O4)也可以用于热化学循环分解水制氢,MnFe2O4的制备流程如下:
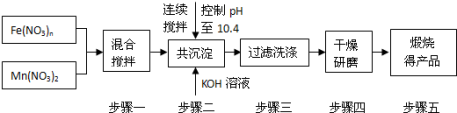
(1)原料Fe(NO3)n中n= ,投入原料Fe(NO3)n和Mn(NO3)2的物质的量之比应为 。
(2)步骤二中“连续搅拌”的目的是 ;步骤三中洗涤干净的标准是 。
(3)利用MnFe2O4热化学循环制氢的反应可表示为:
MnFe2O4 MnFe2O4-x+
MnFe2O4-x+ O2↑
O2↑
MnFe2O4+xH2O=MnFe2O4+xH2↑
请认真分析上述两个反应并回答下列问题:
①若MnFe2O4-x中x=0.8,则MnFe2O4-x中Fe2+占全部铁元素的百分比为 。
②该热化学循环法制氢的优点有(答两点即可) 。
③该热化学循环法制氢尚有不足之处,进一步改进的研究方向是 。
-
(15分)
随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐。最近的研究发现,复合氧化物铁酸锰(MnFe2O4)也可以用于热化学循环分解水制氢,MnFe2O4的制备流程如下:

(1)原来Fe(NO3)n中n=________ ,投入原料Fe(NO3)n和Mn(NO3)2的物质的量之比应为________。
(2)步骤二中“连续搅拦”的目的是________;
步骤三中洗涤干净的标准是________。
(3)利用MnFe2O4热化学循环制氢的反应可表示为:
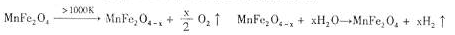
请认真分析上述两个反应并回答下列问题:
①项MnFe2O4-x中x=0.8,则MnFe2O4-x中Fe2+占全部铁元素的百分率为________。
②热化学循环制氢的优点有(答两点即可)________。
③该热化学循环法制氢尚有不足之处,进一步改进的研究方向是________。
-
(15分)
随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐。最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢。
Ⅰ.MnFe2O4的制备:
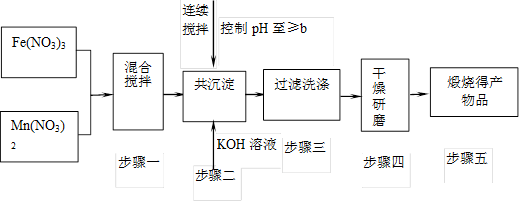

 已知Fe3+、Mn2+沉淀的pH为下表所示。
已知Fe3+、Mn2+沉淀的pH为下表所示。
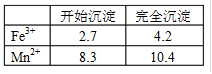
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2
 的物质的量之比应为________。
的物质的量之比应为________。
(2)步骤二中b的值为________。
 (3)步骤三中洗涤干净的标准是________。
(3)步骤三中洗涤干净的标准是________。
Ⅱ.用MnFe2O4热化学循环制氢:
 MnFe2O4(s)→MnFe2O(4-x)(s) +
MnFe2O4(s)→MnFe2O(4-x)(s) +  O2(g);△H1
O2(g);△H1
MnFe2O(4-x)(s)+ xH2O →MnFe2O4(s) + xH2(g);△H2
 请回答下列问题:
请回答下列问题:
(4) 若MnFe2O(4-x)中x=0.8,则MnFe2O(4-x)中Fe2+在全部铁元素中的质量分数为________。
 (5)该热化学循环制氢的优点有________(填序号)。
(5)该热化学循环制氢的优点有________(填序号)。
A.过程简单、无污染 B.物料可循环使用  C.氧气和氢气在不同步骤生成,安全且易分离
C.氧气和氢气在不同步骤生成,安全且易分离
(6)已知 2H2(g)+O2(g)= 2H2O(g);△H3
 则:△H3与△H1、△H2的关系为△H3=。
则:△H3与△H1、△H2的关系为△H3=。
-
随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐.最近研究发现,复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢.
Ⅰ.MnFe2O4的制备:
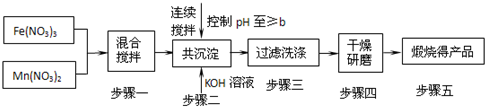
已知Fe3+、Mn2+沉淀的pH为表所示.
| 开始沉淀 | 完全沉淀 |
| Fe3+ | 2.7 | 4.2 |
| Mn2+ | 8.3 | 10.4 |
(1)此工艺中理论上投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比应为________.
(2)步骤二中b的值为________.
(3)步骤三中洗涤干净的标准是________.
Ⅱ.用MnFe2O4热化学循环制氢:
MnFe2O4(s) MnFe2O(4-x)(s)+
MnFe2O(4-x)(s)+ O2(g)△H1
O2(g)△H1
MnFe2O(4-x)(s)+xH2O→MnFe2O4(s)+xH2(g)△H2
请回答下列问题:
(4)若MnFe2O(4-x)中x=0.8,则MnFe2O(4-x)中Fe2+占全部铁元素的百分率为________.
(5)该热化学循环制氢的优点有________(填序号).
A.过程简单、无污染 B.物料可循环使用
C.氧气和氢气在不同步骤生成,安全且易分离
(6)已知 2H2(g)+O2(g)=2H2O(g)△H3则:△H3与△H1、△H2的关系为△H3=________.