-
向2L 的密闭容器中充入7.6molNO 和 3.8mol O2 ,发生如下反应:
①2NO(g)+O2(g) 2NO2 (g) ②2NO2 (g)
2NO2 (g) ②2NO2 (g)  N2O4 (g)测得 NO2和N2O4 的浓度变化如图所示,0~10min 维持容器温度为T1℃,10min 后升高并维持容器的温度为 T2℃。下列说法正确的是
N2O4 (g)测得 NO2和N2O4 的浓度变化如图所示,0~10min 维持容器温度为T1℃,10min 后升高并维持容器的温度为 T2℃。下列说法正确的是
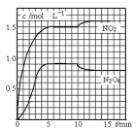
A.前 5min 反应的平均速率 v(N2O4)=0.36mol·L-1 ·min-1
B.T1℃时反应②的化学平衡常数K=0.6
C.若起始时向该容器中充入3.6molNO 2和 2.0mol N2 O4 ,T 1 ℃达到平衡时,N2O4的转化率为10%
D.反应①、②均为吸热反应
-
向2 L的密闭容器中充入7.6 mol NO和3.8 mol O2,发生如下反应:
①2NO(g)+O2(g)=2NO2(g) ②2NO2(g) N2O4(g)
N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10 min维持容器温度为T1℃,10 min后升高并维持容器的温度为T2℃。
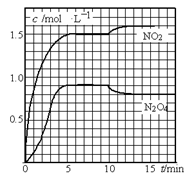
(1)计算前5 min N2O4反应的平均速率。
(2)计算T1℃时反应②的化学平衡常数。
(3)若起始时向该容器中充入3.6 mol NO2和2.0 mol N2O4,判断T1℃时反应②进行的方向,并计算达到平衡时N2O4的物质的量。
-
向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
①2NO(g)+O2(g) 2NO2(g)
2NO2(g)
②2NO2(g) N2O4(g)
N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃。下列说法正确的是
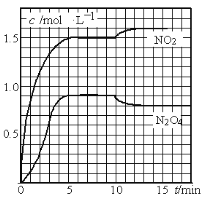
A. 前5min的平均反应速率v(N2O4)=0.18mol·L-1·s-1
B. T1℃时反应②的化学平衡常数K=0.6
C. 反应①、②均为吸热反应
D. 若起始时向该容器中充入3.6mol NO2和2.0mol N2O4,T1℃达到平衡时,N2O4的转化率为10%
-
向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
①2NO(g)+O2(g) 2NO2(g)
2NO2(g)
②2NO2(g) N2O4(g)
N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃。下列说法正确的是
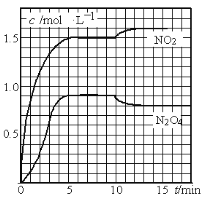
A.前5min的平均反应速率v(N2O4)=0.18mol·L-1·s-1
B.T1℃时反应②的化学平衡常数K=0.6
C.反应①、②均为吸热反应
D.若起始时向该容器中充入3.6mol NO2和2.0mol N2O4,T1℃达到平衡时,N2O4的转化率为10%
-
一定温度下,向aL的密闭容器中加入2molNO2(g), 发生如下反应:2NO2  2NO + O2, 此反应达到平衡状态的标志是( )
2NO + O2, 此反应达到平衡状态的标志是( )
A.单位时间内生成2n molNO同时生成2n molNO2
B.单位时间内生成2 n molNO同时生成n molO2
n molNO同时生成n molO2
C.混合气体中NO2、NO和O2的物质的量之比为2﹕2﹕1
D.混合气体中NO2体积分数为50%
-
在恒温恒容密闭容器中发生反应2NO2 2NO+O2,不能说明反应达到平衡状态的是( )
2NO+O2,不能说明反应达到平衡状态的是( )
A. 2v(O2)=v(NO2) B. 单位时间内生成n mol O2的同时生成2n molNO2
C. 混合气体的颜色不再改变 D. 混合气体的平均相对分子质量不再改变
-
一定温度下,向aL密闭容器中加入1molO2和2molNO,发生如下反应:O2(g)+2NO(g) 2NO2(g),下列条件下,此反应不一定达平衡的是( )
2NO2(g),下列条件下,此反应不一定达平衡的是( )
A.容器内压强不随时间变化
B.容器内各物质的浓度不随时间变化
C.容器内O2、NO、NO2的浓度之比为1∶2∶2
D.单位时间内生成1molO=O,同时生成2molNO2
-
已知在150℃时,NO2按下式发生分解反应2NO2 2NO+O2 △H>0。向容积为1L的密闭容器中加入0.05molNO2在150℃时充分反应,达到平衡后测得c(NO)=0.04mol/L,吸收热量akJ。
2NO+O2 △H>0。向容积为1L的密闭容器中加入0.05molNO2在150℃时充分反应,达到平衡后测得c(NO)=0.04mol/L,吸收热量akJ。
(1)能说明上述反应已经达到化学平衡状态的是 。
A.容器内气体的颜色不再变化
B.容器内压强不再变化
C.容器内气体的密度 不再变化
不再变化
D.容器内气体的平均摩尔质量不再变化
E.v逆(NO2)=v正(NO)
F.相同时间内每消耗2个NO2分子的同时,生成2个NO分子
(2)下列有关该反应的图像中正确的是 。

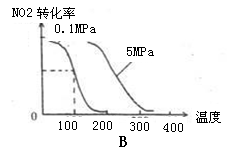
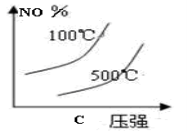
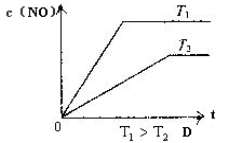
(3)若从反应开始至c(NO)=0.04mol/L共耗时5分钟,则用O2表示的平均反应速率为 。
(4)150℃时上述反应的平衡常数数值为 (可不写单位)。
(5)若在相同的容器内开始时只加入0.05molNO和0.025molO2,在相同的温度下充分反应达到平衡后,恰好放出akJ的热量,则此时O2的转化率为 。
(6)恒容条件下,下列措施中能使n(NO2)/ n(NO)增大的有 。
A.降低温度 B.充入He气
C.再充入1 mol NO (g)和0.5 mol O2(g) D.使用催化剂
-
一定温度下, 向aL的密闭容器中加入2molNO2(g), 发生如下反应:2NO2 2NO+O2, 此反应达到平衡的标志是 ( )
2NO+O2, 此反应达到平衡的标志是 ( )
A. 单位时间内生成2nmolNO同时生成2nmolNO2
B. 混合气体中NO2、NO和O2的物质的量之比为2:2:1
C. 单位时间内生成2nmolNO同时生成nmolO2
D. 混合气体的颜色变浅
-
向2L密闭容器中加入1molNO和1mol活性炭,发生反应:2NO(g)+C(s)  N2(g)+CO2(g) △H = - 213.5kJ/mol,达到平衡的数据如下:
N2(g)+CO2(g) △H = - 213.5kJ/mol,达到平衡的数据如下:
| 温度/℃ | n(活性炭)/mol | n(CO2)/mol |
| T1 | 0.70 | —— |
| T2 | —— | 0.25 |
下列说法不正确的是( )
A. 上述信息可推知:T1<T2
B. T1℃时,该反应的平衡常数K=9/16
C. T1℃时,若开始时反应物的用量均减小一半,平衡后NO 的转化率减小
D. T2℃时,若反应达平衡后再缩小容器的体积。c(N2)/c(NO)不变
2NO2 (g) ②2NO2 (g)
N2O4 (g)测得 NO2和N2O4 的浓度变化如图所示,0~10min 维持容器温度为T1℃,10min 后升高并维持容器的温度为 T2℃。下列说法正确的是







