-
胃舒平主要成分是氢氧化铝,同时含有三硅酸镁( )等化合物。
)等化合物。
(1)三硅酸镁的氧化物形式为_______
(2)铝原子的原子结构示意图为________,写出氢氧化铝与胃酸反应的离子方程式________。
(3)Al2O3、MgO和SiO2都可以制耐火材料, 其原因是______。
A. Al2O3、MgO和SiO2都不溶于水 B.Al2O3、MgO和SiO2都是白色固体
C.Al2O3、MgO和SiO2都是氧化物 D.Al2O3、MgO和SiO2都有很高的熔点
-
(4分)胃舒平主要成分是氢氧化铝,同时含有三硅酸镁( )等化合物。
)等化合物。
(1)三硅酸镁的氧化物形式为_______
(2)铝原子的原子结构示意图为________,写出氢氧化铝与胃酸反应的离子方程式________。
(3)Al2O3、MgO和SiO2都可以制耐火材料, 其主要原因是______。
A. Al2O3、MgO和SiO2都不溶于水 B.Al2O3、MgO和SiO2都有很高的熔点
C.Al2O3、MgO和SiO2都是氧化物 D.Al2O3、MgO和SiO2都是白色固体
-
药物“胃舒平”中含有氢氧化铝,可用来治疗胃酸(主要成分是盐酸)过多。该反应属于
A. 化合反应 B. 分解反应 C. 置换反应 D. 复分解反应
-
(1)某建筑材料,主要成分铝硅酸盐,化学式MgAl2H4Si4O14;化学式改写成氧化物形式为_____________。则材料该与足量的氢氧化钠反应后过滤,滤渣主要是______.写出该过程中发生的离子方程式_______________________________、_______________________________________。
(2)检验CO2中是否混有SO2可将气体通过盛有______的洗气瓶.
(3)鉴别Na2CO3和NaHCO3溶液可选用______(填序号).
①NaOH ②Ca(OH)2 ③BaCl2④K2SO4 ⑤Ca(NO3)2
(4)某溶液中有NH4+,Mg2+,Fe2+,Al3+四种离子,若向其中加入过量的氢氧化钠溶液,加热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是______.
A.NH4+ B.Mg2+ C.Fe2+ D.Al3+
(5)6.4gCu与过量硝酸(60mL 8mol/L)充分反应后,硝酸的还原产物有NO、NO2,反应后溶液中所含H+为n mol,NO、NO2混合气体的物质的量为________________
-
(1)某建筑材料,主要成分为铝硅酸盐,化学式是MgAl2H4Si4O14;化学式改写成氧化物形式为_________。该材料与酸或碱反应时可以看作各氧化物分别与酸、碱反应,则材料该与足量的氢氧化钠反应后过滤,滤渣主要是_______。
(2)除去FeCl2溶液中少量的FeCl3最好加入_________物质。
(3)鉴别Na2CO3和NaHCO3溶液可选用_________。(填序号)
①NaOH;②Ca(OH)2;③BaCl2;④K2SO4;⑤Ca(NO3)2
(4)某溶液中有①SO42―②Mg2+③Fe2+④Al3+四种离子,若向其中加入过量的氢氧化钠溶液,加热并搅拌,再加入过量盐酸,溶液中大量减少的阳离子是
(5)将盛有18mLNO2和O2的混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积是( )
①1.2mL②2.4mL③3.6mL④5.2mL
A.①②B.①③C.②④D.①④
-
铝是地壳中含量最多的金属元素,在自然界主要以化合态的形式存在于氧化铝中。铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质,冶炼金属铝很重要的一个过程是Al2O3的提纯。由于Al2O3是两性氧化物,而杂质SiO2是酸性氧化物,Fe2O3是碱性氧化物,下图为工业上用酸溶法提取铝土矿中的铝。
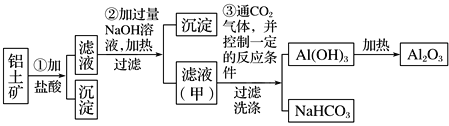
讨论回答下列问题:
(1)①中加盐酸后的沉淀主要是___________(化学式),为了加快铝土矿在盐酸中的溶解,可采取的措施有___________________________(一种即可)。
(2)写出②、③中可能发生反应的离子方程式。
②_______________________、________________、_______________________、________________。
③_____________________、________________。
(3)步骤②中不用氨水沉淀Fe3+的原因:_____________。
-
铝是地壳中含量最多的金属元素,在自然界主要以化合态的形式存在于氧化铝中。铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3等杂质,冶炼金属铝很重要的一个过程是Al2O3的提纯。由于Al2O3是两性氧化物,而杂质SiO2是酸性氧化物,Fe2O3是碱性氧化物,下图为工业上用酸溶法提取铝土矿中的铝。
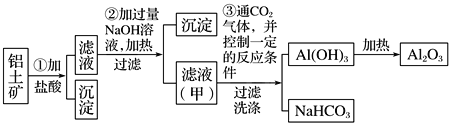
回答下列问题:
(1)①中加盐酸后的沉淀主要是___________(化学式),为了加快铝土矿在盐酸中的溶解,可采取的措施有___________________________(一种即可)。
(2)写出③中可能发生反应的离子方程式。
③_____________________、________________________。
(3)步骤②中不用氨水沉淀Fe3+的原因:_______________________________________。
-
食盐是生活中常用的调味品,胃酸的主要成分是盐酸。下列关于两种物质的说法正确的是( )
A. 炒菜时放入食盐并不破坏NaCl中的化学键
B. 胃舒平(主要成分氢氧化铝)与胃酸反应生成的AlCl3属于离子化合物
C. 盐酸中的溶质HCl属于共价化合物
D. NaCl熔化时破坏共价键
-
根据已经学过的化学知识,回答下列问题。
I.金属及其化合物在生产生活中有着广泛的应用,
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现_______性;_______(填“能”或“不能”)用氢氧化钠溶液代替。
(2)将Cu与稀硫酸混合,二者不能反应,滴入H2O2后,溶液很快变成蓝色,该反应的化学方程式为____________________________________________。
(3)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式_________________________。
II.物质的量是学习化学的基础。
(1)14.4 g CO和CO2的混合气体在标准状况下所占的体积为8.96 L,其中CO的质量为_____。
(2)市售浓H2SO4的质量分数为98%、密度为1.84g/cm3,其浓度为________mol·L-1。
(3)19g某二价金属的氯化物ACl2中含有0.4mo1Cl-离子,金属A的相对原子质量是_______。
(4)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有2.5 mol FeS2参加反应时,被氧化的硫的物质的量为_______mol。
-
下列说法正确的是
①硅在自然界中以游离态和化合态两种形式存在;②SiO2是由1个Si原子和2个O原子形成的SiO2分子;③水泥是硅酸盐材料;④光导纤维的主要成分是Si单质;⑤氮化硅陶瓷可做柴油机受热面的材料;⑥水玻璃可以用作木材防火材料;⑦硅胶可以做干燥剂;⑧氢氟酸可以用来刻蚀玻璃
A.①②③④⑤ B.②③④⑥⑧ C.③⑤⑥⑦⑧ D.③④⑤⑥⑧
)等化合物。

