-
某化学小组用MnO2和浓盐酸共热制取Cl2时,利用刚吸收过SO2的NaOH溶液对其尾气进行吸收处理.请按要求回答下列问题.
(1)请写出用此法制取Cl2的离子方程式: .
(2)该尾气吸收处理一段时间后,吸收液中(假设不含酸式盐)肯定存在的阴离子有OH﹣、Cl﹣、 ;对可能大量存在的其他阴离子(不考虑空气中CO2的影响)设计如下实验进行探究.
①提出假设:
假设1:只存在SO32﹣;假设2. ;假设3:既存在SO32﹣也存在ClO﹣.
②质疑讨论:经分析假设3不合理,理由是 .
③实验方案设计与分析:
限选试剂:3moL•L﹣1H2SO4、1moL•L﹣1NaOH、0.01mol•L﹣1KMnO4、紫色石蕊试液.
实验步骤 预期现象和结论
步骤一:取少量吸收液于试管中,滴加3mol•L﹣1H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中.
步骤二:在A试管中滴加0.01mol•L﹣1KMnO4,振荡. 若溶液褪色,则说明假设1成立.
步骤三:在B试管中滴加 ,振荡. 若 ,则说明假设2成立.
(3)假设有224mL(标准状况下)SO2被15mL 1mol•L﹣1的NaOH溶液完全吸收,得溶液X.忽略盐类的水解,所得X溶液中溶质正盐的物质的量为 .若用0.2000mol•L﹣1KIO3溶液恰好将上述溶液X中所有的硫元素氧化,还原产物为I2,则消耗KIO3溶液的体积为 mL.
高三化学实验题困难题查看答案及解析
-
某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理.
(1)请完成SO2与过量NaOH溶液反应的化学方程式:SO2+2NaOH=______
(2)反应Cl2+Na2SO3+2NaOH═2NaCl+Na2SO4+H2O中的还原剂为______
(3)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl-、OH- 和SO42-.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响).
①提出合理假设
假设1:只存在SO32-
假设2:既不存在SO32-也不存在ClO-
假设3:______
②设计实验方案,进行实验.请在答题卡上写出实验步骤以及预期现象和结论.限选实验试剂:3moL/LH2SO4、1moL/LNaOH、0.01mol/LKMnO4、淀粉-KI溶液、紫色石蕊试液实验步骤 预期现象和结论 步骤1:取少量吸收液于试管中,滴加3moL/LH2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中 步骤2: ______ 步骤3: ______ 高三化学解答题中等难度题查看答案及解析
-
某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
(1)请完成SO2与少量的NaOH溶液反应的化学方程式:(2分)
(2)反应Cl2+Na2SO3+2NaOH===2NaCl+Na2SO4+H2O中每转移2.5mol的电子则参加反应的还原剂的物质的量为________mol.(2分)
(3)吸收尾气一段时间后,吸收液(强碱性)中肯定存在Cl
、OH
和SO
.请设计实验,探究该吸收液中可能存在的其他阴离子(不考虑空气的CO2的影响).
①提出合理假设 .
假设1:只存在SO32-; 假设2:只存在ClO
假设3:既不存在SO32-也不存在ClO
;
假设4:________.(2分)
②设计实验方案进行实验。请在答题卡上写出实验步骤以及预期现象和结论
限选实验试剂:3moL
L-1H2SO4、0.01mol
L-1KMnO4、紫色石蕊试液.(每空2分)
实验步骤
预期现象和结论
步骤1:取少量吸收液于试管中,滴加3 moL
L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中.
步骤2:
步骤3:
高三化学填空题简单题查看答案及解析
-
某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其尾气进行吸收处理。
(1)请完成SO2与过量NaOH溶液反应的化学方程式:____________________________。
(2)反应Cl2+Na2SO3+2NaOH=2NaCl+Na2SO4+H2O中的氧化产物为_______,被还原的元素为________。
高三化学填空题简单题查看答案及解析
-
(16分)某科研小组用MnO2和浓盐酸制备Cl2时,利用刚吸收过少量SO2的NaOH溶液对其发扬进行吸收处理。
(1)请完成SO2与过量NaOH溶液反应的化学方程式:SO2+2NaoH=_____________。
(2)反应Cl2+Na2SO3+2NaOH=2NaCl + Na2SO4 +H2O中的还原剂为______________________-。
(3)吸收尾气一段时间后,吸收液(强碱性) 吵肯定存在Cl- 、OH- 和SO42- 。请设计实验,探究该吸收液中可能存在的其它离子(不考虑空气的CO2的影响)
①提出合理假设
假设1:只存在SO32-
假设2:既不存在SO32-也不存在ClO-
假设3:_____________
②设计实验方案,进行实验。请在答题卡上写出实验步骤以及预期现象和结论。限选实验试剂:3moL
L-1H2SO4、1moL
L-1NaOH、0.01mol
L-1KMnO4、淀粉-KI溶液、紫色石蕊试液.
实验步骤
预期现象和结论
步骤1:取少量吸收液于试管中,滴加3 moL
L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中
步骤2:
步骤3:
高三化学实验题简单题查看答案及解析
-
某课外活动兴趣小组欲用下列化学试剂在实验室里制取Cl2并验证Cl2的某些化学性质。实验试剂:3 mol·L-1 H2SO4、1 mol·L-1 NaOH溶液、MnO2、KMnO4、吸收少量SO2的NaOH溶液、浓盐酸、紫色石蕊试液、饱和NaCl溶液、BaCl2溶液、品红溶液。甲小组设计的实验装置图如下,在B中加入吸收少量SO2的NaOH溶液,D中加入1 mol·L-1 NaOH溶液。请回答下列问题:
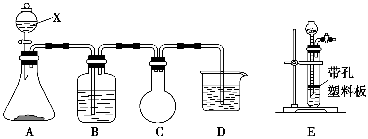
Ⅰ. (1)写出仪器X的名称:________。
(2)写出A中发生反应的化学方程式:__________________________,不能用E装置代替
A装置的原因是__________________________________________。
(3)C装置的作用是_______________________________________。
(4)甲小组通过该实验要验证Cl2的________(填“漂白性”、“还原性”或“氧化性”)。
(5)乙小组认为甲小组设计的实验装置有缺陷,请你帮助甲小组完善该装置。即还要在________和________(填“A”、“B”、“C”或“D”)装置间连接一个装有________的洗气装置。
Ⅱ.丙小组认为反应一段时间后,B装置溶液(强碱性)中肯定存在Cl-、OH-和SO42—,可能还含有其他的阴离子。
请你设计实验帮助丙小组探究该吸收液中可能存在的其他阴离子。
(1)提出合理假设
假设1:只存在________,或只存在________。
假设2:可能两者都________(填“存在”或“不存在”)。
(2)请设计实验验证假设的正确性:_____________________________。
高三化学实验题困难题查看答案及解析
-
某课外活动兴趣小组欲用下列化学试剂在实验室里制取Cl2并验证Cl2的某些化学性质。实验试剂:3 mol·L-1 H2SO4、1 mol·L-1 NaOH溶液、MnO2、KMnO4、吸收少量SO2的NaOH溶液、浓盐酸、紫色石蕊试液、饱和NaCl溶液、BaCl2溶液、品红溶液。甲小组设计的实验装置图如下,在B中加入吸收少量SO2的NaOH溶液,D中加入1 mol·L-1 NaOH溶液。请回答下列问题:
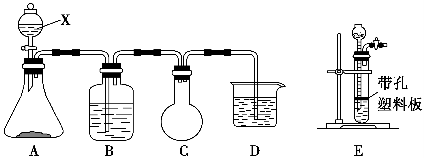
Ⅰ.(1)写出仪器X的名称:________。
(2)写出A中发生反应的化学方程式:__________________________________,
不能用E装置代替A装置的原因是___________________________________。
(3)C装置的作用是_________________________________________________。
(4)甲小组通过该实验要验证Cl2的________(填“漂白性”、“还原性”或“氧化性”)。
(5)乙小组认为甲小组设计的实验装置有缺陷,请你帮助甲小组完善该装置。即还要在________和________(填“A”、“B”、“C”或“D”)装置间连接一个装有________的洗气装置。
Ⅱ.丙小组认为反应一段时间后,B装置溶液(强碱性)中肯定存在Cl-、OH-和SO,可能还含有其他的阴离子。
请你设计实验帮助丙小组探究该吸收液中可能存在的其他阴离子。
(1)提出合理假设
假设1:只存在________,或只存在________。
假设2:可能两者都________(填“存在”或“不存在”)。
(2)请设计实验验证假设的正确性:___________________________________。
高三化学实验题困难题查看答案及解析
-
某化学兴趣小组欲利用MnO2和浓盐酸及如图所示装置制备Cl2。下列分析中不正确的是
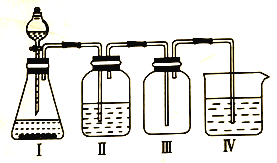
A.I中缺少加热装置
B.Ⅱ为净化Cl2的装置,其盛放的是NaOH溶液
C.Ⅲ为收集Cl2的装置
D.Ⅳ中处理多余的Cl2时,Cl2既作氧化剂,又作还原剂
高三化学单选题简单题查看答案及解析
-
工业制硫酸的过程中利用反应2SO2(g)+O2(g)
2SO3(g)+Q (Q>0),将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收。请回答下列问题:
(1)写出该可逆反应的化学平衡常数表达式 ;
(2)一定条件下,向一带活塞的密闭容器中充入2molSO2和1molO2发生反应,下列说法中,正确的是 (填编号)。
a.若反应速率υ正(O2)=2υ逆(SO3),则可以说明该可逆反应已达到平衡状态
b.保持温度和容器体积不变,充入2 mol N2,化学反应速率加快
c.平衡后移动活塞压缩气体,平衡时SO2、O2的百分含量减小,SO3的百分含量增大
d.平衡后升高温度,平衡常数K增大
将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应得到如下表中的两组数据:
实验编号
温度/℃
起始量/mol
平衡量/mol
达到平衡所需时间/min
SO2
O2
SO2
O2
1
T1
4
2
x
0.8
6
2
T2
4
2
0.4
y
t
(3)实验1从开始到反应达到化学平衡时,υ(SO2)表示的反应速率为 ;
T1 T2 (选填“>”、“<”或“=”),理由是 。尾气SO2用NaOH溶液吸收后会生成Na2SO3。现有常温下0.1mol/LNa2SO3溶液,实验测定其pH约为8,完成下列问题:
(4)该溶液中c(Na+)与 c(OH-) 之比为 。
该溶液中c(OH—) = c(H+)+ + (用溶液中所含微粒的浓度表示)。
(5)如果用含等物质的量溶质的下列各溶液分别来吸收SO2,则理论吸收量由多到少的顺序是 (用编号排序)
A.Na2SO3 B.Ba(NO3)2 C.Na2S D.酸性KMnO4
高三化学填空题极难题查看答案及解析
-
某化学小组用下图所示装置制取氯气,下列说法不正确的是
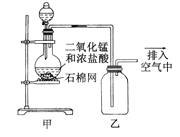
A. 该装置图中至少存在两处明显错误
B. 将烧瓶中的MnO2换成KMnO4可制得Cl2
C. 在乙后连一盛有饱和食盐水的烧杯进行尾气处理
D. 在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸可以证明是否有氯气逸出
高三化学单选题简单题查看答案及解析