-
乙醇的沸点是78 ℃,能与水以任意比混溶,易与氯化钙结合生成配合物。乙醚的沸点为34.6 ℃,难溶于水,乙醚极易燃烧。实验室制乙醚的反应原理是:
2CH3CH2OH CH3CH2—O—CH2CH3 (乙醚)+H2O
CH3CH2—O—CH2CH3 (乙醚)+H2O
实验步骤:
Ⅰ.乙醚的制备
在分液漏斗中加入2 mL 95%的乙醇,在一干燥的三颈烧瓶中放入12 mL 95%的乙醇,在冷水浴中的冷却下边摇动边缓慢加入12 mL浓硫酸,使混合均匀,并加入2粒沸石。实验装置如下图:

将反应瓶放在电热套上加热,使温度迅速地上升到140 ℃,开始由分液漏斗慢慢滴加乙醇,控制流速并保持温度在135~140 ℃之间。待乙醇加完后,继续反应10 min,直到温度上升到160 ℃止。关闭热源,停止反应。
Ⅱ.乙醚的精制
将馏出物倒入分液漏斗中,依次用8 mL 15% NaOH溶液、8 mL饱和食盐水洗涤,最后再用8 mL饱和氯化钙溶液洗涤2次,充分静置后分液。将乙醚倒入干燥的锥形瓶中,用块状无水氯化钙干燥。待乙醚干燥后,加入到蒸馏装置中用热水浴蒸馏,收集33~38 ℃的馏分。
请根据上述信息,完成下列问题:
(1)乙醚的制备和精制过程中都需要使用沸石,其作用是________________________,
如果实验中忘记加沸石,需要怎么处理?______________________________________。
(2)乙醚的制备和精制过程中都需要使用温度计,其水银球位置是否相同?________(填“是”或“否”),原因是_____________________________________________________________。
(3)仪器C的名称为________。
(4)如果温度太高,将会发生副反应,产物是__________。
(5)精制乙醚中,加入15% NaOH溶液的作用是_________,加入饱和氯化钙溶液的作用是_________。
-
(12分)乙醇的沸点是78℃,能与水以任意比例混溶。乙醚的沸点为34.6℃,难溶于水,在饱和Na2CO3溶液中几乎不溶,乙醚极易燃烧。实验室制乙醚的反应原理是

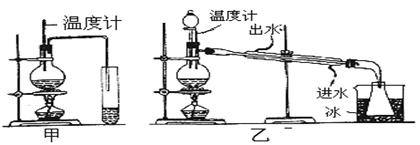
(1)图甲和乙是两套实验室制乙醚的装置,选装置________最合适,
理由是______________________________________________________ _____。
(2)反应液中应加入沸石,其作用是。
(3)反应中温度计水银球的位置是__________________ 。
(4)用装置乙制得的乙醚中可能含有大量的杂质,这杂质是________ ,除去这种杂质的简易方法是________ 。
-
(12分)乙醇的沸点是78℃,能与水以任意比例混溶。乙醚的沸点为34.6℃,难溶于水,在饱和Na2CO3溶液中几乎不溶,乙醚极易燃烧。实验室制乙醚的反应原理是


(1)图甲和乙是两套实验室制乙醚的装置,选装置________最合适,理由是__ 。
(2)反应液中应加入沸石,其作用是________。
(3)反应中温度计水银球的位置是__________________ 。
(4)用装置乙制得的乙醚中可能含有大量的杂质,这杂质是________ ,除去这种杂质的简易方法是________ 。
(5)如果温度太高将会有乙烯生成,该反应的化学方程式是________
________ ,反应类型是________。
-
(8分)乙醇的沸点是78℃,能与水以任意比例混溶。乙醚的沸点为34.6℃,
难溶于水,在饱和Na2CO3溶液中几乎不溶,乙醚极易燃烧。实验室制乙醚的
反应原理是


(1) 图甲和乙是两套实验室制乙醚的装置,选装置________最合适。
(2) 反应液中应加入沸石,其作用是________。
(3) 反应中温度计的位置是________ 。
(4) 用装置乙制得的乙醚中可能含有大量的乙醇,除去乙醇的简易方法是 。
(5) 如果温度太高将会发生另一有机反应,此反应方程式为
________。
-
( 11分)乙醇的沸点是78℃,能与水以任意比混溶。乙醚的沸点为34.6℃,难溶于水,在饱和Na2CO3 溶液中几乎不溶,乙醚极易燃烧。实验室制醚的反应原理是:
2CH3CH2OH H2O + CH3CH2—O—CH2CH3 (乙醚)
H2O + CH3CH2—O—CH2CH3 (乙醚)
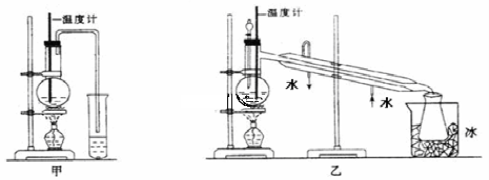
(1)甲图和乙图是两套实验室制乙醚的装置,选装置___(填“甲”或“乙”)最合理,理由是_ 。
(2)反应液中应加入沸石,其作用是____________。
(3)反应中温度计的正确位置是水银球置于________________________。
(4)用上述装置乙制得的乙醚中可能含有大量的杂质,该杂质是__________,除去这种杂质的简易方法是________________________________。
(5)如果温度太高(如170℃),将会发生一个有机副反应,反应方程式为:__________。
-
( 11分)乙醇的沸点是78℃,能与水以任意比混溶。乙醚的沸点为34.6℃,难溶于水,在饱和Na2CO3 溶液中几乎不溶,乙醚极易燃烧。实验室制醚的反应原理是:
2CH3CH2OH  H2O + CH3CH2—O—CH2CH3 (乙醚)
H2O + CH3CH2—O—CH2CH3 (乙醚)

(1)甲图和乙图是两套实验室制乙醚的装置,选装置_______(填“甲”或“乙”)最合理,理由是_____________。
(2)反应液中应加入沸石,其作用是____________。
(3)反应中温度计的正确位置是水银球置于________________________。
(4)用上述装置乙制得的乙醚中可能含有大量的杂质,该杂质是__________,除去这种杂质的简易方法是________________________________。
(5)如果温度太高(如170℃),将会发生一个有机副反应,反应方程式为:____________________________________________。
-
乙醇的沸点是78℃,能与水以任意比混溶。乙醚的沸点为34.6℃,难溶于水,在饱和Na2CO3 溶液中几乎不溶,乙醚极易燃烧。实验室制醚的反应原理是:
2CH3CH2OH→H2O + CH3CH2—O—CH2CH3 (乙醚)
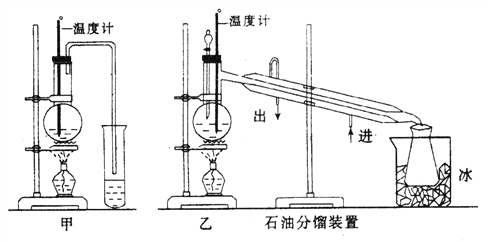
(1)甲图和乙图是两套实验室制乙醚的装置,选装置_________(填“甲”或“乙”)最合理,理由是______________________________。
(2)反应液中应加入沸石,其作用是____________________。
(3)反应中温度计的正确位置是水银球置于____________________。
(4)用装置乙制得的乙醚中可能含有大量的杂质,该杂质是__________,除去这种杂质的简易方法是__________________(提示:乙醚不溶于水,乙醇与水互溶)。
(5)如果温度太高,将会发生副反应,其产物名称为____________。
-
(11分) 已知乙醇可以和氯化钙反应生成微溶于水的CaCl2·6C2H5OH。有关的有机试剂的沸点如下:CH3COOC2H5 77.1℃ C2H5OC2H5(乙醚) 34.5℃ C2H5OH 78.3℃ CH3COOH 118℃ 实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇与少量浓硫酸混合,然后经分液漏斗边滴加醋酸、边加热蒸馏。得到含有乙醇、乙醚、醋酸和水的乙酸乙酯粗产品。
(1)写出合成乙酸乙酯的反应原理:____________________________________________。
(2)反应中加入乙醇是过量的,其目的是:________。
将粗产品再经下列步骤精制:
(3)为除去粗产品其中的醋酸,可向产品中加入__________(填字母)。
A.无水乙醇 B.碳酸钠粉末 C.无水醋酸钠
(4)再向其中加入饱和氯化钙溶液,振荡。其目的是:。
(5)最后,将经过上述处理后的液体放入另一干燥的蒸馏瓶内,再蒸馏。蒸馏时,需要的玻璃仪器有:酒精灯、温度计、冷凝管、锥形瓶、尾接管和____________。冷凝管的水流方向为________进________出,弃去低沸点馏分,收集76—78℃沸程之间的馏分即得。
-
已知乙醇可以和氯化钙反应生成微溶于水的CaCl2·6C2H5OH。有关的有机试剂的沸点如下:
CH3COOC2H5为77.1℃; C2H5OH为78.3℃;
C2H5OC2H5(乙醚)为34.5℃; CH3COOH为118℃。
实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇与少量浓硫酸混合,然后经分液漏斗边滴加醋酸,边加热蒸馏。由上面的实验可得到含有乙醇、乙醚、醋酸和水的乙酸乙酯粗产品。
(1)制取乙酸乙酯的方程式是___________。
将粗产品经下列步骤精制:
(2)为除去其中的醋酸,可向产品中加入__________(填字母)。
A.无水乙醇 B.碳酸钠粉末 C.无水醋酸钠
(3)再向其中加入饱和氯化钙溶液,振荡,分离,其目的是____________________。
(4)然后再向其中加入无水硫酸铜,振荡,其目的是___________________。最后,将经过上述处理后的液体加入另一干燥的蒸馏瓶内,再蒸馏,弃去低沸点馏分,收集沸点在76℃~78℃之间的馏分即得纯净的乙酸乙酯。
-
已知乙醇可以和氯化钙反应生成微溶于水的CaCl2·6C2H5OH。有关的有机试剂的沸点如下:CH3COOC2H5 77.1℃ C2H5OC2H5(乙醚) 34.5℃ C2H5OH 78.3℃ CH3COOH 118℃ 实验室合成乙酸乙酯粗产品的步骤如下:在蒸馏烧瓶内将过量的乙醇与少量浓硫酸混合,然后经分液漏斗边滴加醋酸、边加热蒸馏。得到含有乙醇、乙醚、醋酸和水的乙酸乙酯粗产品。
(1)反应中加入乙醇是过量的,其目的是:________ 。
将粗产品再经下列步骤精制:
(2)为除去其中的醋酸,可向产品中加入__________(填字母)。
A 无水乙醇 B 碳酸钠粉末 C 无水醋酸钠
(3)再向其中加入饱和氯化钙溶液,振荡。其目的是:________。
(4)然后再向其中加入无水硫酸钠,振荡。其目的是:。
最后,将经过上述处理后的液体放入另一干燥的蒸馏瓶内,再蒸馏。弃去低沸点馏分,收集76~78℃沸程之间的馏分即得。
CH3CH2—O—CH2CH3 (乙醚)+H2O






