-
(11分)为确定某酸HA是弱电解质,两同学的实验方案如下:
甲:①称取一定质量的HA,配制0.1 mol·L-1的溶液100 mL;
②用pH计测出该溶液的pH,根据pH=-lg c(H+),推算出溶液中H+的浓度,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制0.1mol·L-1的两种酸溶液各100 mL;
②分别取配制的这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是___ ___。
(2)甲方案中说明HA是弱电解质的理由是测得溶液的H+的浓度_ _0.1 mol·L-1(选填“>”、“<”或“=”)。
(3)乙方案中说明HA是弱电解质的现象是_ __。
A.装盐酸的试管中放出气体的速率快;
B.装HA溶液的试管中放出气体的速率快;
C.两个试管中产生气体的速率一样快。
(4)请你评价:乙方案中的不妥之处:______ ___________________________。
(5)已知在T°C时,0.1 mol·L-1HA溶液中HA的电离度为5%,求该温度下HA的电离常数(写出计算过程)
高二化学实验题极难题查看答案及解析
-
(5分)甲、乙两同学拟用实验确定某酸HA是弱电解质。他们设计的方案(理论方案)分别是:
甲:①称取一定质量的HA配制0.1 mol/L的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=3的两种酸溶液各100 mL;
②分别取这两种溶液各1 mL,加水稀释为100 mL;
③用两支试管分别取相同体积的两种稀释液,同时加入纯度相同、颗粒大小均等的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是 。
(2)甲方案中,能说明HA是弱电质的理由是测得溶液的pH___1(选填“>”、“<”、“=”)。
(3)关于pH试纸的使用方法,下列叙述正确的是 。
a.pH试纸在使用之前应用蒸馏水润湿
b.将pH试纸直接插入待测溶液,取出后再与标准比色卡对比
c.pH试纸测出的数值应该保留一位小数
d.能使pH试纸显红色的溶液显酸性
(4)乙方案中,说明HA是弱电解质的现象是 。
高二化学实验题困难题查看答案及解析
-
(12分)甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。实验方案如下: 甲:①准确配制0.1 mol·L-1的HA、HCl溶液各100 mL;
②取纯度相同,质量、大小相等的锌粒于两只试管中,同时加入0.1 mol·L-1的 HA 、HCl溶液各10 mL,按图装好,观察现象
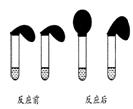
乙:①用pH计测定物质的量浓度均为0.1 mol·L-1 HA和HCl溶液的pH;
②再取0.1 mol·L-1的HA和HCl溶液各2滴(1滴约为1/20 mL)分别稀释至100 mL,再用pH计测其pH变化
(1) 甲、乙两方案中都要用到__________ mL的容量瓶。乙方案中说明HA是弱电解质的理由是,测得0.1 mol·L-1的HA溶液的pH1(填“>”、“<”或“=”) ;甲方案中,说明HA是弱电解质的实验现象是:________
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后, 试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第______步,能证明改变条件弱电解质平衡发生移动。甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:①使HA的电离程度和c(H+)都减小, c(A-)增大,可在0.1 mol/L的HA溶液中,选择加入_________试剂;②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1 mol/L的HA溶液中,选择加入________试剂。
A. NaA固体(可完全溶于水) B.1 mol/LNaOH溶液
C. 1 mol/L H2SO4 D.2 mol/LHA
(3)pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积V的关系如图所示。
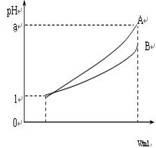
则下列说法不正确的有( )。
A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
高二化学实验题简单题查看答案及解析
-
(5分)用实验确定HCOOH是弱电解质。两同学的方案是:
甲:①称取一定质量的HCOOH配制0.1 mol·L-1的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HCOOH是弱电解质。
乙:①用已知物质的量浓度的HCOOH溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;②分别取这两种溶液各10 mL,加水稀释为100 mL;③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HCOOH是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是________。
(2)甲方案中,说明HCOOH是弱电解质的理由是测得溶液的pH________1(选填>、<、=)。
乙方案中,说明HCOOH是弱电解质的现象是________
a.装HCl溶液的试管中放出H2的速率快;
b.装HCOOH溶液的试管中放出H2的速率快;
c.两个试管中产生气体速率一样快:
(3)一定温度下有:a.盐酸;b.硫酸;c.醋酸三种酸。
①当其物质的量浓度相同时,c(H+)由大到小的顺序是___________________________。
②当c(H+)相同、体积相同时,同时加入镁,若产生相同体积的H2(相同状况),则开始时的反应速率____________________。(用a b c的大小关系表示)
高二化学实验题简单题查看答案及解析
-
(5分)甲、乙两同学拟用实验确定某酸HA是弱电解质。他们的方案分别是:
甲:①称取一定质量的HA配制0.1 mol/L的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是________ 。
(2)甲方案中,说明HA是弱电质的理由是测得溶液的pH___1(选填>,<,=)。简要说明pH试纸的使用方法:
________
(3) 乙方案中,说明HA是弱电解质的现象是_________ 。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
高二化学填空题简单题查看答案及解析
-
(8分)用实验确定某酸HA是弱电解质。两同学的方案是:
甲:①称取一定质量的HA配制0.1 mol·L-1的溶液 100 mL;②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;②分别取这两种溶液各10 mL,加水稀释为100 mL;③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是________。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH________1(选填>、<、=)。
乙方案中,说明HA是弱电解质的现象是________(多选扣分)
a.装HCl溶液的试管中放出H2的速率快;
b.装HA溶液的试管中放出H2的速率快;
c.两个试管中产生气体速率一样快:
(3)请你评价乙方案中难以实现之处和不妥之处。
_________________________________________________________________。
高二化学填空题简单题查看答案及解析
-
甲、乙两同学拟用实验确定某酸HA是弱电解质。他们的方案分别是:
甲:①称取一定质量的HA配制0.1 mol/L的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是________________。
(2)甲方案中,说明HA是弱电质的理由是测得溶液的pH____1(选填“>”、“<”或“=”)。简要说明pH试纸的使用方法:_________________________________________________________。
(3)乙方案中,说明HA是弱电解质的现象是_______________________________________________________________________。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),并作简明扼要表述:_______________________。
高二化学实验题简单题查看答案及解析
-
甲、乙两同学拟用实验确定某酸HA是弱电解质。他们的方案分别是:
甲:①称取一定质量的HA配制0.1 mol/L的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是________ 。
(2)甲方案中,说明HA是弱电质的理由是测得溶液的pH________1(选填“>”、“<”或“=”)。简要说明pH试纸的使用方法:________。
(3)乙方案中,说明HA是弱电解质的现象是
。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),并作简明扼要表述:________ 。
高二化学填空题中等难度题查看答案及解析
-
用实验确定某酸HB的弱电解质。两同学的方案是:
甲:①称取一定质量的HB配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HB是弱电解质。
乙:①用已知物质的量浓度的HB溶液、盐酸,分别配制pH = 1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HB是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是________
(2)甲方案中,说明HB是弱电解质的理由是测得溶液的pH 1(选填>、<、=)
乙方案中,说明HB是弱电解质的现象是________(多选扣分)
A.HCl溶液的试管中放出H2的速率快; B.装HB溶液的试管中放出H2的速率快;
C.两个试管中产生气体速率一样快。
(3)请你评价:乙方案中两个难以实现之处________
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表达。
高二化学填空题简单题查看答案及解析
-
用实验确定某酸HB的弱电解质。两同学的方案是:
甲:①称取一定质量的HB配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HB是弱电解质。
乙:①用已知物质的量浓度的HB溶液、盐酸,分别配制pH = 1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HB是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是________
(2)甲方案中,说明HB是弱电解质的理由是测得溶液的pH________1(选填>、<、=)
乙方案中,说明HB是弱电解质的现象是________(多选扣分)
A.HCl溶液的试管中放出H2的速率快;
B.装HB溶液的试管中放出H2的速率快;
C.两个试管中产生气体速率一样快。
(3)请你评价:乙方案中两个难以实现之处________
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表达。
________
高二化学填空题中等难度题查看答案及解析