-
常温下,取两片质量相等、外形和组成相同表面经过砂纸打磨(完全除掉了氧化物)的铝片,分别加入到盛有体积相同、c(H+)相同的稀硫酸和稀盐酸溶液的两支试管(相同体积)中制取H2。实验现象如下表:
时间
酸1 min
2 min
5 min
15 min
20 min
3mol/L HCl
少量气泡
较多气泡
大量气泡
反应剧烈
铝片耗尽
1.5mol/L H2SO4
均无明显现象(无气泡)
(1)写出以上反应的离子方程式________________________________________。
(2)分析上表数据,你得出的结论是:__________________________________。
(3)你认为出现以上现象的可能原因是(写出一个即可):
_____________________________________________________________;
(4)请设计实验对你的假设进行验证:
______________________________________________________________;
(5)如果上述假设都成立,要使以上稀硫酸与铝反应产生的氢气速率加快,可以采取的措施有(列举三个):____________________________________________________
高二化学实验题中等难度题查看答案及解析
-
(16分)常温下,取两片质量相等、外形和组成相同表面经过砂纸打磨(完全除掉了氧化物)的铝片,分别加入到盛有体积相同、c(H+)相同的稀硫酸和稀盐酸溶液的两支试管(相同体积)中制取H2。实验现象如下表:
时间
酸
1 min
2 min
5 min
15 min
20 min
3mol/L HCl
少量气泡
较多气泡
大量气泡
反应剧烈
铝片耗尽
1.5mol/L H2SO4
均无明显现象(无气泡)
(1)写出以上反应的离子方程式______________________________________________。
(2)分析上表数据,你得出的结论是:________。
(3)你认为出现以上现象的可能原因是(写出一个即可):
______________________________________________________________________;
(4)请设计实验对你的假设进行验证:
__________________________________________________________________;
(5)如果上述假设都成立,要使以上稀硫酸与铝反应产生的氢气速率加快,可以采取的措施有(列举三个):________
高二化学实验题简单题查看答案及解析
-
在学习了化学反应速率知识后,某研究性学习小组进行了科学探究活动。
[探究活动一]探究金属与不同酸反应的反应速率:常温下,用经过砂纸打磨的铝片中取两片质量相等、表面积相同的铝片,分别加入到盛有体积相同、c(H+)相同,足量的稀硫酸和稀盐酸溶液的两支试管中,发现铝片在稀盐酸中消失的时间比在稀硫酸中短。
(1)对[探究活动一]实验现象发生的原因,请你帮该研究性学习小组提出两个假设:
假设Ⅰ_______________________________。
假设Ⅱ_______________________________。
并请你设计实验对以上假设进行验证:
验证假设Ⅰ_______________________________。
验证假设Ⅱ_______________________________。
[探究活动二]某小组在实验室测定氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率。
(2)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)⇌2NH3(g)+CO2(g).
实验测得不同温度下的平衡数据列于下表:
温度(℃)
15.0
20.0
25.0
30.0
35.0
平衡总压强(kPa)
5.7
8.3
12.0
17.1
24.0
平衡气体总浓度(×10-3mol/L)
2.4
3.4
4.8
6.8
9.4
①可以判断该分解反应已经达到化学平衡状态的是 .
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0℃时的分解平衡常数: .
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量 (填“增加”、“减小”或“不变”).
④氨基甲酸铵分解反应的焓变△H 0,熵变△S 0(填>、<或=).
(3)已知:NH2COONH4+2H2O⇌NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间变化趋势如下图所示.
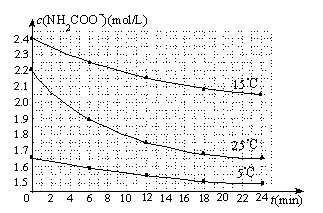
⑤计算25℃时,0~6min氨基甲酸铵水解反应的平均速率: .
⑥根据图中信息,如何说明水解反应速率随温度升高而增大: 。
高二化学实验题困难题查看答案及解析
-
某同学利用如图所示实验装置测定常温常压下的气体摩尔体积。
根据下列步骤完成实验:
①装配好装置,检查气密性
②用砂纸擦去镁带表面的氧化物,然后取0.0480g的镁带加入仪器a中,分液漏斗内加入足量1mol/L硫酸溶液
③量气装置中加入适量水,记录量气管读数(读数为0.10mL)
④通过分液漏斗向仪器a中加入适量硫酸溶液,使镁带与硫酸充分反应
⑤当镁带完全反应后,再次记录量气管读数(读数为49.60mL)。
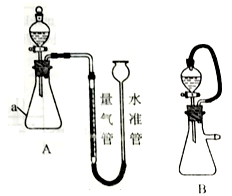
完成下列填空:
(1)仪器a的名称_______,通过分液漏斗向仪器a中加入硫酸溶液的操作是_______。
(2)在记录量气管读数时,应注意将_______,再________,视线与量气管内凹液面相切,水平读数。
(3)该同学测出此条件下气体摩尔体积为__________,测定结果比理论值偏大,可能的原因是(填字母代号)__________。
a.镁带中氧化膜未除尽 b.镁带含有杂质铝
c.③记录量气管读数时俯视读数 d.镁带完全反应后有残留的未溶固体
(4)与原方案装置相比,有同学设想用装置B代替装置A,实验精确度更高。请说明理由____________________。
高二化学实验题中等难度题查看答案及解析
-
利用下左图所示实验装置可以测定常温常压下气体的摩尔体积。
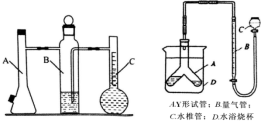 c
c甲同学利用如上左图装置,根据下列步骤完成实验:
① 装配好装置,作气密性检查。
②用砂纸擦去镁带表面的氧化物,然后取0.108g的镁带。
③取下A瓶加料口的橡皮塞,用小烧杯加入20mL水,再把已称量的镁带加到A瓶的底部,用橡皮塞塞紧加料口。
④用注射器从A瓶加料口处抽气,使B瓶导管内外液面持平。
⑤用注射器吸取10mL3mol·L-1硫酸溶液,用针头扎进A瓶加料口橡皮塞,将硫酸注入A瓶,注入后迅速拔出针头。
⑥当镁带完全反应后,读取C瓶中液体的体积,记录数据。⑦用注射器从A瓶加料口处抽出8.0mL气体,使B瓶中导管内外液面持平。⑧读出C瓶中液体体积是115.0mL。
完成下列填空:
(1) 在常温常压下气体摩尔体积理论值约为24.5L/mol,甲同学测出此条件下lmol气体的体积为______,计算此次实验的相对误差为________%〈保留2位有效数字)。引起该误差的可能原因是______。
a.镁带中含铝; b.没有除去镁带表面的氧化物; c.反应放热; d.所用硫酸的量不足
(2) 丙同学提出可用如上右图装置完成该实验。该装置气密性的检查方法是:_____________。
(3) 与原方案装置相比,丙同学使用的装置实验精度更高。请说明理由(回答两条)____________________________________,_____________________________________。
高二化学实验题困难题查看答案及解析
-
(12分)下列是构成原电池的实验方案, 请按要求回答下列问题:
(1)电解质溶液为0.5mol·L-1硫酸溶液,电极为用砂纸打磨过的镁片和铝片,设计成原电池,则铝片为
极(填“正”或“负”),正极电极反应式为 ;若将电解质溶液改为0.5mol·L-1氢氧化钠溶液,则被氧化的是 (填“镁片”或“铝片”),该原电池总反应的离子方程式为:
(2)以“Fe+2Fe3+===3Fe2+ ”反应为原理设计原电池,请在以下该原电池装置图括号中写出电极材料及电解质溶液。

高二化学填空题困难题查看答案及解析
-
铝及铝合金经过阳极氧化,铝表面能生成几十微米厚的氧化铝膜。某研究性学习小组模拟工业法对铝片表面进行氧化处理。分别以铅片、铝片为电极,以硫酸溶液为电解液,按照如图所示装置连接电解池装置,电解40 min后取出铝片,用水冲洗,放在水蒸气中封闭处理20~30 min,即可得到更加致密的氧化膜。下列有关说法正确的是 ( )。
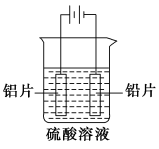
A.电解时电子从电源负极→导线→铝极,铅极→导线→电源正级
B.在电解过程中,H+向阳极移动,SO
向阴极移动
C.电解过程阳极周围溶液的pH下降
D.电解的总反应为2Al+6H+===2Al3++3H2↑
高二化学选择题中等难度题查看答案及解析
-
有关常温下pH均为3的酸酸和硫酸的说法正确的是
A.分别加水稀释100倍后,两种溶液的pH仍相同
B.醋酸中的c(CH3COO-)和硫酸中的c(SO42-)相等
C.分别加入足量锌片,两种溶液生成H2的体积相同
D.两种溶液中,由水电离出的氢离子浓度均为1×10-11 mol•L-1
高二化学选择题中等难度题查看答案及解析
-
在下面列出的事实中,不能证明乙酸
是弱酸的是
A.
的乙酸溶液的
约为3.0
B. 乙酸能跟
溶液反应放出二氧化碳
C. 相同浓度的乙酸和盐酸分别于与表面积完全相同的锌粒反应,盐酸反应速率快
D. 常温下,
乙酸钠溶液的
约为9
高二化学单选题简单题查看答案及解析
-
向体积和pH 均相等的盐酸和醋酸中分别加入等质量的镁粉,镁粉均完全溶解,则产生
的体积
同温同压下测定
随时间变化的关系正确的是
A.
 B.
B. 
C.
 D.
D. 
高二化学单选题中等难度题查看答案及解析