-
用金属钴板(含少量Fe、Ni)制备应用广泛的氯化钴的工艺流程如下:
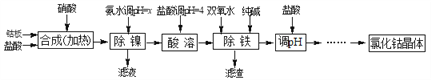
注:钴与盐酸反应极慢,需加入催化剂硝酸才可能进行实际生产。
有关钴、镍和铁化合物的性质见下表:
| 化学式 | 沉淀完全时的pH | 钴镍性质 |
| Co(OH)2 | 9.4 | Co+2HCl=CoCl2+H2↑ Co2++2NH3·H2O=Co(OH)2↓+2NH4+ Co2++2H2O Co(OH)2+2H+ Co(OH)2+2H+ Ni+2HCl=NiCl2+H2↑ Ni2++6NH3·H2O=[Ni(NH3)6]2++6H2O |
| Fe(OH)2 | 9.6 |
| Fe (OH)3 | 3.7 |
(1)“除镍”步骤中,NH3·H2O用量对反应收率的影响见表中数据:从表中数据可知,当PH调节至x=_______时,除镍效果最好。
| 加NH3·H2O调pH | 收率/% | Ni2+含量/% |
| 9 | 98.1 | 0.08 |
| 9.5 | 98 | 0.05 |
| 10 | 97.6 | 0.005 |
| 10.3 | 94 | 0.005 |
(2)“除镍”步骤必须控制在一定的时间内完成,否则沉淀中将有部分Co(OH)2转化为Co(OH)3,此反应的化学方程式为________________。
(3)“除铁”步骤中加入双氧水发生反应的离子方程式是________________________。
(4)“除铁”步骤中加入的纯碱作用是________________________________。
(5)在“调pH”步骤中,加盐酸的作用是______________________________。
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O Fe(OH)3+3H+的平衡常数为_____________________。
Fe(OH)3+3H+的平衡常数为_____________________。
-
用金属钴板(含少量Fe、Ni)制备应用广泛的氯化钴的工艺流程如下:
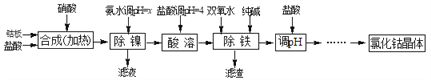
注:钴与盐酸反应极慢,需加入催化剂硝酸才可能进行实际生产。
有关钴、镍和铁化合物的性质见下表:
| 化学式 | 沉淀完全时的pH | 钴镍性质 |
| Co(OH)2 | 9.4 | Co+2HCl=CoCl2+H2↑ Co2++2NH3·H2O=Co(OH)2↓+2NH4+ Co2++2H2O Co(OH)2+2H+ Co(OH)2+2H+ Ni+2HCl=NiCl2+H2↑ Ni2++6NH3·H2O=[Ni(NH3)6]2++6H2O |
| Fe(OH)2 | 9.6 |
| Fe (OH)3 | 3.7 |
(1)“除镍”步骤中,NH3·H2O用量对反应收率的影响见表中数据:从表中数据可知,当PH调节至x=_______时,除镍效果最好。
| 加NH3·H2O调pH | 收率/% | Ni2+含量/% |
| 9 | 98.1 | 0.08 |
| 9.5 | 98 | 0.05 |
| 10 | 97.6 | 0.005 |
| 10.3 | 94 | 0.005 |
(2)“除镍”步骤必须控制在一定的时间内完成,否则沉淀中将有部分Co(OH)2转化为Co(OH)3,此反应的化学方程式为________________。
(3)“除铁”步骤中加入双氧水发生反应的离子方程式是________________________。
(4)“除铁”步骤中加入的纯碱作用是________________________________。
(5)在“调pH”步骤中,加盐酸的作用是______________________________。
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O Fe(OH)3+3H+的平衡常数为_____________________。
Fe(OH)3+3H+的平衡常数为_____________________。
-
铁及其化合物在日常生活中应用广泛,请回答下列问题:
(1)Fe(NO3)3·9H2O易溶于水,微溶于硝酸,主要用作催化剂和媒染剂,工业上用细铁屑与稀硝酸反应制备,主要流程如下:
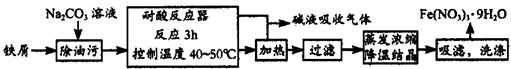
①Na2CO3溶液可以除油污,原因是(用离子方程式表示)_________________________;
②耐腐反应器中可以观察到如下的现象:铁屑__________,溶液颜色变为__________,有______色气体产生;制备过程中需控制加入铁屑的量,当观察到_______________的现象时应停止加入铁屑;
③制得的Fe(NO3)3·9H2O用20% HNO3洗涤,其原因是_________________________。
④若在实验中进行蒸发浓缩、降温结晶的操作,除带铁圈的铁架台、坩埚钳外,还需要的主要仪器有___________。
(2)某兴趣小组在实验室用细铁屑和稀硝酸制备Fe(NO3)3,装置如右图所示(固定所用仪器和加热装置未画出)。
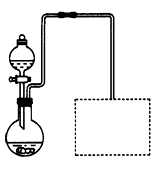
①该实验中对圆底烧瓶加热的最佳方式用__________加热;
②装置中圆底烧瓶上方长导管的作用是_________________;
③请在图中虚线框内画出防止倒吸的尾气吸收装置。(提示:碱液可快速、充分吸收产生的氮的氧化物气体)
-
(12分)有关钴、镍和铁化合物的性质见下表:
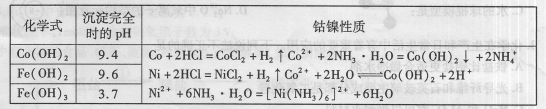
氯化钴可用于化学反应催化剂,油漆催干剂,干湿指示剂,啤酒泡沫稳定剂,陶瓷着色剂,制造隐显墨水等。用金属钴板(含少量Fe、Ni)制备氯化钴的工艺流程如下:
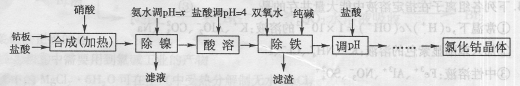
钴与盐酸反应极慢,需加入催化剂硝酸才可能进行实际生产。
(1)“除镍”步骤中,NH3·H2O用量对反应收率的影响,见下表:
从表中可知x=________时,除镍效果最好。
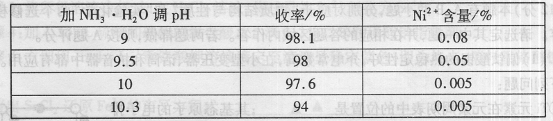
(2)“除镍”步骤必须控制在一定的时间内完成,否则沉淀将有部分Co(OH)3生成,试写出反应的化学方程式________。
(3)“除铁”步骤中加入双氧水发生反应的离子方程式是________.
(4)“除铁”步骤中加入的纯碱作用是________。
(5)在“调pH"步骤中,加盐酸的作用是
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O Fe(OH)3+3H+的平衡常数为________。
Fe(OH)3+3H+的平衡常数为________。
-
铝的单质及其化合物在生产、生活、科研等领城应用广泛。
Ⅰ、工业上用铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)制备铝的某种化合物的工艺流程如下:
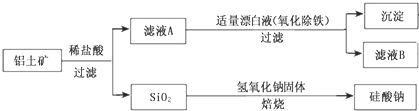
(1)加入盐酸时,氧化铝发生反应的离子方程式为______
(2)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。该过程中涉及某氧化还原反应如下,请完成:Fe2++___ClO-+ ________________________ ________________________═ Fe(OH)3↓+ Cl-+__________
Ⅱ、明矾在日常生活、生产中也占有一席之地。
(3)明矾是净水明星,用离子方程式表示其净水原理_____________________________。
(4)向0.02mol的明矾溶液中逐滴加入150mL0.2mol/LBa(OH)2溶液, 生成沉淀的质量为 _____克。
-
铬(Cr)硬度大、抗腐蚀性和耐磨性好,具有广泛的应用前景。一种以铬铁矿(含FeCr2O4及少量Al2O3、SiO2等)为原料制备金属铬的工艺流程如下:
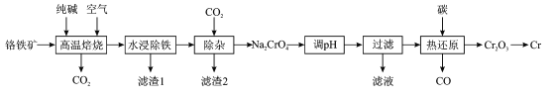
回答下列问题:
(1)“高温焙烧”中主要反应的化学方程式为____。
(2)为提高“水浸”的浸取率,除了适当升高温度,还可采取的措施是____。
(3)“滤渣1”是一种红棕色固体,为检验其中的金属元素,可选择的常用试剂是____。“滤渣2”的主要成分是__________。
(4)“调pH”的目的是____。
(5)“热还原”主要是利用焦炭与重铬酸盐得到Cr2O3和另一种固体产物,该固体产物可返回__________工序循环使用。
(6)可用铝热法还原Cr2O3制备铬单质,铝热反应中镁带的作用是____;还可用惰性电极电解硫酸铬钾[KCr(SO4)2]溶液制备,阴极的电极反应式为____。
-
下列有关物质的性质、应用或制取的说法正确的是( )
A.常温下浓硝酸与铝不反应,可用铝制容器存放浓硝酸
B.除去氯化钙溶液中少量盐酸,加入足量碳酸钙粉末,充分搅拌再过滤
C.自来水厂可用硫酸铁对水进行消毒杀菌
D.水晶项链和餐桌上的瓷盘都是硅酸盐制品
-
(16分)氯化亚铜(CuCl)是有机合成工业中应用较广泛的催化剂,它是白色粉末,微溶于水,不溶于乙醇,在空气中会被迅速氧化。从酸性电镀废液(主要含Cu2+、Fe3+)中制备氯化亚铜的工艺流程如下:
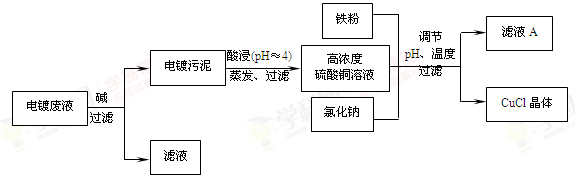
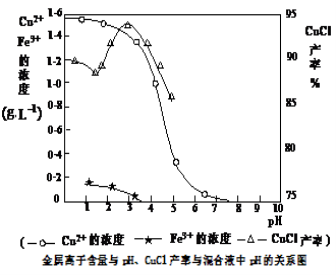
请回答下列问题:
(1)电镀污泥的主要成分是 (写化学式)。
(2)铁粉、氯化钠、硫酸铜在溶液中反应生成CuCl的离子反应方程式为:
。
(3)析出CuCl晶体时的最佳pH在 左右。
(4)析出的CuCl晶体要立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装。真空干燥,密封包装的目的是 。
(5)从滤液A中可回收的主要物质是 (写化学式)。
(6)以碳棒为电极电解CuCl2溶液可得到CuCl。写出电解CuCl2溶液后的阴极上发生的反应为
-
铜及其化合物应用广泛。
Ⅰ.氯化亚铜(CuCl)广泛用于化工、印染、有机合成等行业。以海绵铜(主要成分是Cu和少量CuO) 为原料,采用硝酸铵氧化分解技术生产氯化亚铜的工艺过程如下:
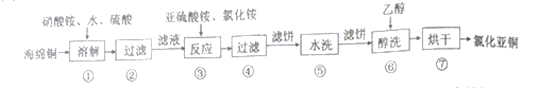
已知:CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易氧化。回答下列问题:
(1)步骤①中N 元素被还原为最低价,则Cu溶解的离子方程式为_______________。
(2)步骤③中(NH4)SO3要适当过量,目的是使Cu2+充分还原,并保证Cu2+的还原速率和_____,其主要反应的离子方程式________________。已知NH4Cl、Cu2+的物质的量之比[n(NH4Cl]/n(Cu2+)] 与Cu2+沉淀率的关系如下图所示,当氯化铵用量增加到一定程度后Cu2+的沉淀率减少,原因是_____________________。
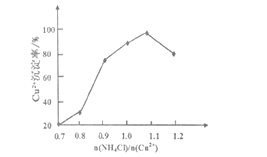
(3)步骤⑥中醇洗的目的是____________________________。
Ⅱ.以氧缺位铁酸铜(CuFe2O4-x)作催化剂,可利太阳能热化学循环法分解H2O制H2,其物质转化如图所示。
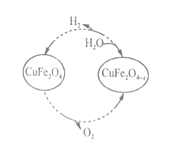
(4)氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式为_______________。
(5)若x=0.15,则1mol CuFe2O4-x参与一次该循环,理论上能制得的H2体积为_______L(标准状况下)。
-
硫酸镍广泛应用于电镀、催化、医药等行业中,具有很高的经济价值。一种用含镍废催化剂(主要含 、C,还含有铝、铁的单质及氧化物,和少量有机物)为原料制备
、C,还含有铝、铁的单质及氧化物,和少量有机物)为原料制备 的工艺流程如下:
的工艺流程如下:

部分阳离子以氢氧化物形式沉淀时的 如下:
如下:
| 沉淀物 | 开始沉淀时的 | 完全沉淀时的 |
| 
| 2.7 | 3.2 |
| 
| 7.6 | 9.7 |
| 
| 7.1 | 9.2 |
回答下列问题:
(1)滤液a中溶质的主要成分除 外,还含有_________________(填化学式)。
外,还含有_________________(填化学式)。
(2)酸溶前需进行“热处理”的主要目的是____________;滤渣b主要成分是________(填化学式)。
(3)加入 溶液时发生反应的离子方程式为_______;简述加入
溶液时发生反应的离子方程式为_______;简述加入 除杂的原理_______。
除杂的原理_______。
(4)操作d为________、过滤、洗涤、干燥;产品晶体中有时会混有少量 ,其原因可能是__________。(写出一点即可)
,其原因可能是__________。(写出一点即可)
(5)取ag上述流程制得的硫酸镍晶体样品溶于蒸馏水中,在不断搅拌下缓慢加入足量丁二酮肟溶液 ,再加入
,再加入 溶液调节溶液的
溶液调节溶液的 在8~9,充分反应后,过滤、洗涤、烘干、称量得到红色固体质量为bg。发生反应的方程式为
在8~9,充分反应后,过滤、洗涤、烘干、称量得到红色固体质量为bg。发生反应的方程式为 (红色)
(红色) ,已知
,已知 相对分子质量为M,列式计算样品纯度为_________。
相对分子质量为M,列式计算样品纯度为_________。

Fe(OH)3+3H+的平衡常数为_____________________。













