-
(1)下图对三种不同类型汽车(以序号1、2、3表示)的废气排放情况进行了比较。废气中的有害成分主要是:碳氢化合物、一氧化碳(CO)、氮氧化物(NOx)、二氧化碳(CO2),这三种汽车分别是以汽油为燃料的汽车、以天然气(主要成分是甲烷)为燃料的汽车和电动汽车。请判断其中序号为1的是________汽车,序号为3的是________汽车。

(2)一氧化氮是大气污染物之一。目前,有一种治理方法是在400°C左右、有催化剂存在的情况下,用氨气把一氧化氮还原为无毒气体。请写出该反应的化学方程式:_______________。
-
汽车尾气污染是由汽车排放的废气造成的环境污染。主要污染物为一氧化碳、碳氢化合物、氮氧化合物等,对人类和动、植物危害甚大。解决汽车尾气问题的主要方法是研究高效催化剂促使尾气中的一氧化碳和氮氧化物反应,转化成无污染的氮气和二氧化碳。
回答下列问题:
(1)在Co+的催化作用下,CO(g)还原N2O(g)的反应历程和能量变化如图所示(逸出后物质认为状态下发生变化,在图中略去)。已知总反应的化学方程式为:CO(g)+N2O(g) CO2(g)+N2(g)。
CO2(g)+N2(g)。
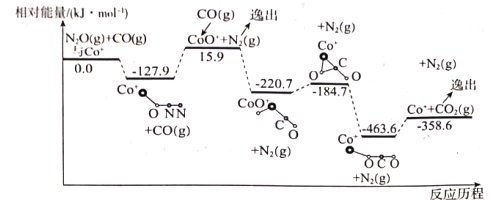
该反应分两步进行:
第一步:Co+(s)+N2O(g) CoO+(s)+N2(g) △H1=+15.9kJ•mol-1;
CoO+(s)+N2(g) △H1=+15.9kJ•mol-1;
笫二步:___;△H2=___;
①填写第二步反应的热化学方程式,并根据反应历程图计算△H2的数值。
②该反应的最高能垒(活化能)为___。
(2)500℃条件下,在容积均为2L的三个密闭容器中,按不同方式投入反应物,发生上述反应,测得相关数据如下表:
| 容器 | 反应物投入的量 | 平衡时 n(N2/mol) | 达到平衡所需时间/min | 平衡时能量变化/kJ |
| 甲 | 1molCO和1molN2O | n1 | t1 | 放热Q1 |
| 乙 | 2molCO和2molN2O | n2 | t2 | 放热Q2 |
| 丙 | 2molCO2和2molN2 | n3 | t3 | 吸热Q3 |
①Q1+ ___358.6(填“>”“=”或“<”下同,t1___t2;
___358.6(填“>”“=”或“<”下同,t1___t2;
②500℃条件下,乙和丙两容器,气体混合物中N2O的物质的量分数x(N2O)与反应时间t的关系如下表:
| t/s | 0 | 20 | 40 | 60 | 80 | 120 |
| 乙 | x(N2O) | 0.5 | 0.32 | 0.20 | 0.12 | 0.088 | 0.07 |
| 丙 | x(N2O) | 0 | 0.030 | 0.048 | 0.059 | 0.065 | 0.07 |
根据上述实验结果,计算出乙容器中0~20s时间内的化学反应速率v(CO)=___;该反应的平衡常数K数值为:___;(保留3位有效数字)
③请推测并在图中画出甲容器中x(N2O)随时间变化的关系图象,标出恰好达到平衡时刻点的位置___。

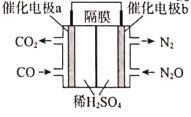
(3)若将CO(g)还原N2O(g)的反应设计成如图的原电池装置,则该电池正极的电极反应式为___。
-
氮氧化物是大气主要污染物,主要来自于工业废气及汽车尾气的排放,工业废气中NO是主要成分之一。
(1)乙烯作为还原剂的脱硝(NO),其反应机理示意图如图所示.写出解吸过程的化学方程式____________________。

(2)FeSO4-Na2SO3复合吸收剂吸收烟气中的NO,该方法利用Fe2+易与NO发生络合反应的特性,原理如下NO+FeSO4 Fe(NO)SO4
Fe(NO)SO4
①如图是一段时间内不同吸收剂对NO脱除率对比,加入Na2SO3溶液后,吸收效率增强,除了Na2SO3也能吸收部分NO外,还能防氧化从而增大Fe2+的含量,写出此原理的离子方程式_______________________________________。

②模拟实验表明,温度过高或过低都会降低NO的脱除率,其原因是_______________________________________。
(3)采用无隔膜法电解食盐水脱氮可将氮氧化物转化成NO3-,原理如图
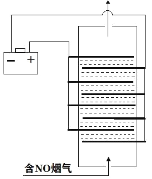
①无隔膜条件下电解食盐水后溶液呈弱碱性,原因是____________________________.
②写出NO发生反应的离子方程式____________________________。
③根据下图所示,脱NO过程中控制溶液pH在______________范围内更合理。

-
氮氧化物是大气主要污染物,主要来自于工业废气及汽车尾气的排放,工业废气中NO是主要成分之一。
(1)乙烯作为还原剂的脱硝(NO),其反应机理示意图如图所示.写出解吸过程的化学方程式____________________。

(2)FeSO4-Na2SO3复合吸收剂吸收烟气中的NO,该方法利用Fe2+易与NO发生络合反应的特性,原理如下NO+FeSO4 Fe(NO)SO4
Fe(NO)SO4
①如图是一段时间内不同吸收剂对NO脱除率对比,加入Na2SO3溶液后,吸收效率增强,除了Na2SO3也能吸收部分NO外,还能防氧化从而增大Fe2+的含量,写出此原理的离子方程式_______________________________________。

②模拟实验表明,温度过高或过低都会降低NO的脱除率,其原因是_______________________________________。
(3)采用无隔膜法电解食盐水脱氮可将氮氧化物转化成NO3-,原理如图

①无隔膜条件下电解食盐水后溶液呈弱碱性,原因是____________________________.
②写出NO发生反应的离子方程式____________________________。
③根据下图所示,脱NO过程中控制溶液pH在______________范围内更合理。

-
环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中的氮氧化物(NOx)、CO等有害气体,消除方法有多种。
(1)用稀土等催化剂能将汽车尾气中的CO、NOx、碳氢化合物转化成无毒物质,从而减少汽车尾气污染。已知:
①N2(g)+ O2(g)=2NO(g) △H=180.5 kJ/mol
②2C(s)+ O2(g)=2CO(g) △H=—221kJ/mol
③C(s)+ O2(g)=CO2(g) △H=—393. 5 kJ/mol
写出NO(g)与CO(g)催化转化成N2(g)和CO2(g)的热化学方程式__________________。
(2)①用甲烷催化还原氮的氧化物可消除氮氧化物的污染CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g) ΔH=QkJ·mol-1,写出上述反应的平衡常数表达式_______,已知该反应的平衡常数K随温度升高而减小,则Q_______0(填“>”或“<”或“=”)。
2N2(g)+CO2(g)+2H2O(g) ΔH=QkJ·mol-1,写出上述反应的平衡常数表达式_______,已知该反应的平衡常数K随温度升高而减小,则Q_______0(填“>”或“<”或“=”)。
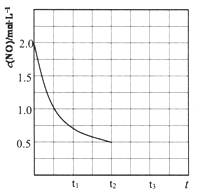
②某温度下,密闭容器中CH4与NO的起始浓度分别为1mol/L、2mol/L,其中c(NO)随时间变化如图所示,t2时达到平衡,保持温度不变在t2时将容器容积压缩到一半,请画出t2-t3 c(CH4)随时间变化的曲线。_______
(3)①为提高反应:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g)中的转化率,可以采取在恒压条件下充入稀有气体,解释其原因______________。
N2(g)+CO2(g)+2H2O(g)中的转化率,可以采取在恒压条件下充入稀有气体,解释其原因______________。
②电解吸收法处理氮氧化物废气的基本原理是用硝酸吸收氮氧化物生成NO2-,同时用石墨电极电解将NO2-转化成NO3-,电解条件下循环利用NO3-来处理氮氧化物。写出该法处理NO2总反应的化学方程式_______。
-
煤是一种常用的燃料。由于煤燃烧产生的废气中含有SO2、NO2和NO等多种有害气体和烟尘,会对环境造成污染,因此需要对煤进行加工后再燃烧,或将废气净化后再排放。
(1)将煤直接进行燃烧,造成环境污染的主要原因之一是形成硝酸型酸雨。
①写出有关物质转化为硝酸的化学方程式____________________________。
②以下是对硝酸型酸雨的评价,其中正确的是_________________________(用序号填空)。
a.杀死水中的浮游生物,减少鱼类食物来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.破坏臭氧层
d.硝酸与土壤中的矿物质发生作用转化为硝酸盐,向植物提供氮肥
(2)如图是对煤燃烧产生的废气进行常温脱硫处理的基本流程示意图,试写出在废气脱硫并形成副产物的过程中所发生的主要化学反应的化学方程式_______。
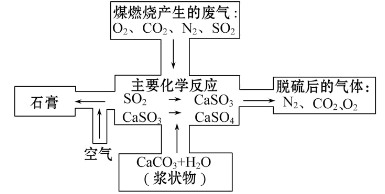
(3)脱硫以后,在废气中含量明显增加的不良气体是(写物质名称)_______,它对环境的负面影响是____________________________________________。
(4)检验脱硫后废气中是否含有SO2的简单方法是_________________________。
-
煤是一种常用的燃料,由于煤燃烧产生的废气含有SO2、NO2和NO等多种有害气体和烟尘会对环境造成污染,因此需要对煤进行加工后再燃烧,或将废气净化后再排放
(1)将煤直接进行燃烧,造成环境污染的主要方面之一是形成硝酸型酸雨
①写出有关物质转化为硝酸的化学方程式
②以下是对硝酸型酸雨的若干项评价,其中正确的是________
a:杀死水中的浮游生物,减少鱼类食物的来源,破坏水生生态系统
b:对电线,铁轨,桥梁,房屋等均会造成严重损害
c:导致臭氧层空洞
d:硝酸与土壤中的矿物质发生作用转化为硝酸盐,向植物提供氮肥。
(2)对煤用石灰石进行脱硫处理,过程中发生的方程式为:
(3)脱硫后,在废气中含有的不良气体是________,它对环境的负面影响是________。
(4)检验脱硫后废气中是否含有SO2的简单方法是________。
-
煤是一种常用的燃料。由于煤燃烧产生的废气中含有SO2、NO2和NO等多种有害气体和烟尘会对环境造成污染,因此需要对煤进行加工后再燃烧,或将废气净化后再排放。
(1)将煤直接进行燃烧,造成环境污染的主要原因之一是形成硝酸型酸雨。
①写出有关物质转化为硝酸的化学方程式______________________________________。
②以下是对硝酸型酸雨的评价,其中正确的是________(用序号填空)。
a.杀死水中的浮游生物,减少鱼类食物来源,破坏水生生态系统;
b.对电线、铁轨、桥梁、房屋等均会造成严重损害;
c.破坏臭氧层;
d.硝酸与土壤中的矿物质发生作用转化为硝酸盐,向植物提供氮肥。
(2)下图是对煤燃烧产生的废气进行常温脱硫处理的基本流程示意图,试写出在废气脱硫并形成副产物的过程中所发生的主要化学反应的化学方程式____________________________。
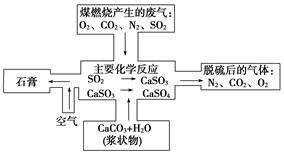
(3)脱硫以后,在废气中含量明显增加的不良气体是(写物质名称)________,它对环境的负面影响是______________________________________________________________________。
(4)检验脱硫后废气中是否含有SO2的简单方法是__________________________________。
-
燃煤废气、汽车尾气中的氮氧化物(NOx)、一氧化碳等有害气体,常用下列方法处理,以减少对环境的污染。
(1)对燃煤废气进行脱硝处理时,常利用甲烷催化还原氮氧化物,如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H =-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H =-1160 kJ·mol-1
则1molCH4将NO2还原为N2的反应热为________;
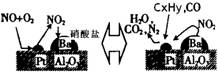
(2)除氮氧化物及CO外,汽车尾气中还含有碳氢化合物等污染物,下图是汽车尾气转化研究的示意图:表示的是Pt/Al2O3/Ba表面吸附与解吸作用的机理,氮氧化物是NO2,碳氢化合物是CxHy,写出两者反应的化学方程式:________,Pt/Al2O3/Ba的作用是________;
(3)平衡常数K的数值大小,是衡量化学反应进行程度的标志,K的数值越大,化学反应的限度越大,反应物反应的越充分。在25℃时,下列反应的平衡常数如下:
N2(g)+O2(g)  2NO(g) K1=1×10-30 ㈠
2NO(g) K1=1×10-30 ㈠
2H2(g)+O2(g)  2H2O(g) K2=2×1081 ㈡
2H2O(g) K2=2×1081 ㈡
2CO2 (g)  2CO(g)+O2(g) K3=4×10-92 ㈢
2CO(g)+O2(g) K3=4×10-92 ㈢
 ①常温下,反应2H2O(g) 2H2(g) +O2(g) 平衡常数K=________;
①常温下,反应2H2O(g) 2H2(g) +O2(g) 平衡常数K=________;
②关于以上反应,下列说法正确的是________
A.常温下,NO,H2O,CO2三种化合物分解放出氧气的倾向大小顺序:NO>H2O>CO2
B.若升高温度,反应㈢的平衡常数K3将增大
C.若只增加压强,且反应物、生成物状态不变,反应㈠平衡不发生移动,平衡常数不变;反应㈡平衡朝正向移动,平衡常数增大
D.若增加汽车发动机空气的进气量,可同时减少氮氧化物和一氧化碳的排放
③基于环保法规,要求改装汽车尾气处理装置,达到使氮氧化物(NO)、一氧化碳转化为无污染、可排放的气体的目的。改装的方法主要是加入有效催化剂,请你根据以上有关数据分析,在不改变其它条件的情况下,可使用催化剂除污染气体的原因:________。
-
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是
| 氧化物 | 环境问题 | 主要来源 |
| A | CO2 | 酸雨 | 化石燃料的燃烧 |
| B | SO2 | 光化学烟雾 | 汽车尾气的排放 |
| C | NO2 | 温室效应 | 工厂废气的排放 |
| D | CO | CO中毒 | 燃料的不完全燃烧 |














