-
(6分)某次采集酸雨样品,每隔一段时间测定一次pH,得到数据如下
时间
开始
8小时
16小时
24小时
32小时
40小时
48小时
pH
5.0
4.8
4.5
4.3
4.2
4.0
4.0
(1)放置时,雨水样品pH变化的主要原因。
(2)pH变化的离子方程式:________
高三化学填空题简单题查看答案及解析
-
酸雨主要是含硫燃料燃烧时释放出的SO2造成的,现收集到雨水样品一份,并每隔一段时间测定该雨水样品的pH,数据如下:
测定时间(时)
0
1
2
4
8
雨水pH
4.73
4.62
4.56
4.55
4.55
试说明上述时间里,雨水样品pH变化的原因_____________________________________。
高三化学选择题中等难度题查看答案及解析
-
A.大量的______和______扩散到大气中,在空气.阳光等作用下发生一系列变化,遇雨时被雨水吸收,当雨水的pH小于______时就形成了酸雨.
某校科技小组的同学们采集酸雨样品,每隔一段时间测定样品的pH,得到下列数据:
回答下列问题:时间 开始 8h后 16h后 24h后 32h后 40h后 48h后 pH 5.0 4.8 4.5 4.3 4.2 4.0 4.0
(1)酸雨放置时,pH发生变好的主要原因为______.
(2)煤中含有游离态的硫,试写出它经过一系列变化最后变成酸雨主要成分的有关化学方程式.(空线不一定填满)______ SO2高三化学解答题中等难度题查看答案及解析
-
俗称海波
是常用的一种定影剂。工业使用的海波中常混有少量
和
的杂质,为测定一种海波晶体样品的成分,某同学称取三份质量不同的该样品,分别加入相同浓度的稀硫酸20mL,充分反应后测得有关实验数据如下
标准状况
。
第一份
第二份
第三份
样品的质量
二氧化硫的体积
硫的质量
下列说法错误的是
A.第一份、第二份样品均完全反应,第三份样品过量
B.样品中
:
:1
C.样品中除了含有
、
,还含有
D.所加硫酸溶液的物质的量浓度为
高三化学单选题中等难度题查看答案及解析
-
我国农业因遭受酸雨而造成每年损失高达15亿多元。为了有效控制酸雨,目前国务院已批准了〈〈酸雨控制区和二氧化硫污染控制区划分方案〉〉等法规。现有雨水样品1份,每隔一段时间测定该雨水样品的ph,所得数据如下:
测试时间
0
1
2
3
4
雨水的ph
4.73
4.62
4.56
4.55
4.55
分析数据,回答下列问题:
(1)雨水样品的pH变化的原因是(用化学方程式表示)________
(2)你认为减少酸雨产生的途径可采用的措施是________(填序号)
①少用煤作燃料 ②把工厂烟囱造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A、①②③ B、②③④⑤ C、①③⑤ D、①③④⑤
(3)在英国进行的一个研究表明:高烟囱可以有效地降低地表SO2浓度。在20世纪的60年代~70年代的10年间,由发电厂排放出上午SO2增加了35%,但由于建筑高烟囱的结果,地面降低了30%之多。请你从全球环境保护的角度,分析这种方法是否可取?。
高三化学填空题中等难度题查看答案及解析
-
在
时,将
气体充入 2L 密闭容器中,发生下列反应:
,每隔一段时间对该容器的物质进行测量,得到的数据如表:下列说法中正确的是
时间
0
20
40
60
80
A.反应开始 20 s 内
的平均反应速率是
B.80 s 时混合气体的颜色与 60 s 时颜色相同,比 40 s 时的颜色深
C.80 s 时向容器内加
mol He,容器体积保持不变,化学反应速率加快
D.80s 时升高温度,则正反应速率加快,逆反应速率也加快
高三化学单选题简单题查看答案及解析
-
在100℃时,将0.40 mol NO2气体充入2 L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:
时间(s)
0
20
40
60
80
n(NO2)(mol)
0.40
n1
0.26
n3
n4
n(N2O4)(mol)
0.00
0.05
n2
0.08
0.08
下列说法中正确的是( )
A.反应开始20 s内NO2的平均反应速率是0.001 mol·L-1·s-1
B.80 s时混合气体的颜色与60 s时颜色相同,比40 s时的颜色深
C.80 s时向容器内加0.32 mol He,同时将容器扩大为4 L,则平衡不移动
D.若起始投料为0.20 mol N2O4,相同条件下达到平衡,则各组分的含量与原平衡相同
高三化学选择题困难题查看答案及解析
-
在100 ℃时,将0.40 mol二氧化氮气体充入2 L密闭容器中,每隔一段时间对该容器内
的物质进行分析,得到如下数据:
时间(s)
0
20
40
60
80
n(NO2)/mol
0.40
n1
0.26
n3
n4
n(N2O4)/mol
0.00
0.05
n2
0.08
0.08
下列说法中正确的是( )
A.反应开始20 s内以二氧化氮表示的平均反应速率为0.001 25 mol·L-1·s-1
B.80 s时混合气体的颜色与60 s时相同,比40 s时的颜色深
C.80 s时向容器中加入0.32 mol氦气,同时将容器扩大为4 L,则平衡将不移动
D.若起始投料为0.20 mol N2O4,相同条件下达平衡,则各组分含量与原平衡体系对应相等
高三化学选择题中等难度题查看答案及解析
-
在100℃时,将0.40mol二氧化氮气体充入2L密闭容器中,每隔一段时间对该容器内的得到数据如下
时间(s)
0
20
40
60
80
n(NO2)/mol
0.40
n1
0.26
n3
n4
n(N2O4)/mol
0.00
0.05
n2
0.08
0.08
下列说法中正确的是
A.反应开始20s内以二氧化氮表示的平均反应速率为0.00125mol·L-1·s-
B.80s时混合气体的颜色与60s时相同,比40s时的颜色深
C.80s时向容器中加入0.32mol氦气,同时将容器扩大为4L,则平衡将不移动
D.若起始投料为0.20molN2O4,相同条件下达平衡,则各组分含量与原平衡体系对应相等
高三化学选择题困难题查看答案及解析
-
(15分)在100℃时,将0.40mol的二氧化氮气体充入2L抽空的密闭容器中,发生反应:
2NO2
N2O4。每隔一定时间就对该容器内的物质进行分析,得到如下表数据:
时间/s
0
20
40
60
80
n(NO2)/mol
0.40
n1
0.26
n3
n4
n(N2O4)/mol
0.00
0.05
n2
0.08
0.08
(1)在上述条件下,从反应开始直至20 s时,二氧化氮的平均反应速率为__________
mol/(L·s)。
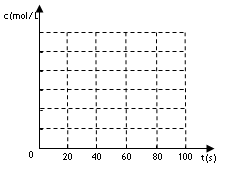
(2)若在相同情况下最初向该容器充入的是四氧化二氮气体,要达到上述同样的平衡状态,四氧化二氮的起始浓度是_________mol/L。假设在80s时达到平衡,请在如图中画出该条
件下N2O4和NO2的浓度随时间变化的曲线。
(3)上述(2)达到平衡后四氧化二氮的转化率为_________,混合气体的平均摩尔质量
为___________。
(4)达到平衡后,如向该密闭容器中再充入0.32molHe气,并把容器体积扩大为4L,则平衡将________(填“向左移动”、“向右移动”或“不移动”)。
高三化学填空题简单题查看答案及解析