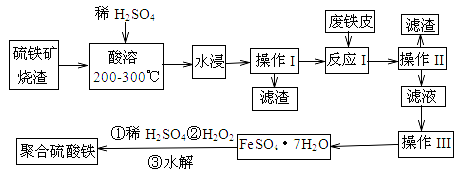-
(13分)氯化铁是一种重要的化学试剂和化工原料,工业上以黄铁矿(主要成分为FeS2)为原料在制备硫酸的同时,利用其煅烧后炉渣的主要成分Fe2O3可制备氯化铁晶体(FeCl3·6H2O),其工艺流程如下(杂质不参与反应):
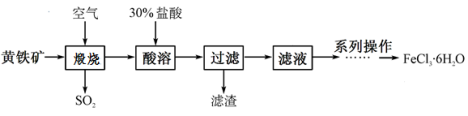
回答下列问题:
(1)高温煅烧时,黄铁矿要粉碎成细小的颗粒,其目的是 。
(2)黄铁矿高温煅烧时发生反应的化学方程式 。
(3)酸溶及后续过程中均需保持盐酸过量,其目的是 、 。
(4)系列操作包括:蒸发浓缩、 、 、洗涤等。蒸发与过滤时玻璃棒的作用分别是: 、 。
(5)取a g黄铁矿,按上述流程制得FeCl3·6H2O晶体,将该晶体溶于水,再将所得溶液蒸干、灼烧,得到b g固体产物(整个过程中的损耗忽略不计),黄铁矿的纯度为 (用含a、b的表达式表示)。
-
黄铁矿既是硫矿又是铁矿,因其呈黄色俗称“愚人金”,是重要的工业原料。工业煅烧过程中常产生废渣,废渣成分主要含铁的几种氧化物和二氧化硅等,利用该废渣可以制备高效净水剂聚合硫酸铁,工艺流程如下:
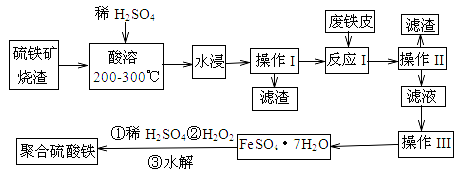
(1)检验“酸溶”后的溶液中含有Fe2+,试剂是 。
(2)硫铁矿烧渣在“酸溶”前要粉碎的主要目的是 。
(3)废铁皮使用前要用纯碱溶液浸泡,目的是 。
(4)“酸溶”过程中Fe2O3溶解的化学反应方程式为 。
(5)“操作Ⅲ”系统操作名称依次为 、 、过滤和洗涤。洗涤的方法是 。
(6)加入适量H2O2的目的是氧化Fe2+,写出H2O2氧化Fe2+为Fe3+的离子方程式: 。
-
(18分)以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
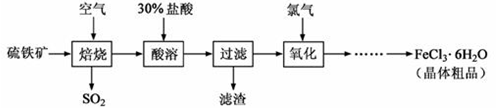
回答下列问题:
(1)将煅烧黄铁矿的化学方程式补充完整:________+________  Fe2O3+ SO2↑;该反应中,FeS2为 剂;SO2为 产物,其常常用于制备硫酸,反应过程中的化学反应方程式为 ________ 、 ________ ;
Fe2O3+ SO2↑;该反应中,FeS2为 剂;SO2为 产物,其常常用于制备硫酸,反应过程中的化学反应方程式为 ________ 、 ________ ;
(2)酸溶及后续过程中均需保持盐酸过量,其目的是 、 ;
(3)通氯气氧化后时,发生的主要反应的离子方程式为 ;
(4)该过程产生的污染空气的气体有三种,尾气均可用强碱溶液吸收,这些反应的离子方程式为 ________ ;。
(5)从FeCl3溶液中得到FeCl3.6H2O晶体的操作为 ________ 。
-
(14分) 硫酸是工业生产中一种重要的化工产品,我国工业生产硫酸的主要方法是接触法,主要原料为黄铁矿,请回答下列问题:
(1)已知煅烧黄铁矿的化学方程式为 4FeS2 + 11O2  2Fe2O3 + 8SO2
2Fe2O3 + 8SO2
该反应中氧化剂和氧化产物之比为 ________;标准状态下得到4.48升SO2 时,一共转移了 ________mol e- 。(每空3分)
(2)已知温度、压强对SO2平衡转化率的影响如下表所示:根据上表回答,SO2转化到SO3的
最佳反应条件是________。(每空2分)
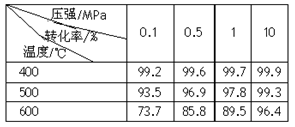
A.400-500℃ 0.1 MPa B.400℃ 10 MPa
C.500℃ 10 MPa D.400-500℃ 1 MPa
(3)在一定条件下,1mol SO2完全转化成SO3气体时放出热量为Q1 KJ,写出该反应的热化学方程式:________。若在该条件下将2 mol SO2 放入一定容积的密闭容器中,一段时间后测得反应放出热量为Q2 KJ,则此时SO2的转化率为________ (用含Q1、Q2代数式表示)。(每空2分)
(4)市售浓硫酸的密度是1.84 g / cm3、质量分数为98 % ,若用H2SO4· XH2O来表示这种浓硫酸,则X为________ 。(每空2分)
-
(12分)黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
(1)将0.050 mol SO2(g)和0.030 mol O2(g)放入容积为1 L的密闭容器中,反应
2SO2(g)+O2(g)  2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。则该条件下反应的平衡常数K=________,SO2的平衡转化率=________。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040 mol/L。则该条件下反应的平衡常数K=________,SO2的平衡转化率=________。
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有________(填字母)
(A)升高温度 (B)降低温度 (C)增大压强
(D)减小压强 (E)加入催化剂 (G)移出氧气
(3)SO2尾气用饱和Na2SO3溶液吸收可得到重要的化工原料,反应的化学方程式为________________________________________________________________。
(4)将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需保持溶液足够酸性,其原因是______________________。
-
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
(1)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g) + O2(g) 2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有________(填字母)
A、升高温度 B、降低温度 C、增大压强 D、减小压强
E、加入催化剂 G、移出氧气
(3)SO2尾气用饱和Na2SO3溶液吸收可得到更要的化工原料,反应的化学方程式为________。
(4)将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需保持溶液足够酸性,其原因是________。
-
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
(1)将0.050 mol SO2(g)和0.030 mol O2(g)放入容积为1 L的密闭容器中,反应
2SO2(g)+O2(g)  2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040
2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040
mol/L。计算该条件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
(2)已知上述反应是放热反应,当该反应处于平衡状态时,下列措施中有利于提高SO2平衡转化率的有________(填字母)
(A)升高温度 (B)降低温度
(C)增大压强 (D)减小压强
(E)加入催化剂 (G)移出氧气
(3)SO2尾气用饱和Na2SO3溶液吸收可得到重要的化工原料,反应的化学方程式为________________________________________________________________。
(4)将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4。酸溶过程中需保持溶液足够酸性,其原因是______________________。
-
【化学―选修2:化学与技术】以硫铁矿(主要成分为FeS2)为原料制取硫酸,其矿渣可用来炼铁。生产工艺示意图如下:

(1)配平煅烧硫铁矿的反应方程式:______FeS2+________O2→_____Fe2O3+______SO2。实际生产中向沸腾炉通入的空气量要大于锻烧硫铁矿所需空气量.其目的是____________________。接触室和热风炉中都装有热交换器,可用反应的余热将通入的气体加热,这样做的好处是_____________________。
(2)生产硫酸时,吸收塔中用98.3%的硫酸吸收而不用水吸收SO3的原因是______________。用含FeS280%的硫铁矿生产硫酸,如果煅烧时有5%的硫损失,SO2转变成SO3的转化率为80%,那么生产98%的浓硫酸3吨,则需要这种硫铁矿___________吨。
(3)CO还原Fe2O3的冶铁过程中,反应物、生成物和温度之间的关系如图所示.

(图中Ⅰ、Ⅱ、Ⅲ、Ⅳ四条曲线是四个化学反应平衡时的气相组成对温度作图得到的;A、B、C 、D四个区域分别是Fe2O3、Fe3O4、FeO、Fe稳定存在的区域)
、D四个区域分别是Fe2O3、Fe3O4、FeO、Fe稳定存在的区域)
①冶炼高炉产生的高炉煤气的主要成分有__________和剩余的CO。
②据图分析,下列说法正确的是________(填字母)。
a.温度低于570 ℃时,Fe2O3还原焙烧的产物中不含FeO
b.温度越高,Fe2O3还原焙烧得到的 固体物质组成中Fe元素的质量分数越高
固体物质组成中Fe元素的质量分数越高
c.Fe2O3还原焙烧过程中及时除去CO2有利于提高Fe的产率
③800℃时,混合气体中CO2体积分数为40%时,Fe2O3用CO还原焙烧反应的化学方程式为____________。
-
【化学―选修2:化学与技术】以硫铁矿(主要成分为FeS2)为原料制取硫酸,其矿渣可用来炼铁。生产工艺示意图如下:
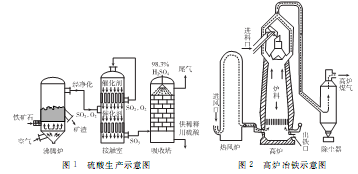
(1)配平煅烧硫铁矿的反应方程式:______FeS2+________O2→_____Fe2O3+______SO2。实际生产中向沸腾炉通入的空气量要大于锻烧硫铁矿所需空气量.其目的是____________________。
接触室和热风炉中都装有热交换器,可用反应的余热将通入的气体加热,这样做的好处是_____________________。
(2)生产硫酸时,吸收塔中用98.3%的硫酸吸收而不用水吸收SO3的原因是________。
用含FeS280%的硫铁矿生产硫酸,如果煅烧时有5%的硫损失,SO2转变成SO3的转化率为80%,那么生产98%的浓硫酸3吨,则需要这种硫铁矿___________吨。
(3)CO还原Fe2O3的冶铁过程中,反应物、生成物和温度之间的关系如图所示.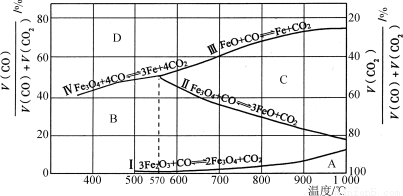
(图中Ⅰ、Ⅱ、Ⅲ、Ⅳ四条曲线是四个化学反应平衡时的气相组成对温度作图得到的;A、B、C、D四个区域分别是Fe2O3、Fe3O4、FeO、Fe稳定存在的区域)
①冶炼高炉产生的高炉煤气的主要成分有__________和剩余的CO。
②据图分析,下列说法正确的是________(填字母)。
a.温度低于570 ℃时,Fe2O3还原焙烧的产物中不含FeO
b.温度越高,Fe2O3还原焙烧得到的固体物质组成中Fe元素的质量分数越高
c.Fe2O3还原焙烧过程中及时除去CO2有利于提高Fe的产率
③800℃时,混合气体中CO2体积分数为40%时,Fe2O3用CO还原焙烧反应的化学方程式为____________。
-
铁黄是一种重要的颜料,化学式为Fe2O3·xH2 O,广泛用于涂料、橡胶、塑料、文教用品等工业。实验室模拟工业利用硫酸渣(含FeZ 0。及少量的CaO, Mg0等)和黄铁矿粉
(主要成分为FeS2)制备铁黄的流程如下:
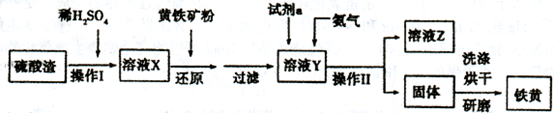
(1)操作I与操作II中都用到玻璃棒,玻璃棒在两种操作中的作用分别是_________、________
(2)试剂a最好选用_________(供选择使用的有:铝粉、空气、浓HNO3 );其作用是_________。
(3)上述步骤中需用到氨气。下列装置可用于实验室制氨气的是__________(填序号)。
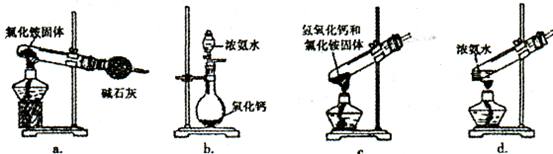
(4)查阅资料知,在不同温度下Fe2 O3被CO还原,产物可能为Fe3 O4 、FeO或Fe,固体质量与反应温度的关系如右图所示。根据图象推断670℃时Fe2 O3还原产物的化学式为M,并设计一个简单的实验,证明该还原产物的成分(依次填写每步操作中所加试剂的化学式、现象和结论)。仪器自选。可供选择的试剂:稀H2SO4、稀盐酸、H2 O2溶液、NaOH溶液、KSCN溶液。
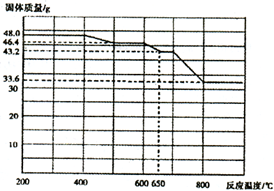
| 加入试剂 | 现象 | 结论 |
| | 则还原产物为________ |