-
某一种胃药中的抑酸剂为碳酸钙,其中所含的抑酸剂质量的测定如下:
①需配制0.1 mol·L-1的HCl溶液和0.1 mol·L-1的NaOH溶液
②取一粒(药片质量相同) 0.2 g的此胃药片,磨碎后加入20.0 mL蒸馏水
③以酚酞为指示剂,用0.1 mol·L-1的NaOH溶液滴定,用去V mL达滴定终点
④加入25 mL 0.1 mol·L-1的HCl溶液
(1)写出实验过程的步骤(写编号顺序) 。
(2)下图所示容器中配制0.1 mol·L-1的HCl溶液和0.1 mol·L-1的NaOH溶液肯定不需要的仪器是(填序号) ,配制上述溶液还需要的玻璃仪器是 (填仪器名称)。
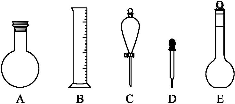
(3)配制上述溶液应选用的容量瓶规格是(填字母) 。
A.50 mL 50 mL
B.100 mL 100 mL
C.100 mL 150 mL
D.250 mL 250 mL
(4)写出有关的化学反应方程式: 、 。
(5)每粒胃药中含碳酸钙的质量为 g。
-
某一种胃药药片的抑酸剂为碳酸钙,其中所含的抑酸剂质量的测定如下:
①需配制0.1 mol/L的HCl溶液和0.1 mol/L的NaOH溶液;
②每次取一粒(药片质量均相同)0.2 g的此胃药片,磨碎后加入20 mL蒸馏水;
③以酚酞为指示剂,用0.1 mol/L的NaOH溶液滴定,需用去Vx mL达到滴定终点;
④加入25 mL 0.1 mol/L的盐酸溶液。
(1)写出全部实验过程的步骤顺序________(写编号顺序)。
(2)如图所示仪器中配制0.1 mol/L的HCl溶液和0.1 mol/L NaOH溶液肯定不需要的仪器是________(填序号),配制上述溶液还需要用到的玻璃仪器是________(填仪器名称)。
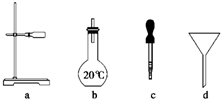
(3)配制上述溶液应选用的容量瓶规格分别为________(填字母)。
A.50 mL,50 mL B.100 mL,100 mL
C.100 mL,150 mL D.250 mL,250 mL
(4)写出反应的化学方程式____________________________________________。
(5)胃药中含CaCO3的质量________g(写出计算式并加以文字说明)。
-
某一种胃药中的抑酸剂为碳酸钙,其中所含的抑酸剂质量的测定如下:
①需配制0.1 mol·L-1的HCl溶液和0.1 mol·L-1的NaOH溶液
②取一粒(药片质量相同)0.2 g的此胃药片,磨碎后加入20.0 mL蒸馏水
③以酚酞为指示剂,用0.1 mol·L-1的NaOH溶液滴定,用去V mL达滴定终点
④加入25 mL 0.1 mol·L-1的HCl溶液
(1)写出实验过程的步骤(写编号顺序) 。
(2)下图所示容器中配制0.1 mol·L-1的HCl溶液和0.1 mol·L-1的NaOH溶液肯定不需要的仪器是(填序号) ,配制上述溶液还需要的玻璃仪器是 (填仪器名称)。
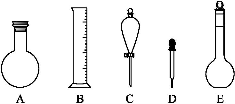
(3)配制上述溶液应选用的容量瓶规格是(填字母) 。
A.50 mL 50 mL
B.100 mL 100 mL
C.100 mL 150 mL
D.250 mL 250 mL
(4)写出有关的化学反应方程式: 、 。
(5)每粒胃药中含碳酸钙的质量为 g。
-
某项目小组同学发现某一种胃药片的止酸剂为碳酸钙,为了测定其中止酸剂的质量特制定了如下操作步骤:
①配制0.2mol·L-1的HCl溶液和0.2mol·L-1的NaOH溶液;②每次取一粒(药片质量均相同)0.2g的此胃药片,磨碎后放入锥形瓶中再加入20mL蒸馏水;③以酚酞作指示剂,用0.2mol·L-1的NaOH溶液滴定,需用去VmL达滴定终点;④加入25mL0.2mol·L-1的HCl溶液。
(1)写出全部实验过程的操作步骤的顺序:__。
(2)如图所示的仪器中配制0.2mol·L-1的HCl溶液和0.2mol·L-1NaOH溶液肯定不需要的仪器是__(填序号),配制上述溶液还需用到的玻璃仪器是__(填仪器名称)。
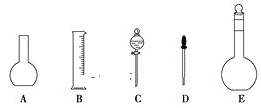
(3)配制上述溶液应选用的容量瓶的规格分别为__(填字母)。
A.50mL、50mL B.100mL、100mL
C.100mL、150mL D.250mL、250mL
(4)配制过程中,下列情况会使配制结果偏高的是__(填序号)。
A.洗净后容量瓶内还残留蒸馏水未烘干
B.量取浓盐酸时,仰视刻度线观察液面
C.定容时,仰视刻度线
D.定容后,加盖倒转摇匀后,发现液面低于刻度线又加水至刻度线
-
第三研究性学习小组发现某一种胃药片的制酸剂为碳酸钙,为了测定其中制酸剂的质量特制定了如下操作步骤:
①配制0.2 mol·L-1的HCl溶液和0.2 mol·L-1的NaOH溶液;②每次取一粒(药片质量均相同)0.2 g的此胃药片,磨碎后放入锥形瓶中再加入20 mL蒸馏水;③以酚酞作指示剂,用0.2 mol·L-1的NaOH溶液滴定,需用去V mL达滴定终点;④加入25 mL 0.2 mol·L-1的HCl溶液。
(1)写出全部实验过程的操作步骤的顺序:____________。
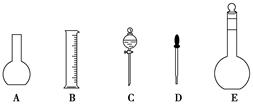
(2)上图所示的仪器中配制0.2 mol·L-1的HCl溶液和0.2 mol·L-1NaOH溶液肯定不需要的仪器是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。
(3)配制上述溶液应选用的容量瓶的规格分别为________(填字母)。
A.50 mL、50 mL B.100 mL、100 mL
C.100 mL、150 mL D.250 mL、250 mL
(4)写出相关的化学反应方程式:
________________________________________________________________________。
(5)做2次平行实验后,则每粒胃药片中含碳酸钙的质量表达式为________________g。
-
某种胃药片的制酸剂为碳酸钙,其中所含的制酸剂质量的测定如下:
①配制0.10 mol·L-1的 HCI和0.10mol·L-1的NaOH溶液
②取一粒(药片质量均相同)0.20g的此胃药片,磨碎后加入20.00mL蒸馏水
③以酚酞为指示剂,用0.1mol·L-1的NaOH溶液滴定至终点④加入50.00mL0.10 mol·L-1的HCl溶液
(1)写出实验过程中至少需要的步骤 (写编号顺序)。
(2)下图所示的仪器中配制0.10 mol·L-1HCl溶液和0.10 mol·L-1的NaOH溶液肯定不需要的仪器是(填序号) ,配制上述溶液还需要的玻璃仪器是(填仪器名称) 。
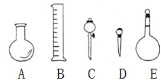
(3)配制0.1mol·L-1的NaOH溶液时,下列操作会使得所配溶液浓度变大的是 。
a.称量NaOH固体时动作过慢
b.溶解氢氧化钠时有部分液体溅出
c.未洗涤烧杯和玻璃棒
d.未冷却至室温就转移到容量瓶中
e.定容时俯视标线
f.摇匀后发现液面低于标线加水至标线
(4)写出有关反应的离子方程式
(5)若滴定消耗NaOH溶液体积为14.00mL,则该胃药中含碳酸钙的质量分数是 。
-
(8分)甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。实验方案如下:
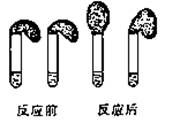
甲:①准确配制0.1mol·L-1的HA、HCl溶液各100mL;
②取纯度相同,质量、大小相等的锌粒放入两只试管中,同时加入0.1mol·L-1的HA、HCl溶液各100mL,按上图装好,观察现象。
乙:①用pH计测定物质的量浓度均为0.1mol·L-1的HA和HCl溶液的pH;
②再取0.1mol·L-1的HA和HCl溶液各2滴(1滴约为 )分别稀释至100mL,
)分别稀释至100mL,
再用pH计测其pH变化。
(1)乙方案中说明HA是弱电解质的理由是,测得0.1mol·L-1的HA溶液的pH________1(填“>”“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是________。
A.装HCl的试管中放出的氢气速率大
B.装HA溶液的试管中放出氢气的速率大
C.两个试管中产生气体速率一样大
(2)乙同学设计的实验第②步,能证明改变条件解质平衡发生移动。加水稀释,弱酸HA的电离程度________(填“增大、减小、不变”)
(3)甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:使HA的电离程度和c(H+)都减小,c(A)增大,可在0.1mol·L-1的HA溶液中,选择加入________试剂。
A.NaA固体(可完全溶于水) B.1mol·L-1NaOH溶液
C.1mol·L-1H2SO4 D.2mol·L-1HA
(4)pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如右图所示,则下列说法不正确的有________

A.若a=4,则A是强酸,B是弱酸
B.若 ,则A、B都是弱酸
,则A、B都是弱酸
C.两种酸溶液的物质的量尝试一定相等
D.稀释后,A溶液的酸性比B溶液弱
-
明矾[KAl(SO4)2·12H2O]是一种重要的化学试剂。下列说法正确的是( )
A.含明矾的药物不宜与胃药奥美拉唑碳酸氢钠胶囊同时服用
B.0.1mol·L-1明矾溶液完全水解生成Al(OH)3胶粒数小于6.02×1022
C.向含0.1mol明矾的溶液中滴入Ba(OH)2溶液,当生成沉淀的质量最大时,SO42-和Al3+全部转化为BaSO4和Al(OH)3沉淀
D.室温下,0.1mol·L-1明矾溶液中水电离出c(H+)小于10-7mol·L-1
-
25℃时,0.1 mol·L-1碳酸钠溶液中通入HCl气体,含碳粒子的浓度与pH的关系如下图所示。下列说法正确的是

A.在pH=7.0时,溶液中含碳粒子只有CO32-和HCO3-
B.向Na2CO3溶液中通入HCl气体,立即产生CO2气体
C.H2CO3的Ka2=1.0×10-10.25
D.向100 mL 0.1 mol·L-1碳酸钠溶液中滴加盐酸至溶液pH=4.0 ,生成CO2气体224 mL
-
碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y·zH2O。某校化学兴趣小组欲测定其化学式,实验设计如下:
实验I:称取一定质量的A,加热分解至恒重。
实验Ⅱ:称取一定质量的A与足量的酸反应,测量生成CO2气体的质量。
可供选择的仪器和药品如图所示:(酸溶液限选6mol/LHCl或6mol/LH2SO4,其它试剂任选。)

回答下列问题:
(1)仪器乙的名称为________。
(2)请选择必要的装置完成实验II,正确的连接顺序为________ (按气流方向,用接口字母表示);选用的酸溶液是________。
(3)有人提出不采用实验I,可在实验II结束后,在A完全反应后所得溶液中滴加足量的氨水,用无灰滤纸过滤,用蒸馏水洗涤反应容器2〜3次,将洗涤液过滤,洗涤沉淀2〜3次,将附着沉淀的滤纸放到坩埚中加热分解至恒重。判断沉淀已洗涤干净的方法是_________________,实际上未采用该方案的原因是不符合实验设计的________原则(填字母编号)。
A.科学性 B.安全性 C.可行性 D.简约性
(4)x与y的关系式是________ (用等式表示)。
(5)通过实验I的相关数据,经计算可得A的摩尔质量为602.0g. mol-1。实验II中称得样品A的质量为9.030g,与足量酸完全反应后,CO2吸收装置增重0.660g,则A 的化学式为________。









