-
乙酰乙酸乙酯是有机合成中非常重要的原料,实验室制备乙酰乙酸乙酯的反应原理、装置示意图和有关数据如下所示:
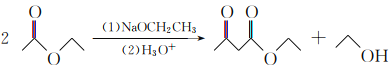
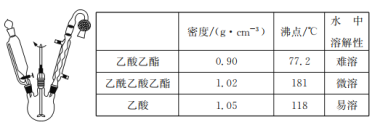
实验步骤:
(I)合成:向三颈烧瓶中加入9.8 mL无水乙酸乙酯,迅速加入0.1 g切细的金属钠。水浴加热反应液,缓慢回流约2h至金属钠全部反应完。停止加热,冷却后向反应混合物中加入50%乙酸至反应液呈弱酸性。
(II)分离与提纯:
①向反应混合物中加入等体积的饱和食盐水,分离得到有机层。
②水层用5 mL无水乙酸乙酯萃取,分液。
③将①②所得有机层合并,洗涤、干燥、蒸馏得到乙酰乙酸乙酯粗产品。
④蒸馏粗产品得到乙酰乙酸乙酯3.9g。
(l)迅速加入金属钠的原因是_________(用化学方程式说明)。
(2)球形冷凝管中冷却水从_____(填“上”或“下”)口进入,上方干燥管中盛有无水CaCl2,其作用是_______。
(3)实验室制备乙酰乙酸乙酯时,通常在无水乙酸乙酯中加入微量的无水乙醇,其作用是_______。
(4)分离与提纯操作①中使用的分离仪器是_______。加入饱和食盐水的作用是_______。
(5)分离与提纯操作③用饱和NaHCO3溶液洗涤的目的是______________。
(6)本实验的产率为______%(结果保留两位有效数字)。
-
乙酰乙酸乙酯是有机合成中非常重要的原料,实验室制备乙酰乙酸乙酯的反应原理、装置示意图和有关数据如下所示:
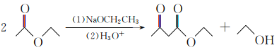
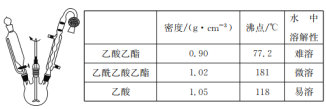
实验步骤:
Ⅰ.合成:向三颈烧瓶中加入9.8ml无水乙酸乙酯,迅速加入0.1g切细的金属钠。水浴加热反应液,缓慢回流约2h至金属钠全部反应完。停止加热,冷却后向反应混合物中加入50%乙酸至反应液呈弱酸性。
Ⅱ.分离与提纯:
①向反应混合物中加入等体积的饱和食盐水,分离得到有机层。
②水层用5mL无水乙酸乙酯萃取,分液。
③将①②所得有机层合并,洗涤、干燥、蒸馏得到乙酰乙酸乙酯粗产品。
④蒸馏粗产品得到乙酰乙酸乙酯3.9g。
(1)球形冷凝管中冷却水从______(填“上”或“下”)口进入,上方干燥管中盛无水CaCl2,其作用是________。
(2)实验室制备乙酰乙酸乙酯时,通常在无水乙酸乙酯中加入微量的无水乙醇,其作用是___。
(3)分离与提纯操作①中使用的分离仪器是________。加入饱和食盐水的作用是 _______。
(4)分离与提纯操作③用饱和NaHCO3溶液洗涤的目的是 _______。
(5)本实验的产率为_______ %(结果保留两位有效数字)。
-
环己酮是重要的化工原料,也是重要的工业溶剂。实验室制备环己酮的原理、有关数据及装置示意图如下:
反应原理: 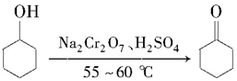
反应放热,温度过高或者重铬酸钠过量会进一步氧化。
主要物料及产物的物理参数:
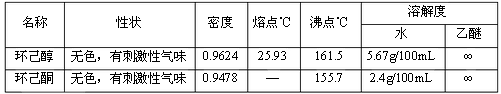
实验装置:
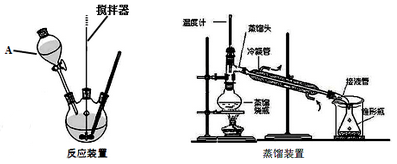
实验步骤:
1.投料:在100mL三颈烧瓶中加入20mL水,慢慢加入5mL浓硫酸摇动,振荡下缓慢加入5mL(4.8g,0.048mol)环己醇,并将混合液温度降至30℃以下。将5g(0.019mol)重铬酸钠溶于水得橙红色溶液备用。
2.反应:将约1/5的重铬酸钠溶液加入三颈烧瓶中,充分搅拌使之混合均匀。冷水浴冷却,控制反应温度在55~60℃。待橙红色消失后,再将剩余的重铬酸钠溶液分四次加入到三颈烧瓶中。当温度自动下降时,加入4mL甲醇使反应液完全变成墨绿色(三价铬);
3.蒸馏:在反应瓶中加入30mL水,并改为蒸馏装置,收集90~99℃之间的馏分(环己酮与水的共沸物)至无油珠为止;
4.萃取、干燥:将馏出液用食盐饱和后转入分液漏斗中,分出有机层。水层用8mL乙醚提取一次,将乙醚提取液和有机层合并,用无水硫酸镁干燥; 5.蒸馏,收集环己酮产品2.6g。 请回答下列问题:
(1)装置A的名称是___________。
(2)完成并配平反应方程式:

(3)反应过程中加入甲醇后有无色气体生成。加入甲醇的作用是___________,请用离子方程式表示反应原理___________。
(4)步骤4向馏出液加入食盐的目的是___________,将乙醚提取液和有机层合并的原因是___________。
(5)计算所得产品的产率___________。(保留三位有效数字)
-
环己酮是重要的化工原料,也是重要的工业溶剂。实验室制备环己酮的原理、有关数据及装置示意图如下:
反应原理:

反应放热,温度过高或者重铬酸钠过量会进一步氧化.
主要物料及产物的物理参数:
| 名称 | 溶解度 | 密度 | 熔点℃ | 沸点℃ | 溶解度 |
| 水 | 乙醚 |
| 环己醇 | 无色,有刺激性气味 | 0.9624 | 25.93 | 161.5 | 5.67g/100mL | 
|
| 环己酮 | 无色,有枣激性气味 | 0.9478 | —— | 155.7 | 2.4g/100mL | 
|
实验装置:
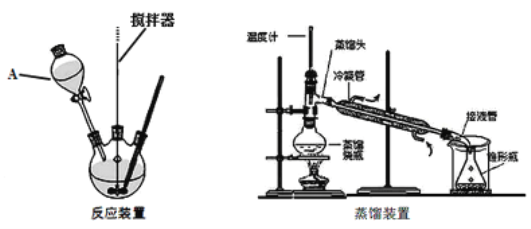
实验步骤:
①投料:在100mL三颈烧瓶中加入20mL水,慢慢加入5mL浓硫酸摇动,振荡下缓慢加入5mL(4.8g,0.048mol)环己醇,并将混合液温度降至30℃以下。将5g(0.019mol)重铬酸钠溶于水得橙红色溶液备用.
②反应:将约1/5的重铬酸钠溶液加入三颈烧瓶中,充分搅拌使之混合均匀。冷水浴冷却,控制反应温度在55-60℃。待橙红色消失后,再将剩余的重铬酸钠溶液分四次加入到三颈烧瓶中,当温度自动下降时,加入4mL甲醇使反应液完全变成墨绿色(三价铬);
③蒸馏:在反应瓶中加入30mL水,并改为蒸馏装置,收集90-99℃之间的馏分(环己酮与水的共沸物)至无油珠为止;
④萃取、干燥:将馏出液用食盐饱和后转入分液漏斗中,分出有机层。水层用8mL乙醚提取一次,将乙醚提取液和有机层合并,用无水硫酸镁干燥;5.蒸馏,收集环己酮产品2.6g。
请回答下列问题:
(1)装置A的名称是________.
(2)完成并配平反应方程式:
_____ +_____Na2Cr2O7+____H2SO4→____
+_____Na2Cr2O7+____H2SO4→____ +____Na2SO4+____Cr2(SO4)3+___H2O___________
+____Na2SO4+____Cr2(SO4)3+___H2O___________
(3)反应过程中加入甲醇后有无色气体生成。加入甲醇的作用是______,请用离子方程式表示反应原理________.
(4)步骤4向馏出液加入食盐的目的是_________,将乙醚提取液和有机层合并的原因是_________.
-
(14分)乙酸异戊酯( )是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图(有关的加热和夹持仪器略去)和有关数据如下:
)是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图(有关的加热和夹持仪器略去)和有关数据如下:
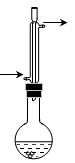
实验步骤:在烧瓶中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热烧瓶,回流50分钟,反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁晶体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
| 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 水中溶解性 |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |
(1)写出制取乙酸异戊酯的化学方程式 。
(2)冷凝管的作用是 ,碎瓷片的作用是 。
(3)若乙酸异戊酯产率偏低,其原因可能是 。
A.原料没有充分反应
B.发生了副反应
C.在进行蒸馏纯化操作时,从143 ℃开始收集馏分
(4)在洗涤、分液操作中,应充分振荡,然后静置,待分层后 (填标号),
A.直接将乙酸异戊酯从分液漏斗上口倒出
B.直接将乙酸异戊酯从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
D.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(5)实验中加入少量无水硫酸镁的目的是 。
(6)本实验的产率是
A.30℅ B.40℅ C.50℅ D.60℅
-
乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
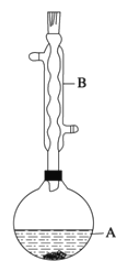
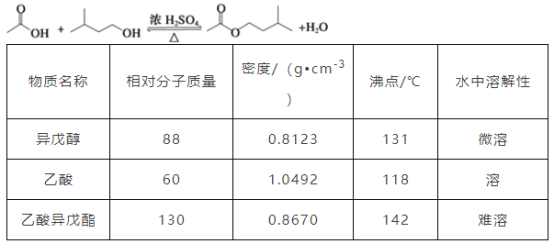
实验步骤: 在A中加入4.4 g异戊醇( ),6.0 g乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
),6.0 g乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。回答下列问题:
(1)仪器B的名称是_________________。
(2)如果加热一段时间后发现忘记加碎瓷片,应该采取的正确操作是________ (填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)在洗涤操作中,第一次水洗的主要目的是________,第二次水洗的主要目的是___________。
(4)分液漏斗在使用前须清洗干净并_______,在洗涤、分液操作中,应充分振荡,然后静置,待分层后_________________(填标号),
a.直接将乙酸异戊酯从分液漏斗上口倒出
b.直接将乙酸异戊酯从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(5)本实验中加入过量乙酸的目的是_________________。
(6)实验中加入少量无水MgSO4的目的是_____________。
(7)在蒸馏操作中,仪器选择及安装都正确的是_____________ (填标号) 。
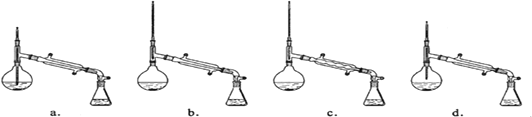
(8)本实验的产率是_____________
a. 30% b. 40% c. 50% d. 60%
(9)在进行蒸馏操作时,若从130 ℃开始收集馏分,会使实验的产率偏_____________ (填“高”或“低”),其原因是_____________。
-
乙酸异戊酯是组成蜜蜂信息素质的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图和有关数据如下:
 实验步骤:
实验步骤:
①在A中加入 4.4 g的异戊醇, 6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A 50分钟,②反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,③分出的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,④进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯 3.77 g。回答下列问题:
(1)异戊醇的系统命名法名称是:________________,
(2)装置B的作用:_____________,
(3)在步骤①中加入过量乙酸的目的是:_____________,
(4)在步骤②洗涤操作中,第一次水洗可以大量洗去的杂质有:___________,
(5)在洗涤、分液操作中,应充分振荡,然后静置,待分层后,先将______从分液漏斗的下口放出,再将______从上口放出,
(6)在步骤③中加入少量无水硫酸镁的目的是:_______________,
(7)本实验的产率是:______,
(8)在步骤④中,若从 130℃开始收集馏分,产率将偏_______(填高或者低)。
-
乙酸环己酯具有香蕉及苹果气味,主要用于配制各种饮料、冰淇淋等,实验室制备乙酸环己酯的反应装置示意图和有关数据如下:

实验步骤:
将12.0g(0.2mol)乙酸、10.0g(0.1mol)环已醇和15mL 环已烷加入装有温度计、恒压滴液漏斗和球形冷凝管的四颈烧瓶中,在搅拌下,慢慢滴加15mL98% 浓硫酸,恒 压滴液漏斗换成分水器装置,加热回流90min,将反应液依次加水、10%的NaHCO3 溶液、水洗涤,然后加无水MgSO4,放置过夜,加热蒸馏, 收集168~174℃的馏
压滴液漏斗换成分水器装置,加热回流90min,将反应液依次加水、10%的NaHCO3 溶液、水洗涤,然后加无水MgSO4,放置过夜,加热蒸馏, 收集168~174℃的馏 分,得到无色透明有香味的液体,得产品6.9g
分,得到无色透明有香味的液体,得产品6.9g

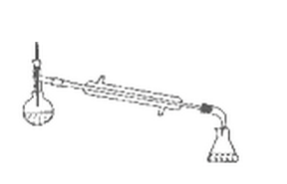
(1)上述反应装置图中存在的一处错误是___________。
(2)实验中控制乙酸的物质的量是环已醇的2 倍,其目的是___________。
(3)使用分水器(如图)的目的是___________ 。
(4)用10%的NaHCO3溶液目的是___________;第二次水洗 的目的是___________ ;加入无水MgSO4 的目的是 ___________。
;加入无水MgSO4 的目的是 ___________。
(5)本次实验产率为___________。
(6)若在进行蒸馏操作时,采用右图装置,会使实验的产率 (填“偏高”“ 偏低”“无影响”), 其原因是_________________。
-
乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
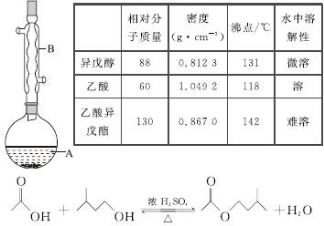
实验步骤:
在A中加入4.4 g异戊醇、6.0 g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50 min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。
回答下列问题:
(1)仪器B的名称是________________。
(2)在洗涤操作中,第一次水洗的主要目的是_______________,第二次水洗的主要目的是________________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是_______________________。
(5)实验中加入少量无水MgSO4的目的是________。
(6)在蒸馏操作中,仪器选择及安装都正确的是________(填标号)。
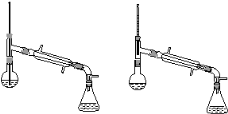
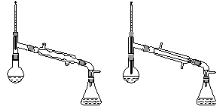
a. b. c. D.
(7)本实验的产率是________(填标号)。
a.30% b.40% c.60% d.90%
(8)在进行蒸馏操作时,若从130 ℃便开始收集馏分,会使实验的产率偏__________(填“高”或“低”),其原因是___________________。
-
乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
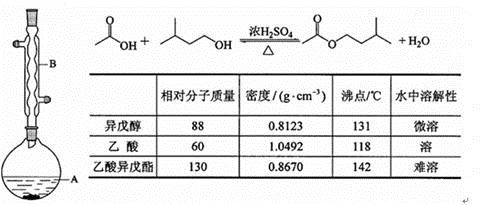
实验步骤:
在A中加入4.4 g的异戊醇、6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。
回答下列问题:
(1)仪器B的名称是______。
(2)在洗涤操作中,第一次水洗的主要目的是____________,第二次水洗的主要目的是___________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后______(填标号)。
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是________________。
(5)实验中加入少量无水MgSO4的目的是___________。
(6)在蒸馏操作中,仪器选择及安装都正确的是______(填标号)。

(7)本实验的产率是______(填标号)。
a.30℅ b.40℅ c.60℅ d.90℅
(8)在进行蒸馏操作时,若从130 ℃便开始收集馏分,会使实验的产率偏__(填“高”或“低”), 原因是_____________。




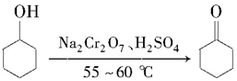









 实验步骤:
实验步骤:






