-
海水资源的利用具有非常广阔的前景。下列关于海水资源利用的说法中不正确的是( )
A. 电解法分解海水,制取洁净的热能资源氢气
B. 采用太阳光照射法晒制工业用食盐
C. 针对能量现状,大力开发潮汐能和波浪能
D. 铀是海水中的微量元素,但核工业的铀主要从海水中提取
高一化学选择题中等难度题查看答案及解析
-
地球上的资源是有限的,要合理地开发和利用.
(1)海水化学资源的利用具有非常广阔的前景.
①下列有关海水综合利用的说法中,正确的是______(填选项序号).
a.海水中含有钾元素,只需经过物理变化就可以得到金属钾
b.用蒸馏、电渗析、离子交换等方法能从海水中提取淡水
c.从海水中可以得到氯化钠,电解熔融氯化钠可制金属钠
d.利用潮汐发电是将化学能转化为电能
②从海水中提取溴单质,其中一步工艺是在预先酸化的浓缩海水中,通入足量的氯气将溴离子氧化,该反应的离子方程式是______.
③海水中含有大量镁元素,可以通过多步转化得到氯化镁,用无水氯化镁冶炼金属镁的化学方程式是______ Mg+Cl2↑高一化学解答题中等难度题查看答案及解析
-
海洋约占地球表面积的71%,是一个远未完全开发的巨大化学资源宝库,海水水资源的利用和海水化学资源的利用具有非常广阔的前景.回答下列问题:
(1)海水淡化处理多用蒸馏法.如图是海水蒸馏原理示意图.蒸馏法的特点是设备结构、操作简单,淡水质量好,但也具有明显的缺陷.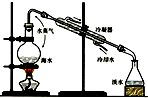
1你认为蒸馏法进行海水淡化的主要缺陷是________;
②我省某沿海地区拟采用蒸馏法兴建一座大型海水淡化工厂,为克服蒸馏法海水淡化的缺陷,请你为该地区提出一条合理化建议________;
(2)海水淡化后得到的淡水应进行技术处理后才能得到完全满足生产、生活要求的水,使用离子交换树脂与水中的离子进行交换是常用的水处理技术.聚丙烯酸钠是一种离子交换树脂,已知丙烯酸钠的化学式为CH2=CH-COONa试写出生成聚丙烯酸钠的化学方程:________;
(3)从海水中可以获取食盐、镁、钾、溴及其化工产品.空气吹出法是目前从海水中提取溴的常用方法,具体流程如下: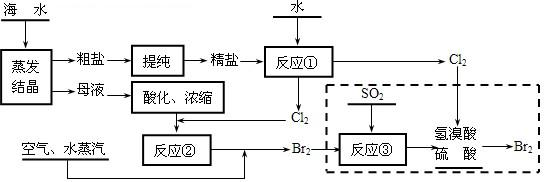
①实验室中粗盐提纯的步骤是________;在反应②中得到的溶液中通入空气、水蒸汽的作用是________;
②反应的离子方程式分别为________;
③在反应中消耗标况下896m3SO2时,共转移________ mol电子;
(4)上述流程中虚线方框内生产流程的作用是________.高一化学填空题中等难度题查看答案及解析
-
漳州市海水资源丰富,漳浦盐场是福建省第三大国有盐场,盐田面积达700万平方米,每年产盐5万多吨。海水化学资源(主要为NaCl和MgSO4及K、Br等元素)的利用具有非常广阔的前景。
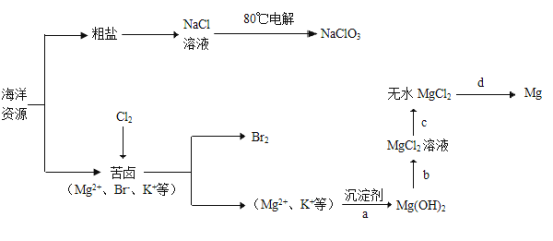
回答下列问题:
⑴NaClO3中氯的化合价_____________。
⑵在a、b、c、d提取镁的过程中,没有涉及的化学反应类型是_________(填序号)。
①分解反应 ②化合反应 ③复分解反应 ④置换反应
⑶苦卤中通入氯气发生的主要离子反应方程式为___________________________________。⑷步骤a中的沉淀剂是____________________。
⑸步骤d中,电解熔融MgCl2得到的镁需要在保护气中冷却,下列气体可以作为保护气的是____________(填序号)。
①N2 ②H2 ③CO2 ④空气
⑹假设该海域海水中MgCl2浓度9.5×10-3g·L-1 ,欲获得24g金属镁需要________L海水。
高一化学实验题中等难度题查看答案及解析
-
海水是巨大的资源宝库,海水资源的利用和海水化学资源的利用具有非常广阔的前景。从海水中提取食盐和溴的过程如下:
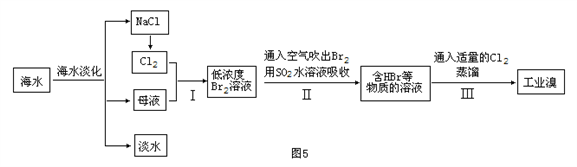
(1)请列举海水淡化的两种方法:____、____。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为_______。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_______。
(4)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如下装置简图。
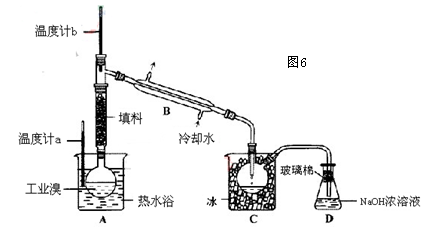
请你参与分析讨论:
①图中仪器B的名称:___。
②实验装置中使用热水浴的原因是_________________。
③C中液体产生颜色为____。为除其物中仍残留的少量Cl2,可向其中加入NaBr溶液,反应的化学方程式为_________________________充分反应后,再进行的分离操作是___。
高一化学填空题中等难度题查看答案及解析
-
(8分)海水水资源的利用和海水化学资源的开发利用具有非常广阔的前景。
(1)列举海水淡化的两种方法:________、 。
(2)采用“空气吹出法”从浓海水吹出Br2,用SO2吸收,则发生反应的离子方程式为 。还可以用纯碱吸收,主要反应是Br2+Na2CO3+H2O → NaBr+NaBrO3+NaHCO3,当吸收1 mol Br2时,转移电子的物质的量为________mol。
(3)按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
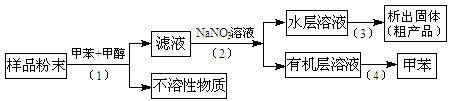
下列说法正确的是________。
A.步骤(1)需要过滤装置 B.步骤(2)需要用到分液漏斗
C.步骤(3)需要用到坩埚 D.步骤(4)需要蒸馏装置
高一化学填空题困难题查看答案及解析
-
海水水资源的利用和海水化学资源的开发利用具有非常广阔的前景。
(1)列举海水淡化的两种方法:______________、______________。
(2)采用“空气吹出法”从浓海水吹出Br2,用SO2吸收,则发生反应的离子方程式为:____。
还可以用纯碱吸收,主要反应是Br2+Na2CO3+H2O → NaBr+NaBrO3+NaHCO3,当吸收1 mol Br2时,转移电子的物质的量为________mol。
(3)按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
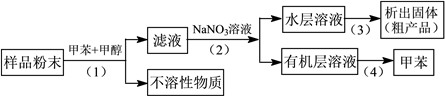
下列说法正确的是________。
A.步骤(1)需要过滤装置 B.步骤(2)需要用到分液漏斗
C.步骤(3)需要用到坩埚 D.步骤(4)需要蒸馏装置
高一化学简答题困难题查看答案及解析
-
(11分)海水中化学资源的利用具有非常广阔的前景。
(1)目前世界上60%的镁是从海水中提取的,其主要步骤如下:
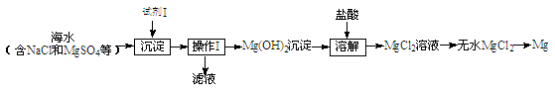
①试剂Ⅰ适宜选用 (填序号)。
A.盐酸 B.石灰乳 C.氯化钠溶液
②操作Ⅰ的名称是 。
③工业上通过电解熔融的MgCl2制备金属Mg,该反应的化学方程式是 。
(2)下图是某课外小组在实验室模拟从海水中提取溴的实验装置。
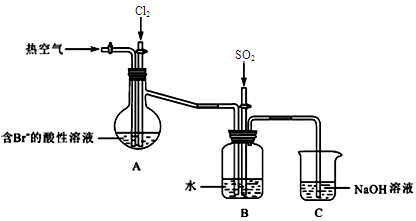
A装置中通入Cl2一段时间后,改通热空气,将Br2吹出至B装置。
①A装置中发生反应生成Br2的离子方程式为 。
② B装置中,Br2被SO2还原,B装置中产生的两种主要阴离子的符号为 、 。
③C装置中NaOH溶液的作用是 。
高一化学填空题困难题查看答案及解析
-
海洋约占地球表面积的71%,海水资源的利用具有非常广阔的前景,从海水中可提取多种化工原料。按下图所示工艺流程可利用海水获得Br2:
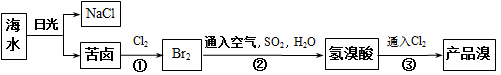
(1)请列举海水淡化的两种方法:________、________
(2)下列不需要化学变化就能够从海水中获得的物质是 。
A.氯、溴、碘 B.食盐、淡水 C.烧碱、氢气 D.钠、镁、铝
(3)步骤 ① 中已获得Br2,步骤②中又将Br2还原为Br-,其目的为_________________。
(4)步骤②用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为________,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是______________。
(5)某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO的浓度之比为1︰3,则溶液中c(Na+)︰c(ClO-)=___________。
高一化学填空题困难题查看答案及解析
-
我国拥有较丰富的地热资源,其开发利用前景广阔。下列关于地热能说法正确的是 ( )
①可以用于洗浴、发电以及供暖等方面
②与煤炭、石油、天然气一样都是化石能源
③主要源于地球内部放射性元素衰变产生的能量
④与地下水结合可形成热水型地热,释放形式之一是温泉
A. ①②③ B. ①②④
C. ①③④ D. ②③④
高一化学单选题中等难度题查看答案及解析