-
碳是构成地球生命的一种重要非金属元素,碳单质很早就被人认识和利用,碳的一系列化合物——有机物,更是生命的根本,下列有关说法正确的是
A. 含碳的化合物数量众多,分布极广
B. 向空气中大量排放二氧化碳气体会形成酸雨,破坏建筑物
C. 碳单质有多种不同的存在形式,如金刚石、12C、14C、C60等
D. 煤、石油属于不可再生资源,天然气、乙醇属于可再生资源
高三化学选择题中等难度题查看答案及解析
-
碳是地球上组成生命的最基本元素之一,与其他元素结合成不计其数的无机物和有机化合物,构成了丰富多彩的世界。碳及其化合物在研究和生产中有许多重要用途。回答下列问题:
(1)冠醚是由多个二元醇分子之间失水形成的环状化合物。X、Y、Z是常见的三种冠醚,其结构如图所示。它们能与碱金属离子作用,并且随着环的大小不同而与不同金属离子作用。
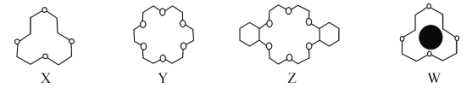
①Li+与X的空腔大小相近,恰好能进入到X的环内,且与氧原子的一对孤电子对作用形成稳定结构W(如图)。基态碳原子核外有___种运动状态不同的电子,其外围电子轨道表示式为___。W中Li+与孤对电子之间的作用属于___(填标号)。
A.离子键 B.共价键 C.氢键 D.配位键 E.以上都不是
②冠醚Y能与K+形成稳定结构,但不能与Li+形成稳定结构,理由是___。
③冠醚分子中氧的杂化轨道的空间构型是___,C—O—C的键角___(填“>”“<”或“=”)109°28′。
(2)碳的一种同素异形体——石墨,其晶体结构及晶胞如图1、图2所示。则石墨晶胞含碳原子个数为___个。已知石墨的密度为ρg·cm-3,C—C键键长为rcm,阿伏加德罗常数的值为NA,计算石墨晶体的层间距d为___cm。
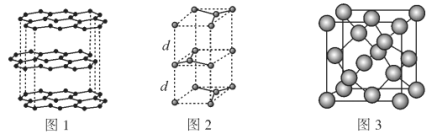
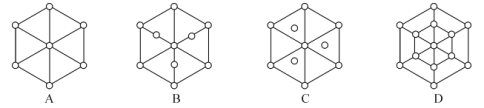
(3)碳的另一种同素异形体——金刚石,其晶胞如图3所示。已知金属钠的晶胞(体心立方堆积)沿其体对角线垂直在纸平面上的投影图如图A所示,则金刚石晶胞沿其体对角线垂直在纸平面上的投影图应该是图___ (从A~D图中选填)。
高三化学综合题困难题查看答案及解析
-
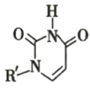
下图表示有关物质(均是中学化学常见的物质)之间的转化关系(其中部分参加反应的水和生成的水未列出),其中B、C为金属单质,E为非金属单质,其余均为化合物,Y、Z的组成元素相同,D为淡黄色的固体。回答系列问题: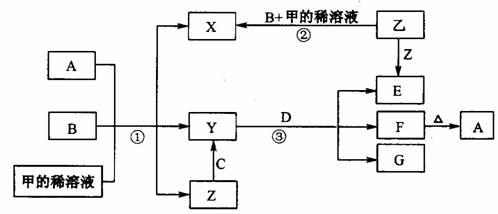
(1)B与甲稀溶液不反应,但与甲的浓溶液在加热条件下能反应。则甲为________,C为________(填写化学式)。
A与B物质的量应满足的关系为。
(2)写出反应③的化学方程式________。
(3)反应②观察到溶液由无色变成蓝色,并且有无色气泡产生。请写出反应②发生的化学反应方程式________,并分析产生气体的原因________。
高三化学填空题中等难度题查看答案及解析
-
选做(12分)【化学——物质结构与性质】第二周期中碳、氮、氧是构成生命物质的三种主要元素,其单质及化合物在生产生活中也有着重要的应用。
(1)第二周期中,元素的第一电离能处于B与N之间的元素有_________种。
(2)某元素位于第四周期VIII族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为_________________________。
(3)乙烯酮(CH2=C=O)是一种重要的有机中间体,可用CH3COOH在痕量(C2H5O)P=O存在下加热脱H2O得到。乙烯酮分子中碳原子杂化轨道类型是________。CH3COOH的沸点比HCOOCH3高的主要原因是_______________________。
(4)CH2=CHCN是制备晴纶的原料,其分子中
键和
键的个数之比为______(填最简整数比)。
(5)碳化硅的结构与金刚石类似,其硬度仅次于金刚石,具有较强的耐磨性能。每个碳原子周围与其距离最近的硅原子有________个。
高三化学填空题困难题查看答案及解析
-
碳是构成地球生命的重要元素。下列说法正确的是
A. 自然界中不存在游离态的碳
B. 碳的化合物数量众多,分布极广
C. 向空气中排放二氧化碳会形成酸雨
D. 煤、石油、天然气属于可再生碳资源
高三化学选择题中等难度题查看答案及解析
-
碳是地球上组成生命的最基本元素之一,可以sp3 、sp2和sp杂化轨道成共价键,具有很强的结合能力,与其它元素结合成不计其数的无机物和有机化合物,构成了丰富多彩的世界。碳及其化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)基态碳原子核外有__________种空间运动状态的电子,其价电子排布图为 。
(2)光气的分子式为COCl2,又称碳酰氯,是一种重要的含碳化合物,判断其分子立体构型为 ,其碳原子杂化轨道类型为 杂化。
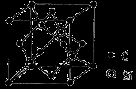
(3)碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,如下表所示:
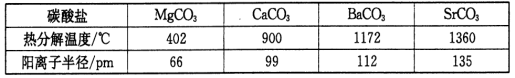
试解释为什么随着阳离子半径的增大,碳酸盐的分解温度逐步升高?
(4)碳的一种同素异形体——C60,又名足球烯,是一种高度对称的球碳分子。立方烷(分子式:C8H8,结构是立方体:
)是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为
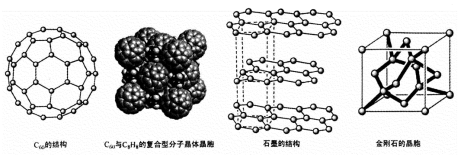
(5)碳的另一种同素异形体——石墨,其晶体结构如上图所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为 个。已知石墨的密度为ρg.cm-3 ,C-C键长为rcm,阿伏伽德罗常数的值为NA,计算石墨晶体的层间距为 cm。
高三化学简答题极难题查看答案及解析
-
碳是地球上组成生命的最基本元素之一,可以sp3 、sp2和sp杂化轨道成共价键,具有很强的结合能力,与其它元素结合成不计其数的无机物和有机化合物,构成了丰富多彩的世界。碳及其化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)基态碳原子核外有__________种空间运动状态的电子,其价电子排布图为 。
(2)光气的分子式为COCl2,又称碳酰氯,是一种重要的含碳化合物,判断其分子立体构型为 ,其碳原子杂化轨道类型为 杂化。
(3)碳酸盐在一定温度下会发生分解,实验证明碳酸盐的阳离子不同,分解温度不同,如下表所示:
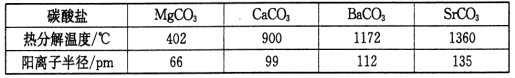
试解释为什么随着阳离子半径的增大,碳酸盐的分解温度逐步升高?
(4)碳的一种同素异形体——C60,又名足球烯,是一种高度对称的球碳分子。立方烷(分子式:C8H8,结构是立方体:
)是比C60约早20年合成出的一种对称型烃类分子,而现如今已合成出一种立方烷与C60的复合型分子晶体,该晶体的晶胞结构如下图所示,立方烷分子填充在原C60晶体的分子间空隙中。则该复合型分子晶体的组成用二者的分子式可表示为

(5)碳的另一种同素异形体——石墨,其晶体结构如上图所示,虚线勾勒出的是其晶胞。则石墨晶胞含碳原子个数为 个。已知石墨的密度为ρg.cm-3 ,C-C键长为rcm,阿伏伽德罗常数的值为NA,计算石墨晶体的层间距为 cm。
高三化学简答题极难题查看答案及解析
-
(1)卤族元素组成的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识它们。

①如图1为碘晶体的晶胞结构。有关说法正确的是_________(填序号)。
a.平均每个晶胞中有4个碘分子
b.平均每个晶胞中有4个碘原子
c.碘晶体为无限延伸的空间结构,是原子晶体
d.碘晶体中存在的相互作用有非极性键和范德华力
②已知CaF2晶胞(图2)的密度为ρ g/cm3,NA表示阿伏加德罗常数的值,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的摩尔质量可表示为_________________。
(2)以MgCl2为原料用电解熔融盐法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外,还有_______________。
(3)有研究表明,化合物X可用于研究模拟酶,当结合
 或Cu(I)(I表示化合价为+1)时,分别形成如下图所示的A和B:
或Cu(I)(I表示化合价为+1)时,分别形成如下图所示的A和B:
①A中连接相邻含N杂环的碳碳键可以旋转,说明该碳碳键具有_________键的特性。
②微粒间的相互作用包括化学键和分子间相互作用,比较A和B中微粒间相互作用力的差异:________________。
高三化学综合题中等难度题查看答案及解析
-
如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).
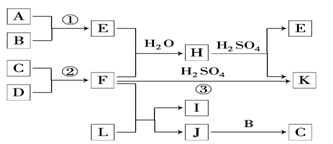
已知:
(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.
(b)反应①、②是化工生产中的重要反应.
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.
(e)化合物J由两种元素组成,其相对分子质量为32.
请按要求填空:
(1)反应③的化学方程式_____________________.
(2)C的结构式__________________________;
H为正盐,则H的化学式为____________________.
(3)L的溶液与化合物E反应的离子方程式: ______________.
(4)化合物J的化学式____________________.
高三化学选择题中等难度题查看答案及解析
-
如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).已知:
(a)A、B、C、D都是非金属单质,其中B、C、D在常温常压下是气体.
(b)反应①、②是化工生产中的重要反应.
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.
(e)化合物J由两种元素组成,它是火箭推进剂的成分之一,其相对分子质量为32.
请按要求填空:
(1)反应③的化学方程式______.
(2)C的结构式______;H的化学式______.
(3)L的溶液与化合物E反应的离子方程式:______.
(4)化合物J的化学式______.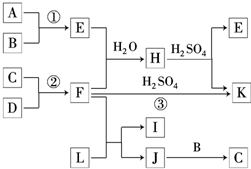
高三化学解答题中等难度题查看答案及解析