-
磷的单质和化合物都是重要的化工产品。查阅资料可知:亚磷酸(H3PO3)、次磷酸(H3PO2)以及它们的盐都有较强的还原性,可用于化学镀银或镀镍。亚磷酸是中强酸,它与足量的NaOH溶液反应生成 Na2HPO3。试回答下列问题:
(1)Na2HPO3中P的化合价为____。
(2)Na2HPO3是____(填“正盐”或“酸式盐”),其溶液的pH____(填“>”、“=”或“<”)7。
(3)次磷酸钠(NaH2PO2)可用于化学镀镍。镀镍溶液中含Ni2+和H2PO2-,在酸性条件下发生下述反应: Ni2++ H2PO2-+ = Ni+ H2PO3-+_____。
①请配平化学方程式___。
②依据化学方程式,反应消耗6 mol H2PO2-时,转移电子数为_____。
高二化学综合题中等难度题查看答案及解析
-
化学反应原理对于研究化学物质有十分重要的意义。
(1)已知次磷酸(H3PO2,一元中强酸)和亚磷酸(H3PO3,结构式为
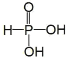 ,二元中强酸)均是重要的精细化工产品。
,二元中强酸)均是重要的精细化工产品。①写出次磷酸的结构式:_____________________________________。
②已知某温度下0.01 mol·L-1的NaOH溶液pH=10,将该NaOH溶液与等浓度等体积的次磷酸溶液混合,混合后溶液pH=7,则此时c(OH-)—c(H3PO2)=___________。(用具体数值表示)
(2)实验室配制FeCl3溶液时,需要将FeCl3固体溶解在较浓的盐酸中,其原因是_______________________________________________________(用离子方程式和必要的文字说明)。
已知25℃时,Fe(OH)3的Ksp=4.0×10-38,配制100ml 5 mol·L-1的FeCl3溶液,至少需要加入_______mL 2 mol·L-1的盐酸(忽略加入盐酸的体积)。
(3)工业废水中的Cr2O72-对生态系统有很大损害。常用的处理方法有两种。
①还原沉淀法:Cr2O72-
Cr3+
Cr(OH)3。常温下,要使Cr3+沉淀完全,溶液的pH应调至________。(已知Cr(OH)3的Ksp=10-32)
②电解法:用铁和石墨做电极,电解产生的还原剂将Cr2O72-还原成Cr3+,最终产生Cr(OH)3沉淀。若有1mol Cr2O72-被还原,理论上导线中通过___________mol电子。
高二化学综合题中等难度题查看答案及解析
-
次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。下列有关说法正确的是
A.用惰性电极电解NaH2PO2溶液,其阳极反应式为:2H2O-4e-=O2↑+4H+
B.H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-=PO23-+3H2O
C.将H3PO2溶液加入到酸性重铬酸钾溶液中,H3PO2的还原产物可能为H3PO4
D.H3PO2溶于水的电离方程式为H3PO2
H++H2PO2-
高二化学单选题中等难度题查看答案及解析
-
次磷酸(H3PO2)是一种精细磷化工产品,属于一元弱酸,具有较强的还原性。下列有关说法正确的是
A.H3PO2溶于水的电离方程式为:H3PO2
3H++PO23-
B.H3PO2与过量NaOH溶液反应的离子方程式为:H3PO2+3OH-=PO23-+3H2O
C.将H3PO2溶液加入到酸性高锰酸钾溶液中,H3PO2的氧化产物为H3PO4
D.用惰性电极电解NaH2PO2溶液,其阳极反应式为:H2PO2-4e-+2H2O =O2↑+4H+
高二化学选择题中等难度题查看答案及解析
-
铜、磷及其化合物在生产、生活中有重要的用途,回答下列问题:
(1)磷的一种化合物叫亚磷酸(H3PO3)。已知:
Ⅰ、0.1mol/L H3PO3溶液的pH=1.7;
Ⅱ、H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ、H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成.
①关于H3PO3的说法:a强酸;b弱酸;c二元酸;d三元酸;e氧化性酸;f还原性酸,其中正确的是__________
A.bdf B.bcf C.ade D.bce,
②写出H3PO3与少量NaOH溶液反应的离子方程式__________;
③Na2HPO3为__________(填“正盐”或“酸式盐”)
(2)碘化亚铜可作催化剂,饲料添加剂等,是难溶于水的固体.铜可以与氢碘酸发生置换反应得到氢气,试从离子浓度对离子反应方向影响的角度解释此反应能够发生的原因__________,CuSO4溶液也能使淀粉-KI试纸变蓝,用离子方程式说明其原理__________;
(3)纳米氧化亚铜是一种具有良好光电效应的材料,工业上制备它的方法之一是:先向KOH溶液中加入一定量的CuSO4溶液,再加入一定量的肼(N2H4),加热并保持反应体系的温度在90℃,反应完全后,分离、洗涤、真空干燥所得到的固体样品。检验反应混合体系内纳米Cu2O已经生成的实验方法的名称是__________。
高二化学填空题困难题查看答案及解析
-
由短周期元素组成的化合物X是某抗酸药的有效成分。某同学欲探究X的组成。
查阅资料:①由短周期元素组成的抗酸药的有效成分有碳酸氢钠、碳酸镁、氢氧化铝、硅酸镁铝、磷酸铝、碱式碳酸镁铝。
②Al3+在pH=5.0时沉淀完全;Mg2+在pH=8.8时开始沉淀,在pH=11.4时沉淀完全。
实验过程:
Ⅰ.向化合物X粉末中加入过量盐酸,产生气体A,得到无色溶液。
Ⅱ.用铂丝蘸取少量Ⅰ中所得的溶液,在火焰上灼烧,无黄色火焰。
Ⅲ.向Ⅰ中所得的溶液中滴加氨水,调节pH至5~6,产生白色沉淀B,过滤。
Ⅳ.向沉淀B中加过量NaOH溶液,沉淀全部溶解。
Ⅴ.向Ⅲ中得到的滤液中滴加NaOH溶液,调节pH至12,得到白色沉淀C。
(1)Ⅰ中气体A可使澄清石灰水变浑浊,A的化学式是________。
(2)由Ⅰ、Ⅱ判断X一定不含有的元素是磷、________。
(3)Ⅲ中生成B的离子方程式是__________________________________________________。
(4)Ⅳ中B溶解的离子方程式是__________________________________________________。
(5)沉淀C的化学式是________。
(6)若上述n(A)∶n(B)∶n(C)=1∶1∶3,则X的化学式是__________________________。
高二化学综合题中等难度题查看答案及解析
-
关于氮族元素(从N到Bi)单质及其化合物的性质递变规律说法正确的是( )
A.单质的熔、沸点依次增大 B.单质磷的化学活泼性比氮气强
C.气态氢化物的还原性依次减弱 D.磷酸的酸性比硝酸强
高二化学选择题简单题查看答案及解析
-
已知吡啶(
)与苯环性质相似。有机物M与磷酸在一定条件下形成磷酸吡醛,
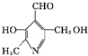 (M)+H3PO4
(M)+H3PO4H2O+
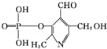 (磷酸吡醛),磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )
(磷酸吡醛),磷酸吡醛是细胞的重要组成部分.下列说法不正确的是( )A.M能使酸性高锰酸钾溶液褪色
B.1 mol M能与金属钠反应,消耗2 mol Na
C.1 mol磷酸吡醛与NaOH溶液反应,最多消耗3 mol NaOH
D.M与足量H2反应后所得有机物的分子式为C8H17O3N
高二化学选择题困难题查看答案及解析
-
磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
(1)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
①2Ca3(PO4)2(s)+10C(s)
6CaO(s)+P4(s)+10CO(g)ΔH1=+3 359.26 kJ·mol-1
②CaO(s)+SiO2(s)
CaSiO3(s) ΔH2=-89.61 kJ·mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)
6CaSiO3(s)+P4(s)+10CO(g)ΔH3则ΔH3= kJ·mol-1。
(2)白磷中毒后可用CuSO4溶液解毒,解毒原理可用下列化学方程式表示: 11P4+60CuSO4 +96H2O
20Cu3P +24H3PO4+60H2SO4 6 mol CuSO4能氧化白磷的物质的量是 。
(3)磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH的关系如图所示。

①为获得尽可能纯的NaH2PO4,pH应控制在 ; pH=8时,溶液中主要含磷物种浓度大小关系为 。
②Na2HPO4溶液显碱性,若向溶液中加入足量的CaCl2溶液,溶液则显酸性,其原因是 (写离子方程式)。
(4)磷的化合物三氯氧磷(
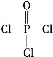 )与季戊四醇(
)与季戊四醇(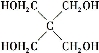 )以物质的量之比2∶1反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X的核磁共振氢谱如下图所示。
)以物质的量之比2∶1反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X的核磁共振氢谱如下图所示。
①酸性气体是 (填化学式)
②X的结构简式为 。
高二化学填空题极难题查看答案及解析
-
(1)磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)═6CaO(s)+P4(s)+10CO(g)△H1=+3359.26 kJ•mol﹣1
CaO(s)+SiO2(s)═CaSiO3(s)△H2=﹣89.61 kJ•mol﹣1
写出白磷(P4)由Ca3(PO4)2、焦炭和SiO2在一定条件下反应的热化学方程式为:_____。
(2)电子工业中清洗硅片上的SiO2(s)的反应为SiO2(s)+4HF(g)═SiF4(g)+2H2O(g)△H(298.15 K)=﹣94.0 kJ•mol﹣1△S(298.15 K)=﹣75.8 J•mol﹣1•K﹣1,设△H和△S不随温度而变化,此反应自发进行的温度是_____
高二化学计算题中等难度题查看答案及解析