-
化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分【解析】
2Mg5Al3(OH)19(H2O)4=27H2O+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据__、__;
(2)用离子方程式表示除去固体产物中Al2O3的原理__。
-
Ⅰ.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分【解析】
2Mg5Al3(OH)19(H2O)4 27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据____________。
(2)用离子方程式表示除去固体产物中Al2O3的原理________。
(3)已知MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理_______。
Ⅱ.磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
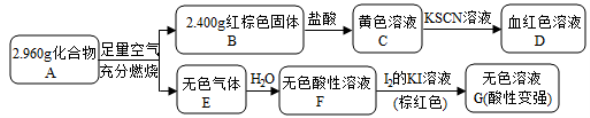
请回答:
(1)A的组成元素为_________(用元素符号表示),化学式为______。
(2)溶液C可溶解铜片,例举该反应的一个实际应用____________。
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g·L−1),该气体分子的电子式为____。写出该反应的离子方程式__________。
(4)写出F→G反应的化学方程式_____________。设计实验方案探究溶液G中的主要微粒(不考虑H2O、H+、K+、I−)______________。
-
Ⅰ.化合物 Mg5Al3(OH)19(H2O)4 可作环保型阻燃材料,受热时按如下化学方程式分【解析】
2Mg5Al3(OH)19(H2O)4 27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据___________。
(2)用离子方程式表示除去固体产物中 Al2O3 的原理___________
(3)已知 MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理_____________。
Ⅱ.磁性材料 A(M=296g/mol)是由两种元素组成的化合物,某研究小组按如图流程探 究其组成:
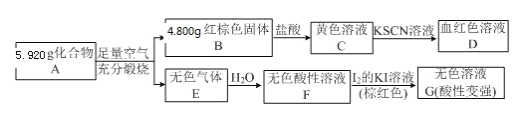
请回答:
(4)A的化学式为_____。C 中呈黄色的离子对应元素在元素周期表中的位置为__________。
(5)已知化合物 A 能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下,该气体对氨气的相对密度为2),该气体分子的电子式为_____。写出该反应的离子方程式_________。
(6)写出F→G反应的化学方程式____________。
-
Ⅰ.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分【解析】
2Mg5Al3(OH)19(H2O)4  27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据____________。
(2)用离子方程式表示除去固体产物中Al2O3 的原理________。
(3)已知MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理____________。
Ⅱ.磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
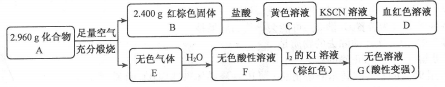
请回答:
(1)A的组成元素为_________(用元素符号表示),化学式为______。
(2)溶液C可溶解铜片,例举该反应的一个实际应用____________。
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g·L-1),该气体分子的电子式为____。写出该反应的离子方程式__________。
(4)写出F→G反应的化学方程式_____________。设计实验方案探究溶液G中的主要微粒(不考虑H2O、H+、K+、I-)______________。
-
I.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分【解析】
2Mg5Al3(OH)19(H2O)4 27H2O↑+10MgO+3A12O3
27H2O↑+10MgO+3A12O3
(1)写出该化合物作阻燃剂的两条依据____________________________________。
(2)用离子方程式表示除去固体产物中A12O3的原理________________________。
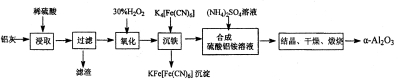
II.以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为A12O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:
(1)用图中“滤渣”和NaOH 焙烧制备硅酸钠,可采用的装置为_______(填选项编号)。
焙烧制备硅酸钠,可采用的装置为_______(填选项编号)。
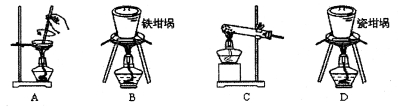
(2)验证“沉铁”后,溶液中是否还含有铁离子的操作方法为____________________。
(3)若用调节溶液的pH“沉铁”,则得到Fe(OH)3,己知:
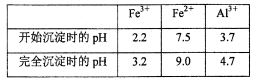
为保证产品的纯度,最好选用下列物质中的_______调节pH(填字母), 调节pH的范围为_____。
调节pH的范围为_____。
a.A12O3
B.H2SO4
C.NaOH
D.Na2CO3
(4)煅烧硫酸铝铵晶体,发生的主要反应为:
4[NH4Al(SO4)2·12H2O] 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,
将产生的气体通过下图所示的装置。
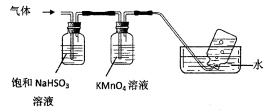
①集气瓶中收集到的气体是_____________________(填化学式)。
②KMnO4溶液褪色,发生的离子反应方程式为_________________________________。
-
Ⅰ.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分【解析】
2Mg5Al3(OH)19(H2O)4 27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据____________。
(2)用离子方程式表示除去固体产物中Al2O3的原理________。
(3)已知MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理____________。
Ⅱ.磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
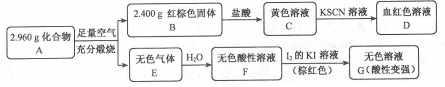
请回答:
(1)A的组成元素为_________(用元素符号表示),化学式为______。
(2)溶液C可溶解铜片,例举该反应的一个实际应用____________。
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g·L-1),该气体分子的电子式为____。写出该反应的离子方程式__________。
(4)写出F→G反应的化学方程式_____________。设计实验方案探究溶液G中的主要微粒(不考虑H2O、H+、K+、I-)______________。
-
Ⅰ.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分【解析】
2Mg5Al3(OH)19(H2O)4  27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
(1)写出该化合物作阻燃剂的两条依据________________。
(2)用离子方程式表示除去固体产物中Al2O3 的原理__________________。
(3)已知MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理________________。
Ⅱ.磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
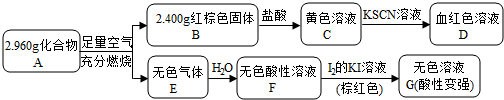
请回答:
(1)A的组成元素为_____________(用元素符号表示),化学式为__________。
(2)溶液C可溶解铜片,例举该反应的一个实际应用________________。
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g·L-1),该气体分子的电子式为________。写出该反应的离子方程式______________。
(4)写出F→G反应的化学方程式_____________。设计实验方案探究溶液G中的主要微粒(不考虑H2O、H+、K+、I-)______________。
-
Ⅰ.化合物Mg5Al3(OH)19(H2O)4可做环保型阻燃材料,受热时按如下化学方程式分【解析】
2Mg5Al3(OH)19(H2O)4  27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
Ⅱ.磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
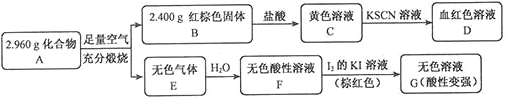
(1)A的组成元素为_________(用元素符号表示),化学式为______。
(2)溶液C可溶解铜片,列举该反应的一个实际应用____________。
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g·L-1),该气体分子的电子式为____。写出该反应的离子方程式__________。
(4)写出F→G反应的化学方程式_____________。设计实验方案探究溶液G中的主要微粒(不考虑H2O、H+、K+、I-)______________。
-
Ⅰ.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分解:2Mg5Al3(OH)19(H2O)4 27H2O↑+10MgO+3Al2O3。
27H2O↑+10MgO+3Al2O3。
(1)用离子方程式表示除去固体产物中Al2O3的原理______________________________。
(2)已知MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理__________________。
Ⅱ.NaH和NaAlH4都是重要的还原剂,一定条件下金属钠和H2反应生成NaH。NaH与水反应可生成H2,NaH与AlCl3反应可得到NaAlH4,请推测并回答:
(1)NaH与AlCl3反应得到NaAlH4的化学方程式___________________________________。
(2)NaAlH4与水发生氧化还原反应的化学方程式__________________________________。
(3)NaH在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程中生成两种产物,其反应的化学方程式为_____。
-
化合物Mg5Al3(OH)x(H2O)4可作环保型阻燃材料,受热时会发生如下分解反应(其中M是某种物质,a为化学计量数):2Mg5Al3(OH)x(H2O)4 27H2O↑+10M+aAl2O3下列说法正确的是
27H2O↑+10M+aAl2O3下列说法正确的是
A.a=2
B.x=18
C.M的化学式为MgO
D.该反应中Mg5Al3(OH)x(H2O)4既是氧化剂又是还原剂
27H2O↑+10MgO+3Al2O3









