某小组同学在实验室以下图所示的仪器和药品,进行氯气和铜粉反应的实验(部分夹持装置已省略).请按要求回答下列问题:
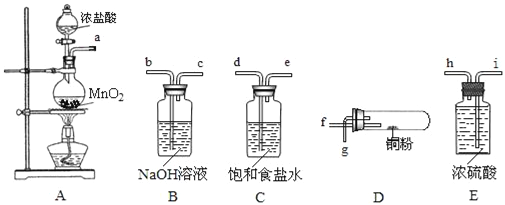
(1)装置A烧瓶中发生反应的化学方程式为_____.
(2)按气流方向连接各仪器接口的顺序是(填接口字母):
a→_________________________________________.
(3)装置C中饱和食盐水的作用是_____.
(4)装置B中发生反应的离子方程式为_____.
(5)加热装置D时,铜粉发生反应的化学方程式为_____.
高一化学实验题中等难度题
某小组同学在实验室以下图所示的仪器和药品,进行氯气和铜粉反应的实验(部分夹持装置已省略).请按要求回答下列问题:

(1)装置A烧瓶中发生反应的化学方程式为_____.
(2)按气流方向连接各仪器接口的顺序是(填接口字母):
a→_________________________________________.
(3)装置C中饱和食盐水的作用是_____.
(4)装置B中发生反应的离子方程式为_____.
(5)加热装置D时,铜粉发生反应的化学方程式为_____.
高一化学实验题中等难度题
某小组同学在实验室以下图所示的仪器和药品,进行氯气和铜粉反应的实验(部分夹持装置已省略).请按要求回答下列问题:

(1)装置A烧瓶中发生反应的化学方程式为_____.
(2)按气流方向连接各仪器接口的顺序是(填接口字母):
a→_________________________________________.
(3)装置C中饱和食盐水的作用是_____.
(4)装置B中发生反应的离子方程式为_____.
(5)加热装置D时,铜粉发生反应的化学方程式为_____.
高一化学实验题中等难度题查看答案及解析
某同学在实验室以下图所示的仪器和药品,进行氯气和铜粉反应的实验(部分夹持装置已省略)。请按要求回答下列问题:
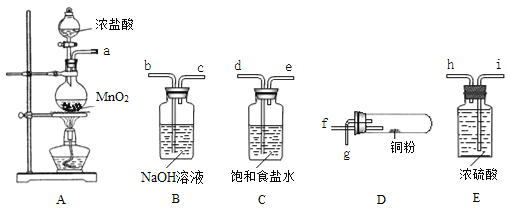
(1)装置A烧瓶中发生反应的化学方程式为_____________________________________。
(2)按气流方向连接各仪器接口的顺序是(填接口字母):
a→______________________。
(3)装置B中发生反应的离子方程式为________________________,装置C中饱和食盐水的作用是__________________________________。
(4)加热装置D时,铜粉发生反应的化学方程式为____________________________。
(5)比较下列两组实验,你认为下列说法正确的是_____(填序号)。
实验①:将足量的二氧化锰与含0.4molHCl的浓盐酸反应。
实验②:将8.7g二氧化锰与足量的浓盐酸反应。
A.①产生的氯气多 B.产生的氯气一样多
C.②产生的氯气多 D.无法判断
高一化学实验题困难题查看答案及解析
(共7分)某同学设计了下图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:

(1)若A为浓氨水,B为氧化钙,C中盛有AlCl3溶液,旋开活塞E,足够长时间后,观察到C中的现象为,圆底烧瓶中发生反应的化学方程式为________;
(2)若A为30%的H2O2溶液,B为二氧化锰,C中盛有酸化过的FeCl2溶液,旋开活塞E后,C中的现象为________,圆底烧瓶中发生反应的化学方程式为________;
(3)利用上述装置还可以验证SO2的化学性质, A为较浓硫酸,B为亚硫酸钠,则C中盛有________
溶液可验证SO2的氧化性; C中盛有________溶液可验证其还原性; 而C中盛有________溶液可验证其漂白性。
高一化学填空题简单题查看答案及解析
某校化学兴趣小组的同学分别对氯气和氯水的性质进行探究。
Ⅰ.下图是实验室制备氯气并进行一系列相关实验的装置(部分夹持装置已略)。
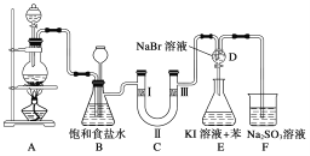
(1)制备氯气选用的药品为二氧化锰和浓盐酸,A中反应的化学方程式为
__________________________________。
(2)装置B中饱和食盐水的作用是______;同时装置B还能监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象______。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ处最好依次放入________(填序号)。
①干燥的有色布条 ②湿润的有色布条 ③碱石灰④无水氯化钙 ⑤浓硫酸
(4)当向D中缓缓通入一定量氯气时,D中溶液逐渐变为______色;再打开D装置活塞,将装置D中少量溶液滴入锥形瓶E中,振荡,观察到的现象是___________________。
(5)有人提出,装置F中可改用足量的饱和NaHSO3溶液吸收氯气,请判断是否可行________(填“是”或“否”),理由是__________________________________ (用离子反应方程式表示)。
高一化学实验题中等难度题查看答案及解析
下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备和A中加热装置已省略)。
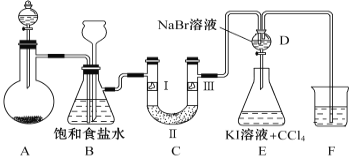
请回答:
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,相关反应的化学方程为________________。
(2)装置B中饱和食盐水的作用是____________。同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象___________________________________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入_______。
| 选项 | Ⅰ | Ⅱ | Ⅲ |
| A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| B | 干燥的有色布条 | 硅胶 | 湿润的有色布条 |
| C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| D | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)装置F烧杯中盛放的试剂是_______________。
(5)设计装置D、E的目的是比较Cl2、Br2、I2的氧化性强弱。当向D中缓缓通入足量氯气时,可以看到无色溶液逐渐变为橙黄色,说明Cl2的氧化性大于Br2。打开装置D的活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是________________________________________。该现象_____________(填“能”或“不能”)说明Br2 的氧化性强于I2 。
高一化学实验题中等难度题查看答案及解析
某化学小组经查阅资料得知常温下过量的氨气和氯气能反应生成氯化铵,该实验小组对该反应进行探究,部分实验装置如下(夹持装置略去)
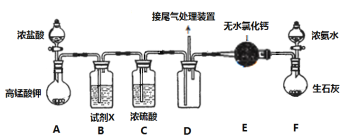
回答下列问题
(1)装置F是NH3的制备装置,其中盛放浓氨水的仪器名称是___________,再写出一种在实验室制备NH3的反应原理(用化学方程式表示)____________。
(2)某同学认为应将E中的无水氯化钙换成碱石灰,他的理由______________。
(3)装置A中发生反应的离子方程式为___________。
(4)装置B中盛装的试剂X的名称为_________,该装置的作用为__________。
(5)装置D的设计中有明显不足之处,请提出改进意见______________。
(6)某同学设计实验证明装置D中所得固体为氯化铵,请把实验步骤写完整:
①取少量装置D中所得固体产物配成溶液,并取少量溶液于两支试管中;
②__________________________;
③向另一只试管中加过量稀硝酸,再加AgNO3溶液,有白色沉淀生成,结论:常温下过量的氨气和氯气反应可生成氯化铵。
高一化学实验题中等难度题查看答案及解析
某化学兴趣小组的同学利用如图所示实验装置进行某些气体的制备、性质等实验(图中夹持装置有省略)。请按要求填空:
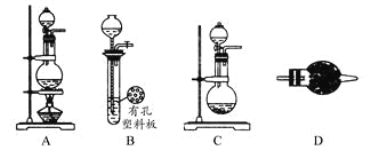
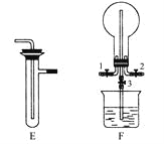
Ⅰ.探究氯气与氨气的反应
(1)为制取干燥氨气,可将装置C与___(填装置名称)连接;装置C中的烧瓶内固体宜选用___。
a.氯化钙 b.碱石灰 c.五氧化二磷 d.生石灰
(2)装置A、E、E连接可制取纯净、干燥的氯气,则两个E装置内的药品依次是__。
(3)装置F可用于探究氯气与氨气的反应。实验时打开开关1、3,关闭2,先向烧瓶中通入___(填名称),然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体。实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子___,F的烧杯中所装液体为__,所起的作用是__。
Ⅱ.探究某些物质的性质
(1)利用装置A、E,可设计实验比较Cl-和Br-的还原性强弱。将装置A中产生的气体通入盛有NaBr溶液的装置E中,充分反应后取下E,加入CCl4,静置后观察到____的实验现象,则证明Br-的还原性强于Cl-。
(2)将装置B、C分别与F相连后,进行H2S与SO2反应的实验。简述检查装置B气密性的操作____,F的烧瓶中发生反应的化学方程式为____。
高一化学实验题中等难度题查看答案及解析
某化学学习小组同学根据实验室现有的制取氨气的药品,设计了右图所示的实验装置(部分夹持仪器未画出),制取并探究氨气的还原性、检验反应产物。请回答下列问题:
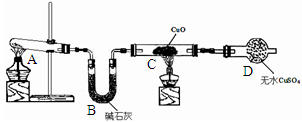
(1)A中发生反应的化学方程式是________。
(2)B中碱石灰的作用是________。
(3)C中黑色固体变红,且产生的气体对空气无污染,写出该反应的化学方程式________;
D中发生的现象是________________________________________________________________________。
(4)该装置存在明显缺陷,该缺陷是________。
(5)工业中常用氮气与氢气在高温、高压、铁触媒做催化剂的条件下合成氨气,该小组同学模拟该条件也合成出了氨气。已知起始时,将2 mol N2、6 mol H2充入一个容积为2 L的密闭容器中发生反应,过了5 min后,混合气体的总物质的量减少了1 mol,求在这段时间内以H2表示的化学反应速率
为。
高一化学实验题困难题查看答案及解析
某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:

(1)若A为水,B为过氧化钠,C中盛有稀硫酸和FeCl2混合溶液,旋开 活塞E后,C中溶液颜色变化为 ,烧瓶中发生反应的化学方程式为 。
(2)若A为盐酸、B为大理石(主要成分为CaCO3粉末)、C中盛有水玻璃,则小试管中的现象是 ,固体的主要成分为(写化学式)_________________。
(3)利用上述装置可以验证SO2的性质, 若A为浓硫酸,B为亚硫酸钠粉末,那么C中盛有 溶液时可验证其具有漂白性;而C中盛有 溶液时可验证其具有还原性(各填一种物质名称)。
高一化学填空题困难题查看答案及解析
某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
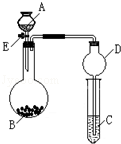
(1)若A为水,B为过氧化钠,C中盛有酸化过的FeCl2溶液,旋开活塞E后,烧瓶中发生反应的化学方程式为 ,C中的现象为
(2)利用上述装置可以验证物质的性质,如设计证明氧化性:KMnO4>Cl2 并制取漂白液(有效成分为NaClO),则A为浓盐酸,B为高锰酸钾C中发生反应的离子方程式为 D装置的作用是: 也可设计证明酸性的强弱:H2SO4>H2CO3>H2SiO3则A为硫酸、B为纯碱、C中盛有水玻璃,则小试管中的现象是 .
(3)利用上述装置可以验证SO2的性质,若A为浓硫酸,B为亚硫酸钠固体,那么C中盛有 溶液时可验证其具有漂白性;而C中盛有 溶液时可验证其具有还原性.
高一化学实验题极难题查看答案及解析