-
工业合成氨的反应为:N2(g) + 3H 2(g)  2NH3(g); △H<0
2NH3(g); △H<0
(1)、随着温度升高,平衡常数K值变_______。
(2)改变反应条件,会使平衡发生移动。如下图像表示随条件改变,氨气的百分含量的变化趋势。

当横坐标为压强时,变化趋势正确的是(选填字母序号)_________,
当横坐标为温度时,变化趋势正确的是(选填字母序号)__________。
(3)如图所示三个容积相同的容器①、②、③,若起始温度相同,分别向三个容器中充入①中3mol H2和1mol N2;②中2mol NH3;③中1.5mol H2和0.5mol N2和1mol NH3;一定条件下反应,达到平衡时各容器中NH3物质的百分含量由大到小的顺序为_____(填容器编号)。

(4)氨气和氧气从145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图所示):

4NH3+5O2⇌4NO+6H2O 4NH3+3O2⇌2N2+6H2O 温度高于900℃时,NO产率下降的原因_____。
-
工业合成氨反应的化学方程式为:N2(g)+3H2(g)  2NH3(g) △=-92.3kJ/mol。一定温度下,向体积为2L的密闭容器中加入1mol N2和3mol H2,经2min后达到平衡,平衡时测得NH3的浓度为0.5 mol/L。
2NH3(g) △=-92.3kJ/mol。一定温度下,向体积为2L的密闭容器中加入1mol N2和3mol H2,经2min后达到平衡,平衡时测得NH3的浓度为0.5 mol/L。
(1)2min 内H2的反应速率v(H2)= ;
(2)充分反应并达到平衡时,放出的热量 92.3kJ(填“大于”、“小于”或“等于”)。
原因是 。
(3)下列说法可证明反应达到平衡状态的 。
A.单位时间内,断开1mol N≡N,同时断开3mol H—H
B.单位时间内,形成1mol N≡N,同时形成3mol N—H
C.单位时间内,断开1mol N≡N,同时断开6mol N—H
D.单位时间内,形成1mol N≡N,同时断开3mol H—H
(4)氨的一个重要用途是用于制备火箭发射原料N2H4(肼),已知:火箭发射的原理是N2H4(肼)在NO2中燃烧,生成N2、水蒸气。根据如下反应:
N2(g)+2O2(g)=2NO2(g) △H1=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H2=-534.0kJ/mol
写出在相同状态下,发射火箭反应的热化学方程式 。
-
随着世界粮食需求量的增长,农业对化学肥料的需求量越来越大,其中氮肥是需求量最大的一种化肥.而氨的合成为氮肥的生产工业奠定了基础,其原理为:N2+3H2⇌2NH3
(1)在N2+3H2⇌2NH3的反应中,一段时间后,NH3的浓度增加了0.9mol•L-1.用N2表示其反应速率为0.15mol•L-1•s-1,则所经过的时间为________;
A.2s B.3s C.4s D.6s
(2)下列4个数据是在不同条件下测得的合成氨反应的速率,其中反应最快的是________;
A.v(H2)=0.1mol•L-1•min-1 B.v(N2)=0.1mol•L-1•min-1
C.v(NH3)=0.15mol•L-1•min-1 D.v(N2)=0.002mol•L-1•min-1
(3)在一个绝热、容积不变的密闭容器中发生可逆反应:N2(g)+3H2(g)⇌2NH3(g)△H<0.下列各项能说明该反应已经达到平衡状态的是________.
A.容器内气体密度保持不变
B.容器内温度不再变化
C.断裂1mol N≡N键的同时,断裂6mol N-H键
D.反应消耗N2、H2与产生NH3的速率之比1:3:2.
-
合成氨是工业上的重要反应:N2(g)+3H2(g) 2NH3(g),下列说法不正确的是
2NH3(g),下列说法不正确的是
A. 反应达平衡状态后,各物质浓度不变,反应停止
B. 反应达平衡状态后,单位时间内生成1mol N2的同时消耗3mol H2
C. 在上述条件下,N2不可能100%转化为NH3
D. 使用催化剂是为了加快反应速率,提高生产效率
-
合成氨时,在某个密闭容器中发生反应:3H2(g)+N2(g) 2NH3(g)
2NH3(g)
(1)下列能使反应速率加快的是_____________________
①升高温度 ②减小容器体积 ③通入N2 ④通入Ar使压强增大 ⑤通入HCl气体 ⑥加入合适的催化剂
A.①③④⑤ B.①②③⑥ C.①②③④ D.②④⑤⑥
(2)在恒温、恒容的条件下,下列说法能表示反应达到化学平衡状态的是__________
①当有1molN2被消耗,就有2molNH3生成
②当有6molH—H键形成时,就有12molN—H键形成
③2 正(N2)=
正(N2)= 逆(NH3)
逆(NH3)
④N2的物质的量不再变化
⑤H2、N2、NH3的浓度之比等于3:1:2
⑥混合气体的密度不变
⑦混合气体的压强不变
⑧混合气体的平均相对分子质量不变
A.①③④⑤⑦ B.①②③④⑧ C.②③④⑦⑧ D.②④⑤⑥
(3)在2 L定容密闭容器中通入1 mol N2(g)和3 mol H2(g),发生反应:3H2(g)+N2(g) 2NH3(g)(放热反应)。测得压强-时间图像如图甲,测得p2=0.8p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如图乙图像。
2NH3(g)(放热反应)。测得压强-时间图像如图甲,测得p2=0.8p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如图乙图像。

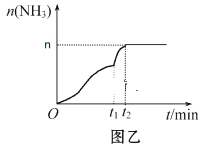
①如图甲,反应开始至平衡时NH3的平均反应速率为_____________________,平衡时氢气的转化率为_________。
②如图乙,下列说法正确的是_________
A.t1时刻可能是加入了催化剂
B.改变条件可以使H2 100℅转化为NH3
C.增大N2的浓度,可以提高H2的转化率
D.t2时刻,N2的浓度与NH3的浓度之比为1:2
-
合成氨反应:N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ•mol-1,在反应过程中,正反应速率的变化如图.下列说法正确的是( )
2NH3(g)△H=-92.4kJ•mol-1,在反应过程中,正反应速率的变化如图.下列说法正确的是( )
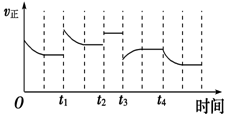
A.t1时升高了温度
B.t2时使用了催化剂
C.t3时增大了压强
D.t4时降低了温度
-
(8分)下表表示合成氨反应(N2+3H2  2NH3)在不同条件下达到平衡时混合物中氨的含量[起始时v(N2):v(H2)==1:3]。
2NH3)在不同条件下达到平衡时混合物中氨的含量[起始时v(N2):v(H2)==1:3]。
|  压强(MPa) 压强(MPa)
 氨的含量 氨的含量
温度(℃) | 0.1 | 10 | 30 | 60 | 100 |
| 200 | 0.153 | 0.815 | 0.899 | 0.954 | 0.988 |
| 300 | 0.022 | 0.520 | 0.710 | 0.842 | 0.926 |
| 400 | 0.004 | 0.251 | 0.470 | 0.652 | 0.798 |
分析上表数据,回答下列问题:
(1)200℃、100MPa时,平衡混合物中氨的含量已达0.988,如果继续增大压强________
(填“能”或“不能”)使平衡混合物中氨的含量等于1,理由是:________
。
(2)欲使平衡混合物中氨的含量增大,则可采取的措施有: ________。
(3) 欲使平衡混合物中氨的含量为0.710,则选择的反应条件应为:
欲使平衡混合物中氨的含量为0.710,则选择的反应条件应为:
-
某温度下,对于反应N2(g)+3H2(g)  2NH3(g) ΔH=-92.4 kJ/mol,N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是
2NH3(g) ΔH=-92.4 kJ/mol,N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是

A.平衡状态由A变到B时,平衡常数K(A) = K(B)
B.将1 mol氮气、3 mol氢气,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ
C.升高温度,逆反应速率增大,正反应速率减小
D.上述反应达到平衡后,增大H2浓度,平衡正向移动,H2转化率增大
-
在工业上合成氨反应:N2+3H2  2NH3 ,欲增大反应速率,下列措施可行的是:
2NH3 ,欲增大反应速率,下列措施可行的是:
A.降低温度 B.减小压强 C.减小H2的浓度 D.使用催化剂
-
反应N2(g)+3H2(g) 2NH3(g)是一放热反应。如果反应在密闭容器中进行,下列有关说法中不正确的是( )
2NH3(g)是一放热反应。如果反应在密闭容器中进行,下列有关说法中不正确的是( )
A. 升高温度会使反应速率加快
B. 当NH3的浓度不再变化时,反应达到了平衡状态
C. 在高温和催化剂作用下,H2可以100%地转化为NH3
D. 使用催化剂可以加快反应速率
2NH3(g); △H<0





