H2O2是一种二元弱酸,对于0.1 mol·L-1的过氧化氢溶液,下列叙述不正确的是( )
A.H2O2的电离方程式可写作H2O2H++HO2-,HO2-
H++O42-
B.加水稀释过程中,K1(H2O2)增大,α(H2O2)增大,c(H+)增大
C.加入少量浓盐酸,过氧化氢的电离平衡逆向移动,水的电离平衡逆向移动
D.加入少量氯化铁溶液,溶液中产生大量气泡
高三化学选择题中等难度题
H2O2是一种二元弱酸,对于0.1 mol·L-1的过氧化氢溶液,下列叙述不正确的是( )
A.H2O2的电离方程式可写作H2O2H++HO2-,HO2-
H++O42-
B.加水稀释过程中,K1(H2O2)增大,α(H2O2)增大,c(H+)增大
C.加入少量浓盐酸,过氧化氢的电离平衡逆向移动,水的电离平衡逆向移动
D.加入少量氯化铁溶液,溶液中产生大量气泡
高三化学选择题中等难度题
H2O2是一种二元弱酸,对于0.1 mol·L-1的过氧化氢溶液,下列叙述不正确的是( )
A.H2O2的电离方程式可写作H2O2H++HO2-,HO2-
H++O42-
B.加水稀释过程中,K1(H2O2)增大,α(H2O2)增大,c(H+)增大
C.加入少量浓盐酸,过氧化氢的电离平衡逆向移动,水的电离平衡逆向移动
D.加入少量氯化铁溶液,溶液中产生大量气泡
高三化学选择题中等难度题查看答案及解析
常温下,0.1mol·L-1的H2A溶液中各种微粒浓度的对数值(lgc)与pH的关系如图所示。
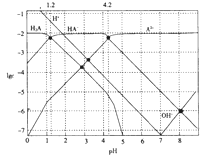
下列说法不正确的是
A. H2A是二元弱酸
B. HA-H++A2-的电离平衡常数Ka=10-12
C. 0.1mol·L-1的H2A溶液中:c(H+)=c(HA-)+2c(A2-)+c(OH-)
D. pH=4.2 时:c(HA-)=c(A2-)>c(H+)>c(H2A)>c(OH-)
高三化学单选题中等难度题查看答案及解析
常温下,运用电离理论做出的预测正确的是
A.测定某二元弱酸钠盐溶液的pH,可能小于7
B.稀释0.1mol/LCH3COOH(aq),可能变大也可能变小
C.在20.00mL浓度均为0.100 mol/L的HCl与CH3COOH混合溶液中滴加0.200mol/LNaOH溶液至pH=7,NaOH溶液体积一定小于20.00mL
D.pH=8的碱性溶液中一定没有CH3COOH分子
高三化学多选题中等难度题查看答案及解析
改变0.1 mol·L-1二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示[已知]。下列叙述不正确的是( )
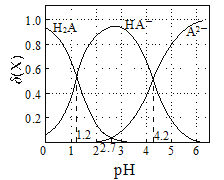
A.NaHA溶液中,HA-的水解能力小于HA-的电离能力
B.lg[K2(H2A)]=-4.2
C.将等物质的量的NaHA和Na2A混合物溶于水,所得的溶液中α(HA-)=α(A2-)
D.0.1 mol·L−1 NaHA溶液中:c(Na+)+c(A2−)+c(H2A)+c(HA−)=0.2 mol·L−1
高三化学单选题困难题查看答案及解析
常温下,向0.1mol·L−1二元弱酸H2A的溶液中逐滴加入NaOH溶液,H2A、HA-、A2−的物质的量分数随pH的变化如图所示。下列叙述正确的是( )
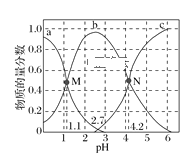
A.a曲线代表HA−的物质的量分数随pH的变化
B.M点pH=1.1时,溶液中微粒浓度关系为c(H+)>c(HA−)=c(H2A)
C.pH=2.7时,c(A2−)+c(HA−)+c(H2A)=0.1mol·L−1
D.N点pH=4.2时,c(A2−)=c(HA−),溶液中不存在H2A分子
高三化学单选题中等难度题查看答案及解析
常温下,向0.1mol·L−1二元弱酸H2A的溶液中逐滴加入NaOH溶液,H2A、HA-、A2−的物质的量分数随pH的变化如图所示。下列叙述正确的是( )
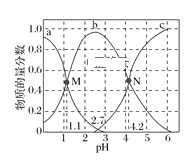
A.a曲线代表HA−的物质的量分数随pH的变化
B.M点pH=1.1时,溶液中微粒浓度关系为c(H+)>c(HA−)=c(H2A)
C.pH=2.7时,c(A2−)+c(HA−)+c(H2A)=0.1mol·L−1
D.N点pH=4.2时,c(A2−)=c(HA−),溶液中不存在H2A分子
高三化学单选题中等难度题查看答案及解析
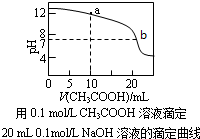

高三化学选择题中等难度题查看答案及解析
向10 mL 0.1mol/L二元弱酸H2A溶液中滴加0.1mol/L NaOH 溶液,溶液中各组分物质的量分数δ(X) [δ(X)=]随pH的变化如图所示。下列叙述错误的是

A. Ka1(H2A) 为10-3.1
B. pH=5.0时,c(Na+)>c(HA-)>c(H+)>c(OH-) >c(A2-)
C. pH=8.2时,c (Na+) +c(H+) =c(OH-) +3c(A2-)
D. pH 由5.0 调至10.5 时,主要反应的离子方程式为HA-+OH-=A2-+H2O
高三化学单选题困难题查看答案及解析
t℃时,向20.00mL0.1mol/L二元弱酸H2X溶液中滴入0.1mol/LNaOH溶液,溶液中由水电离出的c水(OH-)的负对数[-lgc 水(OH-)]与所加NaOH溶液体积的关系如图所示。下列说法中不正确的是
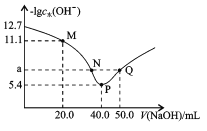
A.M点溶液中:c(Na+)>c(HX-)>c(H2X)
B.P点溶液中: c(OH-)-c(H+)=c(HX-)+2c(H2X)
C.溶液中
D.水的电离程度:P>N=Q>M,且a=7
高三化学单选题困难题查看答案及解析
双氧水(H2O2)和水都是极弱的电解质,但H2O2 溶液显弱酸性。把H2O2 看成二元弱酸,则下列化学方程式不正确的是
A. H2O2 在水中电离的离子方程式:H2O2H++HO2-
B. 少量Na2O2与稀盐酸反应的离子方程式:O22-+2H+==H2O2
C. H2O2 稀溶液与Ba(OH)2稀溶被反应生成正盐的化学方程式:H2O2 +Ba(OH)2=BaO2+2H2O
D. H2O2 稀溶液与Ba(OH)2 稀溶液反应生成酸式盐的化学方程:2H2O2 +Ba(OH)2=Ba(HO2)2+2H2O
高三化学单选题中等难度题查看答案及解析