-
(8分)把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间(单位:秒)的关系可用如图曲线来表示,回答下列问题:
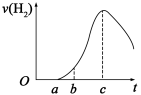
(1)曲线由O →a段不产生氢气的原因(请用有关反应的化学方程式表示)是 。
(2)曲线a→c段,产生氢气的速率增加较快,而曲线由c以后,产生氢气的速率逐渐下降,解释上述现象的原因是 。
(3)在b到c这段时间内,收集到氢气VL(标准状况),则这段时间内用硫酸表示的平均速率为 (假设反应前后溶液体积不变)。
(4)对于足量镁条和100ml 2mol/L硫酸生成氢气的反应,下列措施能减缓反应速率,但又不影响生成氢气的总量的是 。
① 加NaOH固体;
② 加适量BaCl2溶液;
③ 加KNO3溶液;
④ 加适量H2O;
⑤ 将镁条换成镁粉;
⑥ 加小苏打溶液;
⑦ 加少量CuSO4溶液;
⑧ 加适量Na2SO4溶液;
⑨ 将2 mol/L硫酸换成160mL 2.5mol/L的盐酸 ;
(5)若使用催化剂,会不会使氢气的产量增加? (填“会”或“不会”)。
-
把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
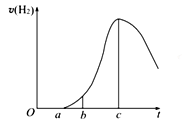
(1)曲线由O→a段不产生氢气的原因是____ ;有关反应的离子方程式为_____ ;
(2)曲线a→c段,产生氢气的速率增加较快的主要原因____ ___ ____ _ __ ;
(3)该反应若使用催化剂,能使H2产量增多吗? (填“能” 或“不能” )
-
把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
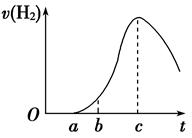
(1)曲线由O →a段不产生氢气的原因是___________________________________
有关反应的化学方程式为_________________________________
(2)曲线a→c段,产生氢气的速率增加较快的主要原因是_________________________
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是_________________________
(4)该反应若使用催化剂,可使H2产量增多吗______________(填“会”或“不会”)。
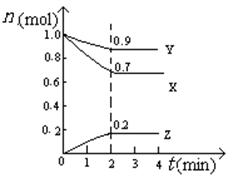
(5)某温度时,在2L密闭容器中X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。
由图中的数据分析,该反应的化学方程式为________ 。
反应从开始至2min末,Z的平均反应速率为________。
-
(8分)把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:

(1)曲线由O →a段不产生氢气的原因是____________________________________________________________;
有关反应的化学方程式为
__________________________________________________;
(2)曲线a→c段,产生氢气的速率增加较快的主要原因是
________________________________________________________________________
________________________________________________________________________;
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是_________________________;
(4)该反应若使用催化剂,可使H2产量增多吗?______(填“会”或“不会”)。
-
(一)把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
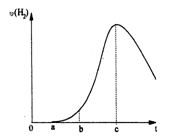
(1)曲线由O →a段不产生氢气的原因是__________ 有关反应的化学方程式为____ __________
(2)曲线a→c段,产生氢气的速率增加较快的主要原因是____________________________
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是_________________________________
(4)该反应若使用催化剂,可使H2产量增多吗?______________(填“会”或“不会”)。
-
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如右的坐标曲线来表示,回答下列问题:
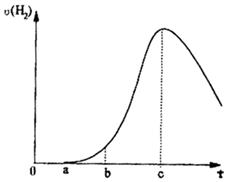
1.曲线由0→a段不产生氢气的原因____________________,
有关的离子方程式为___________________________;
2.曲线由a→b段产生氢气的速率较慢的原因________________;
3.曲线由b→c段,产生氢气的速率增加较快的主要原因___________;
4.曲线由c以后,产生氢气的速率逐渐下降的主要原因____________。
-
I.把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用下图所示的坐标曲线来表示。
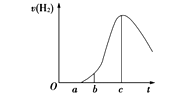
请回答下列问题。
(1)曲线由O→a段不产生氢气的原因是____________________。
有关反应的化学方程式为_________________________。
(2)曲线由a→c段,产生氢气的速率增加较快的主要原因是_______________________________。
(3)曲线由c以后产生氢气的速率逐渐下降的主要原因是_______________________________。
II.某同学在用稀硫酸与锌反应制取氢气的实验中,发现加入少量硫酸铜溶液可以加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有:______________、_________________;
(2) 硫酸铜溶液可以加快氢气生成速率的原因:__________________;
(3) 实验中现有Na2SO4、MgSO4、 Ag2SO4、 K2SO4四种溶液,可与上述实验中CuSO4溶液起相似作用的是:________。
-
I.把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L﹣1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用下图所示的坐标曲线来表示.请回答下列问题.

(1)曲线由O→a段不产生氢气的原因是_____.有关反应的化学方程式为_____.
(2)曲线由a→c段,产生氢气的速率增加较快的主要原因是_____.
(3)曲线由c以后产生氢气的速率逐渐下降的主要原因是_____.
II.某同学在用稀硫酸与锌反应制取氢气的实验中,发现加入少量硫酸铜溶液可以加快氢气的生成速率.请回答下列问题:
(1)上述实验中发生反应的化学方程式有:_____、_____;
(2)硫酸铜溶液可以加快氢气生成速率的原因:_____;
(3)实验中现有Na2SO4、MgSO4、Ag2SO4、K2SO4四种溶液,可与上述实验中CuSO4溶液起相似作用的是:_____.
-
(9分)把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol·L-1盐酸溶液的烧杯中,该铝片与盐酸反应产生氢气的速率与反应时间的关系可用下图所示的坐标曲线来表示,回答下列问题:
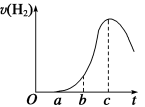
(1)曲线O→a段不产生氢气的原因,用化学方程式解释为 。
(2)曲线b→c段产生氢气的速率增加较快的主要原因是 。
(3)向溶液中加入下列物质,能加快上述化学反应速率的是 。
A.蒸馏水
B.改用铝粉
C.饱和氯化钠溶液
D.浓盐酸
E.少量硫酸铜溶液
-
把在空气中久置的铝片5.0 g投入盛有 500mL0.5 mol·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如右的坐标曲线来表示,回答下列问题:
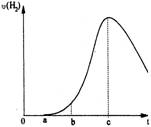
(1)曲线由0→a段不产生氢气的原因___________,
有关反应的离子方程式为____________________;
(2)曲线由a→b段产生氢气的速率较慢的原因___________
有关的化学方程式__________________________;
(3)曲线由b→c段,产生氢气的速率增加较快的主要原因_________________________;
(4)曲线由c以后,产生氢气的速率逐渐下降的主要原因_________________________。










