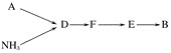-
高纯氧化铁性能稳定,无毒、无臭、无味,是食品、药品、化妆品常用着色剂。 某实验小组用工业FeCl3粗品(含Ca、Mn、Cu等杂质离子)为原料,以萃取剂Y(甲基异丁基甲酮)萃取法制取高纯氧化铁。实验过程中的主要操作步骤如下:

已知:试剂X是浓盐酸,HCl(浓)+FeCl3 HFeCl4
HFeCl4
请回答下列问题:
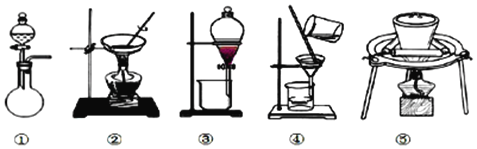
(1)据上述实验操作过程判断,下列实验装置中,没有用到的是_________(填序号)

(2)用萃取剂Y萃取的步骤中:
①Ca、Mn、Cu等杂质离子几乎都在_________ (填“水”或“有机”)相中。
②分液时,为保证液体顺利流下,应先_________,再打开旋塞,待下层液体完全流尽时,关闭悬塞后再从上口倒出上层液体。
(3)制备萃取剂Y(甲基异丁基甲酮)时,其粗产品中含有异丙叉丙酮、4-甲基-2-戌醇、酸性物质等杂质。一般可采用蒸馏法进行提纯。蒸馏时,应将温度计水银球置于_________。蒸馏前,预处理粗产品时,可以先用_________洗(填所选试剂对应的字母,下同),后用_________洗,最后用_________洗。
A水 B碳酸氢钠溶液 C乙醇
(4)下列试剂中,反萃取剂Z的最佳选择是_________,反萃取能发生的原因是_________(从化学平衡的角度进行解释)。
A.高纯水 B.盐酸 C.稀硫酸 D.酒精
(5)测定产品中氧化铁的含量需经酸溶、还原为Fe2+,然后在酸性条件下用标 准K2Cr2O7溶液滴定(还原产物是Cr3+,杂质不与K2Cr2O7反应)。现准确称取1.0g样品经酸溶、还原为Fe2+,用0.1000mol/L的标准溶液进行滴定。
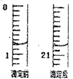
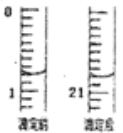
①滴定起始和终点的液面位置如图,则消耗K2Cr2O7标准溶液体积为_________mL。
②产品中氧化铁的含量为_________(保留三位有效数字)。
(6)我国早期科技丛书《物理小识·金石类》就有煅烧青矾(又名绿矾,FeSO4·7H2O)制氧化铁的记载:“青矾厂气熏人,衣服当之易烂,载木不盛”,据此分析,写出煅烧青矾制氧化铁的化学方程式:_________。
-
高纯氧化铁性能稳定,无毒、无臭、无味,是食品、药品、化妆品常用着色剂。 某实验小组用工业FeCl3粗品(含Ca、Mn、Cu等杂质离子)为原料,以萃取剂Y(甲基异丁基甲酮)萃取法制取高纯氧化铁。实验过程中的主要操作步骤如下:

已知:试剂X是浓盐酸,HCl(浓)+FeCl3 HFeCl4
HFeCl4
请回答下列问题:
(1)据上述实验操作过程判断,下列实验装置中,没有用到的是_________(填序号)
(2)用萃取剂Y萃取的步骤中:
①Ca、Mn、Cu等杂质离子几乎都在_________ (填“水”或“有机”)相中。
②分液时,为保证液体顺利流下,应先_________,再打开旋塞,待下层液体完全流尽时,关闭悬塞后再从上口倒出上层液体。
(3)制备萃取剂Y(甲基异丁基甲酮)时,其粗产品中含有异丙叉丙酮、4-甲基-2-戊醇、酸性物质等杂质。一般可采用蒸馏法进行提纯。蒸馏时,应将温度计水银球置于_________。蒸馏前,预处理粗产品时,可以先用_________洗(填所选试剂对应的字母,下同),后用_________洗,最后用_________洗。
A水 B碳酸氢钠溶液 C乙醇
(4)下列试剂中,反萃取剂Z的最佳选择是_________,反萃取能发生的原因是_________(从化学平衡的角度进行解释)。
A.高纯水 B.盐酸 C.稀硫酸 D.酒精
(5)测定产品中氧化铁的含量需经酸溶、还原为Fe2+,然后在酸性条件下用标 准K2Cr2O7溶液滴定(还原产物是Cr3+,杂质不与K2Cr2O7反应)。现准确称取1.0g样品经酸溶、还原为Fe2+,用0.1000mol/L的标准溶液进行滴定。
①滴定起始和终点的液面位置如图,则消耗K2Cr2O7标准溶液体积为_________mL。
②产品中氧化铁的含量为_________(保留三位有效数字)。
-
保险粉又称连二亚硫酸钠(Na2S2O4),可用于纺织工业的漂白剂、脱色剂,脱氯剂。Na2S2O4是白色粉末,无味,易溶于水、难溶于乙醇,具有极强的还原性,在空气中易被氧化,在碱性介质中稳定。
Ⅰ.甲酸钠( HCOONa) 法制备过程如下:

(1)连二亚硫酸钠中硫元素的化合价为______________。
(2)实验室用Na2SO3 固体和某酸反应制备SO2气体,制备SO2时所选用的酸,你认为下列最适宜选用的是______________。
A.浓盐酸 B.浓硝酸
C.质量分数为70%的硫酸 D.质量分数为10%的硫酸
(3)步骤①中制备连二亚硫酸钠的化学方程式可表示为____________________________。
(4)上述步骤②中,加入适量乙醇水溶液的作用是______________。
(5)在包装保存“保险粉”时加入少量的Na2CO3固体,目的是_________________________。
(6)①现将0.05mol/L Na2S2O4溶液在空气中放置,其溶液的pH 与时间(t)的关系如图所示。

t1时溶液中只有NaHSO3一种溶质,此时含硫元素的粒子浓度由大到小的顺序为_______________。
②t1~t2段发生化学反应的离子方程式为______________________________。
Ⅱ.电解法制备:工业上用惰性电极电解NaHSO3溶液得到Na2S2O4。过程如图所示
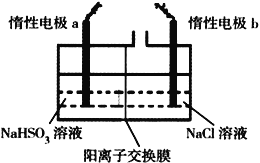
(7) ①产品在_________________(填“阳极”、“阴极”)得到。
②若不加隔膜,则连二亚硫酸钠产率降低,其原因是__________________________________。
-
氯化亚铜(CuCl)在石油工业生产中常用作脱硫剂和脱色剂.工业生产氯化亚铜的一种工艺流程如图所示:
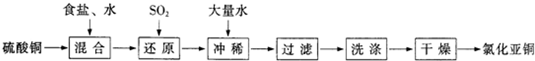
已知:①CuCl难溶于水和乙醇,干燥的CuCl在空气中比较稳定,但湿的CuCl在空气中易发生水解和氧化;②CuCl溶于氯化钠的浓溶液可生成CuCl2-,CuCl2-的溶液用水稀释可生成CuCl沉淀,反应式为CuCl2- CuCl↓+Cl-.
CuCl↓+Cl-.
(1)往CuSO4和NaCl混合液中通入SO2可生成CuCl2-和硫酸,请写出反应的离子方程式:________.
(2)在反应(1)中,温度升至70~80℃,并使用NaCl浓溶液,主要目的是________.
(3)在反应(1)中,还原剂除了可用SO2外,还可选用________(填标号).
A.Na2SO3 B.Cu C.Ag
(4)过滤所得沉淀须迅速用________(填“水”或“95%乙醇”)洗涤、干燥得CuCl成品.
(5)合成氨工业生产中的CO会使催化剂中毒,可通过下列反应除去.
[Cu(NH3)2]Ac(aq)+CO(g)+NH3(g)=[Cu(NH3)3]Ac•CO(aq)△H<0,生产中为了提高CO的吸收率,可采用的措施是________.
(6)CuOH不稳定易分解为Cu2O 298K时,CuOH的Ksp=1.0×10-14,CuCl的Ksp=1.2×10-6.把CuCl固体和NaOH溶液混合,加热,得到红色沉淀,该沉淀的化学式为________.
-
亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒,国际上对食品中亚硝酸钠的用量控制在很低的水平上。某学习小组针对亚硝酸钠设计了如下实验:
(实验Ⅰ)制备NaNO2
该小组查阅资料知:2NO+Na2O2=2NaNO2;2NO2+Na2O2=2NaNO3。
制备装置如图所示(夹持装置略去):

(1)装置D可将剩余的NO氧化成NO3-,发生反应的离子方程式为____________。
(2)如果没有B装置,C中发生的副反应有_____________、____________。
(3)甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质。于是进行了适当的改进,改进后提高了NaNO2的纯度,则其改进措施是________________________________。
(实验Ⅱ)测定制取的样品中NaNO2的含量
步骤:
a.在5个有编号的带刻度试管(比色管)中分别加入不同量的NaNO2溶液,各加入1 mL的M溶液(M遇NaNO2呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为10 mL并振荡,制成标准色阶:
| 试管编号 | ① | ② | ③ | ④ | ⑤ |
| NaNO2含量/(mg·L-1) | 0 | 20 | 40 | 60 | 80 |
b.称量0.10 g制得的样品,溶于水配成500 mL溶液。取5 mL待测液,加入1 mL M溶液,再加蒸馏水至10 mL并振荡,与标准色阶比较。
(4)步骤b中比较结果是:待测液颜色与③标准色阶相同,则甲同学制得的样品中NaNO2的质量分数是________。
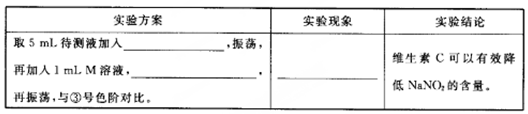
(5)用目视比色法证明维生素C可以有效降低NaNO2的含量。设计并完成下列实验报告。
| 实验方案 | 实验现象 | 实验结论 |
| 取5 mL待测液,加入______________,振荡,再加入1 mL M溶液,_______________,再振荡,与③标准色阶对比 | _______________ | 维生素C可以有效降低NaNO2的含量 |
-
亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒,国际上对食品中亚硝酸钠的用量控制在很低的水平上。某学习小组针对亚硝酸钠设计了如下实验:
【实验I】制备NaNO2
该小组查阅资料知:①2NO+Na2O2=2NaNO2;2NO2+Na2O2=2NaNO3
②NO能被酸性高锰酸钾氧化为NO3-。
设计制备装置如下(夹持装置略去)。
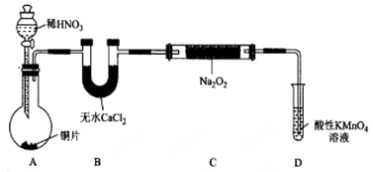
(1)装置A中用于盛放稀HNO3溶液的仪器名称为___________________;
写出装置A中发生主要反应的离子方程式 。
(2)装置D的作 用为_________________。
用为_________________。
(3)如果没有B装置,写出C中发生副反应的化学方 程式①_______________、②____________。
程式①_______________、②____________。
(4)甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质。请设计一种提高NaNO2纯度的改进措施 。
【实脸II】测定制取的样品中NaNO2的含量
步骤:已知在酸性溶液中,NO2-可将MnO4-还原为Mn2+。为测定亚硝酸钠的含量,称取4.000 g样品溶于水配成250 mL溶液,取25.00 mL溶液于锥形瓶中,用0.1000 mol·L-1酸性KMnO 4溶液进行滴定,实验所得数据如下表所示:
4溶液进行滴定,实验所得数据如下表所示:

(5)根据表中数据,计算所得固体中亚硝酸钠的质量分数__________。
-
(13分)亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒,国际上对食品中亚硝酸钠的用量控制在很低的水平上。某学习小组针对亚硝酸钠设计了如下实验:
【实验I】制备NaNO2
该小组查阅资料知:2NO+Na2O2=2NaNO2;2NO2+Na2O2=2NaNO3
设计制备装置如下(夹持装置略去):
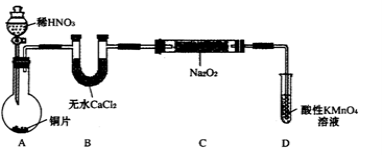
(1)装置D可将剩余的NO氧化成NO3-,发生反应的离子方程式为 。
(2)如果没有B装置,C中发生的副反应有 。
(3)甲同学检查完装置气密性良好后进行实验,发现NaNO2的纯度较低。乙同学对上述装置进行适当改进后提高了NaNO2的纯度,其改进措施是 。
(4)丙同学对B中的药品进行了更换,也提高了NaNO2的纯度。丙更换的药品最好是 。
【实验Ⅱ】测定甲、乙同学制取的样品中NaNO2的含量
步骤:a.在5个有编号的带刻度试管(比色管)中分别加入不同量的NaNO2溶液,各加入1 mL的M溶液(M遇NaNO2呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为10 mL并振荡,制成标准色阶:

b.分别称量0.10 g甲、乙制得的样品溶于水配成500 mL溶液,贴上标签甲、乙。再分离别取5 mL甲、乙待测液,各加入1 mL M溶液,均加蒸馏水至10 mL振荡,分别与标准色阶比较。
(5)步骤b中比较结果是:甲待测液颜色与③号色阶相同,乙待测液颜色与④号色阶相同。则甲同学制得的样品中NaN02的纯度是 %。
(6)用目视比色法证明维生素C可以有效降低NaNO2的含量。设计并完成下列实验报告。

-
亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒,国际上对食品中亚硝酸钠的用量控制在很低的水平上。某学习小组针对亚硝酸钠设计了如下实验:
【实验I】制备NaNO2
该小组查阅资料知:2N0+Na2O2=2NaNO2;2NO2+Na2O2=2NaNO3。
设计制备装置如下(夹持装置略去)。
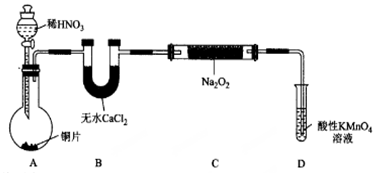
(1)装置D可将剩余的NO氧化成NO3-,发生反应的离子方程式为_______________。
(2)如果没有B装置,C中发生的副反应有____________。
(3)甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质。于是在A 与B 装且间增加了___________装置,改进后提高了NaNO2的纯度。
【实脸II】 测定制取的样品中NaNO2的含量
步骤:
A.在5个有编号的带刻度试管(比色管)中分别加人不同址的NaNO2溶液,各加入1 ml的M溶液(M遇NaNO2呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为10 mL并振荡,制成标准色阶:
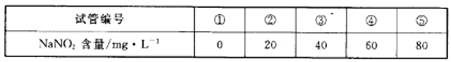
b.称量0.10g制得的样品溶于水配成500 ml溶液。取5mL待测液,加入1mlM溶液,后加蒸馏水至10mL振荡,与标准色阶比较。
(4)步脚b中比较结果:待测液颜色与③号色阶相同。则甲同学制得的样品中NaNO2的质量分数是______%。
(5)用目视比色法证明维生素C可以有效降低NaNO2的含量。设计并完成下列实验报告。
-
二氧化钛被认为是现今世界上性能最好的一种白色颜料。同时它有较好的紫外线掩蔽作用,超细的二氧化钛粉末也被加入到防晒膏中制成防晒化妆品。现在某实验小组按照下面的流程来合成纳米二氧化钛。
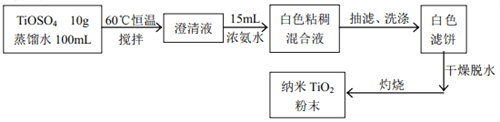
实验机理: TiOSO4+2NH3•H2O = TiO(OH)2↓+(NH4)2SO4
信息提示:①钛元素化合物的性质和铝有一定的相似性。TiO2具有两性,Ti(OH)4不稳定,容易失去一分子水形成TiO(OH)2。
②钛的原子量: 48
③浓氨水的密度:0.91g •cm-3
(1)灼烧时用到的硅酸盐容器是_______。
(2)下列说法正确的是_______。
A. 为了加快反应速率,可以用氢氧化钠溶液代替浓氨水
B. 为了提高产率,反应容器需要用滤液洗
C. 为了防止抽滤时滤纸破裂,抽滤时可以使用两层滤纸
D. 为了加快干燥的速率,干燥时可以用小火加热
E. 灼烧后需要冷却到室温,称量一次所得数值即为 TiO2的质量
(3)为了使实验过程中尽可能的减少环境污染,同时要注意操作的安全性, 请你指出该反应装置图中的需要改进之处(指出两处即可)_____________。

(4)反应后的白色粘稠混合液经过抽滤、洗涤可以得到白色滤饼。如何证明白色滤饼已经洗干净了呢?_____。
(5)焙烧后有时会有少量的TiO2残留在容器中无法去除,我们可以用NaOH溶液将残留的TiO2洗干净。请你用化学方程式表示该洗涤原理___________。
(6)最后称得纳米 TiO2 的质量是a 克,请你计算用该方法制备 TiO2的产率________。
-
工业尾气中的氮氧化物常用氨催化吸收法,原理是NH3与NOx反应生成无毒物质。某同学采用以下装置和步骤模拟工业上氮氧化物的处理过程。
(一)提供的装置
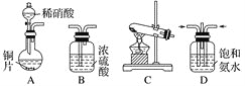
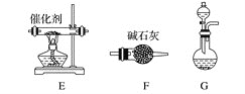
(二)NH3的制取
(1)下列有关实验室制备气体的说法正确的是__________(填序号)。
①可以用排饱和食盐水的方法收集氯气 ②用赤热的炭与水蒸气反应制取氢气 ③实验室制氧气有时需要加热,有时不需要加热 ④用无水氯化钙干燥氨气 ⑤用浓盐酸洗涤高锰酸钾分解制氧气的试管
(2)从所提供的装置中选取一个能制取氨气的装置:________________(填序号)。
(3)当采用你所选用的装置制取氨气时,相应反应的化学方程式是___________。
(三)模拟尾气的处理
选用上述部分装置,按下列顺序连接成模拟尾气处理装置,回答有关问题:
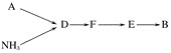
(4)A中反应的离子方程式为___________。
(5)D装置中的液体可换成________(填序号)。
a CuSO4 b H2O c CCl4 d 浓硫酸
(6)该同学所设计的模拟尾气处理实验还存在的明显缺陷是________________。

HFeCl4