头孢克洛是人工合成的第二代口服头孢菌抗生素,主要用于上、下呼吸道感染、中耳炎、皮肤、尿道感染等症状,其结构如图所示,下列关于头孢克洛的说法错误的是

A.其分子式可以表示为C15H16ClN3O6S
B.该物质具有两性
C.lmol该化合物与NaOH溶液作用时消耗NaOH的物质的量最多为6 mol
D.该物质的分子结构中有3个手性碳原子
高三化学选择题中等难度题
头孢克洛是人工合成的第二代口服头孢菌抗生素,主要用于上、下呼吸道感染、中耳炎、皮肤、尿道感染等症状,其结构如图所示,下列关于头孢克洛的说法错误的是

A.其分子式可以表示为C15H16ClN3O6S
B.该物质具有两性
C.lmol该化合物与NaOH溶液作用时消耗NaOH的物质的量最多为6 mol
D.该物质的分子结构中有3个手性碳原子
高三化学选择题中等难度题
头孢克洛是人工合成的第二代口服头孢菌抗生素,主要用于上、下呼吸道感染、中耳炎、皮肤、尿道感染等症状,其结构如图所示,下列关于头孢克洛的说法错误的是

A.其分子式可以表示为C15H16ClN3O6S
B.该物质具有两性
C.lmol该化合物与NaOH溶液作用时消耗NaOH的物质的量最多为6 mol
D.该物质的分子结构中有3个手性碳原子
高三化学选择题中等难度题查看答案及解析
 ,关于头孢呋辛酯的下列说法不正确的是( )
,关于头孢呋辛酯的下列说法不正确的是( )
高三化学选择题中等难度题查看答案及解析
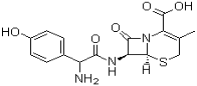
头孢羟氨苄(如图)被人体吸收效果良好,疗效明显,且毒性反应极小,因而被广泛适用于敏感细菌所致的尿路感染、皮肤软组织感染以及急性扁桃体炎、急性咽炎、中耳炎和肺部感染等的治疗。已知肽键可以在碱性条件下水解。下列对头孢羟氨苄的说法中正确的是
 ·H2O
·H2O
A.头孢羟氨苄的化学式为C16H16N3O5S·H2O
B.1mol头孢羟氨苄与NaOH溶液和浓溴水反应时,分别需要消耗NaOH 4mol和Br2 3mol
C.在催化剂存在的条件下,1mol头孢羟氨苄消耗7molH2
D.头孢羟氨苄能在空气中稳定存在
高三化学选择题简单题查看答案及解析
头孢羟氨苄(如图)被人体吸收效果良好,疗效明显,且毒性反应极小,因而被广泛适用于敏感细菌所致的尿路感染、皮肤软组织感染以及急性扁桃体炎、急性咽炎、中耳炎和肺部感染等的治疗。已知肽键可以在碱性条件下水解。下列对头孢羟氨苄的说法中正确的是( )
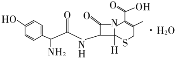
A. 头孢羟氨苄的化学式为C16H16N3O5S·H2O
B. 1 mol头孢羟氨苄与NaOH溶液和浓溴水反应时,分别需要消耗NaOH 4 mol和Br2 3mol
C. 在催化剂存在的条件下,1mol头孢羟氨苄消耗7 mol H2
D. 头孢羟氨苄能在空气中稳定存在
高三化学单选题简单题查看答案及解析
头孢羟氨苄(如图)被人体吸收效果良好,疗效明显,且毒性反应极小,因而被广泛适用于敏感细菌所致的尿路感染、皮肤软组织感染以及急性扁桃体炎、急性咽炎、中耳炎和肺部感染等的治疗。已知肽键可以在碱性条件下水解。下列对头孢羟氨苄的说法中正确的是 ( )
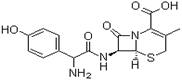
A.头孢羟氨苄的化学式为C16H16N3O5S·H2O
B. 1mol头孢羟氨苄与NaOH溶液和浓溴水反应时,分别需要消耗NaOH 4mol和Br2 3mol
C.在催化剂存在的条件下,1mol头孢羟氨苄消耗7molH2
D. 头孢羟氨苄能在空气中稳定存在
高三化学选择题中等难度题查看答案及解析
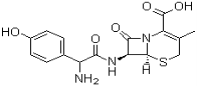
头孢羟氨苄(如图)被人体吸收效果良好,疗效明显,且毒性反应极小,因而被广泛适用于敏感细菌所致的尿路感染、皮肤软组织感染以及急性扁桃体炎、急性咽炎、中耳炎和肺部感染等的治疗。已知肽键可以在碱性条件下水解。下列对头孢羟氨苄的说法中正确的是
 ·H2O
·H2O
A.头孢羟氨苄的化学式为C16H16N3O5S·H2O
B.1mol头孢羟氨苄与NaOH溶液和浓溴水反应时,分别需要消耗NaOH 4mol和Br2 3mol
C.在催化剂存在的条件下,1mol头孢羟氨苄消耗7molH2
D.头孢羟氨苄能在空气中稳定存在
高三化学选择题简单题查看答案及解析
头孢呋辛酯胶囊为第二代头孢菌素类抗生素,其结构简式如下,有关该化合物的下列说法错误的是
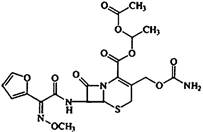
A.分子式为C20H22N4O10S
B.在酸性条件下加热水解,有CO2放出,在碱性条件下加热水解有NH3放出
C.1mol该物质在碱性条件下水解,最多消耗5molNaOH
D.能发生加成、氧化、还原、取代等反应
高三化学选择题简单题查看答案及解析
莫西沙星主要用于治疗呼吸道感染,合成路线如下:
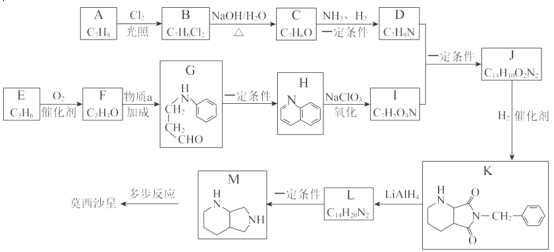
已知:+H2O
(1)A 的结构简式是__。
(2)A→B 的反应类型是__。
(3)C 中含有的官能团是__。
(4)物质 a 的分子式为 C6H7N,其分子中有__种不同化学环境的氢原子。
(5) I 能与 NaHCO3 反应生成 CO2,D+I→J 的化学方程式是__。
(6) 芳香化合物 L 的结构简式是__。
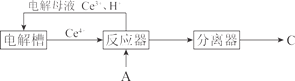
(7)还可用 A 为原料,经如下间接电化学氧化工艺流程合成 C,反应器中生成 C 的离子方程式是__。
高三化学推断题困难题查看答案及解析
叠氮化钠(NaN3)是一种应用广泛的化工产品,可用于合成抗生素头孢菌素药物的中间体,汽车安全气囊等。回答下列问题:
Ⅰ.实验室制备NaN3
水合肼(N2H4·H2O) 与亚硝酸甲酯(CH3ONO)在氢氧化钠存在下制备NaN3,其反应装置如图所示:
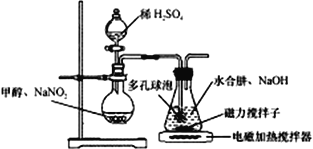
已知:2CH3OH+2NaNO2+H2SO4→2CH3ONO+ Na2SO4+2H2O; NaN3无色无味,微溶于醇、溶于水
(1)N2H4的电子式为_______________;NaN3晶体中阴离子与阳离子个数比为______________。
(2)装置中多孔球泡的作用是___________________。
(3)锥形瓶中水合肼与亚硝酸甲酯在30℃时可以反应生成叠氮酸钠、甲醇等物质,写出该反应的化学方程式_______________________________。
Ⅱ.回收甲醇
将制备反应后所得混合溶液加入烧瓶中,按照下图所示装置进行减压蒸馏。
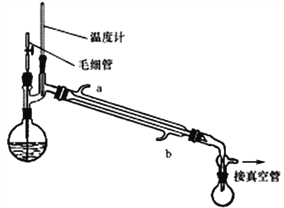
已知:
| 物质 | CH3OH | N2H4 | NaN3 |
| 沸点/℃ | 64.7 | 113.5 | 300 |
NaN3在40℃时分解
(4)实验时冷凝管中冷却水要“b进a出”原因是______________________。
(5)甲醇回收时需用减压蒸馏的原因是________________________。
(6)下列有关毛细管的作用说法正确的是_______________。
A.平衡圆底烧瓶内外压 B.作为气化中心,使蒸馏平稳
C.避免液体过热而暴沸 D.冷凝回流作用
Ⅲ.产品提取及纯度测定
将蒸馏后所得母液降温结晶,过滤得NaN3湿品;再用去离子水重结晶得NaN3产品并用碘量法测定产品纯度。取产品6.50g加入足量去离子水中溶解,并加入适量稀硫酸酸化;向混合液中加入20.00mL 1.00mol·L-lKMnO4溶液,溶液呈紫红色;再加入足量KI溶液消耗过量的KMnO4溶液;其后用0.100mol·L-lNa2S2O3标准溶液滴定所产生的I2,消耗Na2S2O3溶液30.00mL。
(7)实验所得产品的纯度为______________________。
已知:①产品中杂质不参与反应;
②测定过程中发生的反应:
10NaN3+2KMnO4+8H2SO4==2MnSO4+K2SO4+5Na2SO4+8H2O+15N2↑;
10KI+2KMnO4+8H2SO4==2MnSO4+6K2SO4+8H2O+5I2;
I2+2Na2S2O3==2NaI +Na2S4O6。
高三化学综合题困难题查看答案及解析
叠氮化钠(NaN3)是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,可用于合成抗生素头孢菌素药物的中间体、汽车安全气囊的药剂等。氨基钠(NaNH2)的熔点为210℃,沸点为400℃,在水溶液中易水解。实验室制取叠氮化钠的实验步骤及实验装置如下:
①打开止水夹K1,关闭止水夹K2,加热装置D一段时间;
②加热装置A中的金属钠,使其熔化并充分反应后,再停止加热装置D并关闭K1;
③向装置A中b容器内充入加热介质并加热到210~220℃,打开止水夹K2,通入N2O:
④冷却,向产物中加入乙醇,减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。

回答下列问题:
(1)装置B中盛放的药品为____________;装置C的主要作用是________________。
(2)氨气与熔化的钠反应生成NaNH2的化学方程式为__________。
(3)步骤③中,为了使反应受热均匀,A装置里a容器的加热方式为_____;生成NaN3的化学方程式为_____;N2O可由NH4NO3在240~245℃分解制得(硝酸铵的熔点为169.6℃),则不能选择的气体发生装置是________(填序号)。

(4)图中仪器a用的是铁质而不用玻璃,其主要原因是_____________。步骤④中用乙醚洗涤的主要目的是_______________。
(5)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:①将2.500g试样配成500.00mL溶液。②取50.00mL溶液置于锥形瓶中,加入50.00mL0.1010mol·L-1(NH4)2Ce(NO3)6溶液。③充分反应后,将溶液稍稀释,向溶液中加入8mL浓硫酸,滴入3滴邻菲啰啉指示液,用0.0500mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+消耗溶液体积为29.00mL。测定过程的反应方程式为:
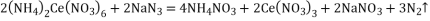
则试样中NaN3的质量分数为_______________。
高三化学实验题中等难度题查看答案及解析