-
2017年我国自主产权“全球首套煤基乙醇工业化项目”投产成功。“煤基乙醇”就是以煤为原料制备乙醇。乙醇能做燃料,可以添加到汽油中。下列说法错误的是
A. 煤制乙醇,有利于保护环境,实现能源充分利用
B. 煤制乙醇可缓解靠发酵产生乙醇导致的“与人类争粮”的局面
C. 等物质的量的乙醇、汽油完全燃烧,乙醇放出的热量多
D. 乙醇是世界公认的优良汽油添加剂,可有效改善汽油品质
高三化学选择题中等难度题查看答案及解析
-
2017 年采用中国自主知识产权的全球首套煤基乙醇工业化项目投产成功。某地用煤制乙醇的过程表示如下。

(1)Cu(NO3)2 是制备“催化剂X”的重要试剂。
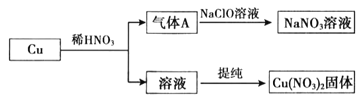
①气体A 是_________。
②实验室中用Cu( NO3)2 固体配制溶液,常加入少量稀HNO3。运用化学平衡原理简述HNO3 的作用: ________。
③NaClO溶液吸收气体A 的离子方程式是_________。
(2)过程a包括以下3个主要反应:
I.CH3COOCH3(g) +2H2(g)
C2H5OH(g) +CH3OH(g) △H1
II.CH3COOCH3(g)+C2H5OH(g)
CH3COOC2H5(g)+ CH3OH(g) △H2
III.CH3COOCH3(g) + H2(g)
CH3CHO(g) +CH3OH(g) △H3
相同时间内,测得CH3COOCH3转化率、乙醇和乙酸乙酯的选择性( 如乙醇的选择性=
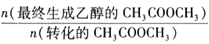 )如下图所示。
)如下图所示。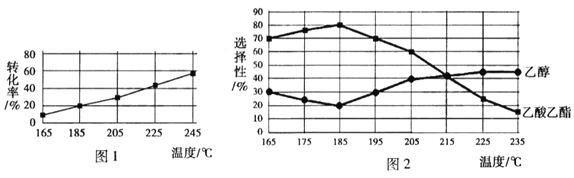
①已知:△H1< 0。随温度降低,反应I化学平衡常数的变化趋势是________。
②下列说法不合理的是_______。
A.温度可影响反应的选择性
B.225℃~235℃,反应I处于平衡状态
C.增大H2 的浓度,可以提高CH3COOCH3 的转化率
③为防止“反应III”发生,反应温度应控制的范围是____________。
④在185℃,上述反应中CH3COOCH3起始物质的量为5mol,生成乙醇的物质的量是____。
高三化学综合题中等难度题查看答案及解析
-
2017年采用中国自主知识产权的全球首套煤基乙醇工业化项目投产成功。某地煤制乙醇的过程表示如下。
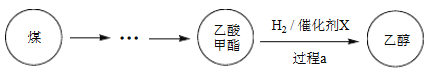
(1)Cu(NO3)2是制备“催化剂X”的重要试剂。
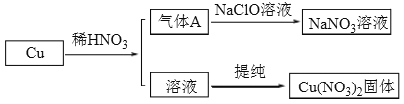
① 气体A是_______。
② 实验室用Cu(NO3)2固体配制溶液,常加入少量稀HNO3。运用化学平衡原理简述HNO3的作用_______。
③ NaClO溶液吸收气体A的离子方程式是_______。
(2)过程a包括以下3个主要反应:
Ⅰ.CH3COOCH3(g)+2H2(g)
C2H5OH(g)+CH3OH(g) ΔH1
Ⅱ.CH3COOCH3(g)+C2H5OH(g)
CH3COOC2H5 (g)+CH3OH(g) ΔH2
Ⅲ.CH3COOCH3(g)+H2(g)
CH3CHO(g)+CH3OH(g) ΔH3
相同时间内,测得CH3COOCH3转化率、乙醇和乙酸乙酯的选择性(如乙醇选择性=
 )如下图所示。
)如下图所示。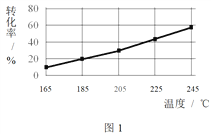

① 已知:ΔH1 < 0。随温度降低,反应Ⅰ化学平衡常数的变化趋势是_______。
② 下列说法不合理的是________。
A.温度可影响反应的选择性
B.225℃~235℃,反应Ⅰ处于平衡状态
C.增大H2的浓度,可以提高CH3COOCH3的转化率
③ 为防止“反应Ⅲ”发生,反应温度应控制的范围是_______。
④ 在185℃下,CH3COOCH3起始物质的量为5 mol,生成乙醇的物质的量是____。
高三化学综合题中等难度题查看答案及解析
-
新旧动能转换工程之一是新能源新材料的挖掘和应用。乙二醇是重要的化工原料, 煤基合成气(CO、 H2)间接制乙二醇具有转化率高、回收率高等优点,是我国一项拥有自主知识产权的世界首创技术,制备过程如下:
反应 I: 4NO(g)+4CH3OH(g)+O2(g)
4CH3ONO(g)+2H2O(g) △H1 = a kJ·mol-1
反应 II: 2CO(g)+2CH3ONO(g)
CH3OOCCOOCH3(l) + 2NO(g) △H2= b kJ·mol-1
反应 III: CH3OOCCOOCH3(1)+4H2(g)
HOCH2CH2OH(1)+2CH3OH(g) △H3= c kJ·mol-1
(1)请写出煤基合成气[n(CO): n(H2)= 1:2]与氧气间接合成乙二醇的总热化学方程式________,已知该反应在较低温条件下能自发进行,则该反应的△H ____0(填“>”“<”或“=”)。
(2)一定温度下,在 2 L 的密闭容器中投入物质的量均为 0.4mol的CO 和 CH3ONO发生反应 II,10min 达到平衡时CO的体积分数与NO的体积分数相等。
①下列选项能判断反应已达到化学平衡状态的是________。
a. CO 的质量不再变化 b. 混合气体的密度不再变化
c.单位时间内生成 CO 和 NO 的物质的量相等 d. CO 和 CH3ONO 的浓度比不再变化
②10min 内该反应的速率 ν(NO)=____________;该温度下化学平衡常数 K=_________。若此时向容器中再通入0.4 mol NO,一段时间后,达到新平衡时 NO的体积分数与原平衡时相比______(填“增大”“相等”“减小”或“不能确定”)。
③若该反应△H<0,在恒容的密闭容器中,反应达平衡后,改变某一条件,下列示意图正确的是____________(填字母)。
高三化学综合题中等难度题查看答案及解析
-
新旧动能转换工程之一是新能源新材料的挖掘和应用。乙二醇是重要的化工原料, 煤基合成气(CO、 H2)间接制乙二醇具有转化率高、回收率高等优点,是我国一项拥有自主知识产权的世界首创技术,制备过程如下:
反应 I: 4NO(g)+4CH3OH(g)+O2(g)
4CH3ONO(g)+2H2O(g) △H1 = a kJ·mol-1
反应 II: 2CO(g)+2CH3ONO(g)
CH3OOCCOOCH3(l) + 2NO(g) △H2= b kJ·mol-1
反应 III: CH3OOCCOOCH3(1)+4H2(g)
HOCH2CH2OH(1)+2CH3OH(g) △H3= c kJ·mol-1
(1)请写出煤基合成气[n(CO): n(H2)= 1:2]与氧气间接合成乙二醇的总热化学方程式________,已知该反应在较低温条件下能自发进行,则该反应的△H ____0(填“>”“<”或“=”)。
(2)一定温度下,在 2 L 的密闭容器中投入物质的量均为 0.4mol的CO 和 CH3ONO发生反应 II,10min 达到平衡时CO的体积分数与NO的体积分数相等。
①下列选项能判断反应已达到化学平衡状态的是________。
a. CO 的质量不再变化 b. 混合气体的密度不再变化
c.单位时间内生成 CO 和 NO 的物质的量相等 d. CO 和 CH3ONO 的浓度比不再变化
②10min 内该反应的速率 ν(NO)=____________;该温度下化学平衡常数 K=_________。若此时向容器中再通入0.4 mol NO,一段时间后,达到新平衡时 NO的体积分数与原平衡时相比______(填“增大”“相等”“减小”或“不能确定”)。
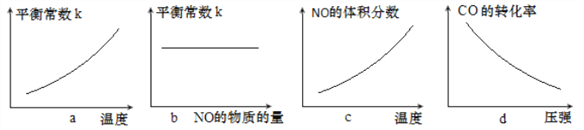
③若该反应△H<0,在恒容的密闭容器中,反应达平衡后,改变某一条件,下列示意图正确的是____________(填字母)。

高三化学综合题中等难度题查看答案及解析
-
氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车备受青睐。我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,并加快向产业化的目标迈进。氢能具有的优点包括( )
①原料来源广;②易燃烧、热值高;③储存方便;④制备工艺廉价易行
A.①② B.①③ C.③④ D.②④
高三化学选择题简单题查看答案及解析
-
氢能是一种既高效又干净的新能源,发展前景良好,用氢作能源的燃料电池汽车倍受青睐。我国拥有完全自主知识产权的氢燃料电池轿车“超越三号”,已达到世界先进水平,并加快向产业化的目标迈进。下列有关说法正确的是( )
A.氢制备工艺廉价易行,且储存方便
B.燃料电池车中能量转化率为100%
C.燃料电池车是直接将化学能转化为电能
D.利用热电厂的电能电解蒸馏水制备氢气是一种环保之举
高三化学选择题中等难度题查看答案及解析
-
我国在南海北部神弧海域进行的可燃冰试采成功,这标志着我国成为全球第一个实现了在海域可燃冰试开采中获得连续稳定产气的国家。可燃冰主要成分是甲烷,可以用作燃料和制氢原料。甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸气重整两个过程。发生的主要反应如下:
化学方程式
焓变ΔH/(kJ·mol-1)
活化能Ea/(kJ·mol-1)
甲烷氧化
CH4(g)+2O2(g)
CO2(g)+2H2O(g)
-802.6
125.6
CH4(g)+O2(g)
CO2(g)+2H2(g)
-322.0
172.5
蒸气重整
Ⅰ.CH4(g)+H2O(g)
CO(g)+3H2(g)
+206.2
240.1
Ⅱ.CH4(g)+2H2O(g)
CO2(g)+4H2(g)
+165
243.9
下列说法不正确的是
A.CO(g)+H2O(g)
CO2(g)+H2(g) ΔH=+41.2kJ·mol-1
B.反应Ⅱ逆反应活化能Ea=78.9kJ·mol-1
C.初始阶段:甲烷氧化的速率大于甲烷蒸气重整的速率
D.甲烷自热重整方法的突出优点是能量循环利用
高三化学单选题中等难度题查看答案及解析
-
随着能源危机的加剧,我国也在大力推广新一代乙醇燃料,广西是我国甘蔗产量主产区之一,乙醇可以从甘蔗中提炼加工出来,乙醇除用作燃料外,还可以用它合成其他有机物。下面是以乙醇为起始原料的转化关系,请回答相关问题。
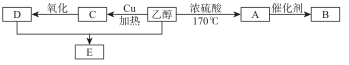
①B在日常生活中常用来作食品包装袋,但往往会带来环境问题。
写出A→B的化学方程式: 。
②写出乙醇→A的化学方程式: 。
③写出乙醇→C的化学方程式: 。
④写出E的方程式: 。
高三化学填空题中等难度题查看答案及解析
-
据报道,我国拥有完全自主产权的氢氧燃料电池车在北京奥运会期间为运动员提供服务。某种氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是( )
A. 正极反应式为:O2+2H2O+4e-===4OH-
B. 工作一段时间后,电解液中KOH的物质的量不变
C. 该燃料电池的总反应方程式为:2H2+O2===2H2O
D. 用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.1 mol电子转移
高三化学选择题中等难度题查看答案及解析