-
在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g) + O2(g) = 2CO2(g) △H ="-566" kJ/mol
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) △H ="-890" kJ/mol
由1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为( )
A.2912kJ B.2953kJ C.3236kJ D.3867kJ
高二化学选择题中等难度题查看答案及解析
-
在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g) + O2(g) = 2CO2(g);△H =-566kJ/mol
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l);△H =-890kJ/mol
由1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为( )
A.2912kJ B.2953kJ C.3236kJ D.3867kJ
高二化学选择题简单题查看答案及解析
-
在一定条件下,CH4和CH3OH的燃烧的热化学方程式分别为:
CH4(g)+2O2(g)=CO2(g) + 2H2O(g) ΔH=-890kJ/mol
CH3OH(g)+1.5O2(g)=CO2(g) + 2H2O(g) ΔH=-750kJ/mol
如果有CH4和CH3OH的混合气体充分燃烧,放出的热量为806kJ,将生成的气体通过浓硫酸,浓硫酸增重36g。则混合气体中CH4和CH3OH的体积比________。
高二化学计算题简单题查看答案及解析
-
在一定条件下,CH4和CH3OH的燃烧的热化学方程式分别为:
CH4(g)+2O2(g)=CO2(g) + 2H2O(g) ΔH=-890kJ/mol
CH3OH(g)+1.5O2(g)=CO2(g) + 2H2O(g) ΔH=-750kJ/mol
如果有CH4和CH3OH的混合气体充分燃烧,放出的热量为806kJ,将生成的气体通过浓硫酸,浓硫酸增重36g。则混合气体中CH4和CH3OH的体积比________。
高二化学填空题简单题查看答案及解析
-
在一定条件下,CO和CH4燃烧的热化学方程式分别为:( )
2CO(g) + O2(g) = 2CO2(g);△H ="-566" kJ/mol
CH4(g) + 2O2(g) = CO2(g) + 2H2O(l);△H ="-890" kJ/mol
由1molCO和3molCH4组成的混和气在上述条件下完全燃烧时,释放的热量为
A. 2912kJ B. 2953kJ C. 3236kJ D. 3867kJ
高二化学单选题中等难度题查看答案及解析
-
在一定条件下,CO和CH4燃烧的热化学方程式分别为:2CO(g)+O2(g) =2CO2(g)
H= -566 kJ/mol,CH4(== CO2(g) + 2H2O(l)
H= -890 kJ/mol, 由1molCO和3molCH4组成的混合气体在上述条件下完全燃烧时,释放的热量为
A.2912 kJ B.2953 kJ C.3236 kJ D.3867 kJ
高二化学选择题中等难度题查看答案及解析
-
在一定条件下,CH4和CO燃烧的热化学方程式分别为:
CH4(g)+2O2(g)
2H2O(l)+CO2(g) ΔH =﹣890 kJ/mol
2CO(g)+O2(g)
2CO2(g) ΔH =﹣566 kJ/mol
如果有CH4和CO的混合气体充分燃烧,放出的热量为262.9 kJ,生成的CO2用过量的饱和石灰水完全吸收,得到50g白色沉淀。则混合气体中CH4和CO的体积比为( )
A.1∶2 B.1∶3 C.2∶3 D.3∶2
高二化学单选题中等难度题查看答案及解析
-
(5分)在一定条件下,甲烷与一氧化碳的燃烧的热化学方程式分别为:
CH4(g)+2O2(g)=CO2(g)+ 2H2O(l) △H =-890kJ/mol
2CO(g) + O2(g)= 2CO2(g) △H =-566.0kJ/mol
一定量的甲烷与一氧化碳的混合气完全燃烧时,放出的热量为262.9 kJ,生成的CO2用过量的饱和石灰水完全吸收,可得到50g白色沉淀。求混合气体中甲烷和一氧化碳的体积比。
高二化学计算题中等难度题查看答案及解析
-
已知: ① CH3OH(g) + 3/2O2(g) = CO2(g) + 2H2O(g) △H= -a kJ•mol-1
② CH4(g) + 2O2(g) = CO2(g) + 2H2O(g) △H= -b kJ•mol-1
③ CH4(g) + 2O2(g) = CO2(g) + 2H2O(l) △H= -c kJ•mol-1
则下列叙述正确的是
A. 由上述热化学方程式可知b>c
B. 甲烷的燃烧热为b kJ•mol-1
C. 2CH3OH(g) = 2CH4(g) + O2(g) △H= 2(b-a) kJ•mol-1
D. 当甲醇和甲烷物质的量之比为1: 2,完全燃烧生成CO2(g)和H2O(l)时,放出的热量为Q kJ,则该混合物中甲醇的物质的量为Q/(a+2b)mol
高二化学单选题中等难度题查看答案及解析
-
下列叙述中,正确的是( )
A.甲烷的标准燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g) + 2O2(g) === CO2(g) + 2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应,放热19.3 kJ,其热化学方程式为:
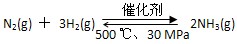 ΔH=-38.6 kJ·mol-1
ΔH=-38.6 kJ·mol-1C.相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量
D.常温下,反应C(s) + CO2(g) === 2CO(g)不能自发进行,则该反应的ΔH>0
高二化学选择题简单题查看答案及解析