-
A、B是短周期元素,最外层电子排布式分别为msx,nsxnpx+1。A与B形成的离子化合物加蒸馏水溶解后可使酚酞试液变红,同时有气体逸出,该气体可使湿润的红色石蕊试纸变蓝,则该化合物的相对分子质量是
A..38 B.55 C.100 D.135
高二化学选择题简单题查看答案及解析
-
A、B是短周期元素,最外层电子排布式分别为3s2,2s22p3。A与B形成的离子化合物加蒸馏水溶解后可使酚酞试液变红,同时有气体逸出,该气体可使湿润的红色石蕊试纸变蓝,则该化合物的分子量是
A.38 B.55 C.100 D.135
高二化学单选题简单题查看答案及解析
-
A、B、C、D、E、F六种短周期主族元素的原子序数依次增大。A是元素周期表中原子半径最小的元素;B元素的原子最外层电子数是次外层电子数的2倍;D与A能形成两种原子个数比分别为1:1和1:2的共价化合物X和Y;D还能与E形成两种原子个数比分别为1:1和1:2的离子化合物M和N;F的最高正化合价为+6。
回答下列问题:
(1)C元素的化学名称为____________,F元素的化学名称为____________。
(2)Y的电子式为____________,M中阴离子的离子符号为___________。
(3)由以上六种元素中的两种原子构成的五核10e-分子的空间构型是______________。
(4)用电子式表示化合物E2F的形成过程为____________________。
(5)D、F的简单氢化物的沸点高低为____________(用化学式表示)。
高二化学推断题困难题查看答案及解析
-
A、B、C、D、E都是短周期元素,原子序数依次增大;A原子中电子运动的轨道只有一种形状;B、C同周期,A、D同主族.D、B能形成两种离子化合物甲和乙,原子个数比分别为2:1和1:1;E元素原子的最外层电子数是其电子总数的
.根据以上信息回答下列问题:
(1)甲、乙中含有非极性键的物质的电子式是______.
(2)E、C分别形成的氢化物稳定性大小关系是______.(用氢化物的化学式作答)
(3)C和D的离子中,半径较小的是______(填离子符号).画出C和D的离子的结构示意图______,______.
(4)写出B元素基态原子的轨道表示式______.
(5)X是与E同主族的短周期元素,下表列出了X原子间各种共价键的键能:
通过计算说明X2中的______(填“σ键比π键稳定”或“π键比σ键稳定”).键类型 X-X X=X X≡X 键能(kJ/mol) 159 418 946 高二化学解答题中等难度题查看答案及解析
-
( 9分)A、B都是短周期元素,原子最外层电子排布式分别为(n+1)sx、nsx+1npx+3。A与B可形成化合物D。D溶于水时有气体逸出,该气体能使带火星的木条复燃。请回答下列问题:
(1)比较电离能:I1(A)________I1(B)(填“>”或“<”,下同),比较电负性:A________B。
(2)通常A元素的化合价是________,对A元素呈现这种价态进行解释:
①用原子结构的观点进行解释: _______________________________________。
②用电离能的观点进行解释: ___________________________________________。
③写出D跟水反应的离子方程式:_______________________________________。
高二化学填空题简单题查看答案及解析
-
(8分)A、B、C、D、E、F为原子序数依次增大的短周期元素,B、C相邻且同周期,A、D同主族。C原子最外层电子数是核外电子层数的3倍,A、C能形成两种化合物甲和乙,原子个数比分别为2∶1和1∶1,甲为常见的溶剂。E是地壳中含量最多的金属元素;F元素为同周期电负性最大的元素。D和F可形成化合物丙,E和F可形成化合物丁。G为第四周期未成对电子数最多的元素。请回答下列问题:
(1)写出G基态原子的价电子排布式 。
(2) B和C比较,第一电离能较大的是 (填元素符号),其原因为 。
(3)甲、乙两分子的中心原子的杂化类型是否相同 (相同、不相同)。
(4)已知化合物丁熔点190℃,沸点183℃。丙和丁比较,熔点较高的是 (填化学式),
(5)配合物戊由G3+与甲、元素F构成,已知该配合物的配位数为6。在含有0.1mol戊的溶液中加入AgNO3溶液至过量,经过滤、洗涤、干燥后,得到28.7g白色沉淀。,则戊的化学式为 。
高二化学填空题中等难度题查看答案及解析
-
A、B都是短周期元素,原子最外层电子排布分别为(n+1)sx、nsx+1npx+3。A与B可形成化合物C和D。D溶于水时有气体E逸出,E能使带火星的木条复燃。请回答下列问题:
(1)比较电离能:①I1(A)与I2(A)________;②I1(A)与I1(B)________;
③I1(B)与I1(He)________。
(2)通常A元素的化合价是________。(3)对A元素呈现这种价态进行解释。
①用原子结构的观点进行解释:_________________________________;
②用电离能的观点进行解释:______________________________。
③写出D跟水反应的离子方程式:______________________________。
高二化学综合题中等难度题查看答案及解析
-
短周期主族元素W、X、Y和Z的原子序数依次增大,W的气态氢化物的水溶液可使酚酞变红,W与X可形成一种红棕色有刺激性气味的气体,Y的原子半径是所有短周期主族元素中最大的,Z原子最外层电子数与W原子的电子总数相同。下列说法中正确的是( )
A. 简单氢化物沸点:Z<W B. 简单离子半径:W<X<Y
C. W的氧化物对应水化物均为强酸 D. Y与Z形成的化合物的水溶液呈碱性
高二化学单选题困难题查看答案及解析
-
短周期主族元素A、B、C、D、E原子序数依次增大,A是周期表中原子半径最小的元素,B是形成化合物种类最多的元素,C原子的最外层电子数是次外层电子数的3倍,D是同周期中金属性最强的元素,E的负一价离子与C的某种氢化物分子含有相同的电子数.
(1)A、C、D形成的化合物中含有的化学键类型为 .
(2)已知:
①E﹣E→2E△H=+a kJ•mol﹣1;
②2A→A﹣A△H=﹣b kJ•mol﹣1;
③E+A→A﹣E△H=﹣c kJ•mol﹣1;
写出298K时,A2与E2反应的热化学方程式 .
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g)⇌X(g)△H=﹣a kJ•mol﹣1(a>0,X为A、B、C三种元素组成的一种化合物).初始投料与各容器达到平衡时的有关数据如下:
实验
甲
乙
丙
初始投料
2molA2、1molBC
1molX
4molA2、2molBC
平衡时n(X)
0.5mol
n2
n3
反应的能量变化
放出Q1kJ
吸收Q2kJ
放出Q3kJ
体系的压强
P1
P2
P3
反应物的转化率
α1
α2
α3
①在该温度下,假设甲容器从反应开始到平衡所需时间为4min,则A2的平均反应速率v(A2)= .
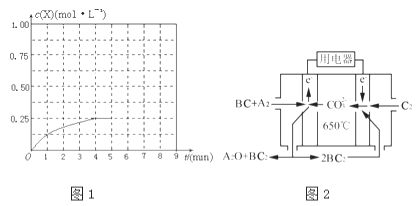
②计算该温度下此反应的平衡常数K= .
③三个容器中的反应分别达平衡时各组数据关系正确的是 (填字母).
A.α1+α2=1
B.Q1+Q2=a
C.α3<α1
D.P3<2P1=2P2
E.n2<n3<1.0mol
F.Q3=2Q1
④在其他条件不变的情况下,将甲容器的体系体积压缩到1L,若在第8min达到新的平衡时A2的总转化率为75%,请在图1中画出第5min到新平衡时X的物质的量浓度的变化曲线.
(4)熔融碳酸盐燃料电池(MCFC)是一种高温燃料电池,被称为第二代燃料电池.目前已接近商业化,示范电站规模已达2MW,从技术发展趋势来看,是未来民用发电的理想选择方案之一.现以A2(g)、BC(g)为燃料,以一定比例Li2CO3和Na2CO3低熔混合物为电解质.写出碳酸盐燃料电池(MCFC)正极电极反应式 .
高二化学填空题简单题查看答案及解析
-
C、D、G、I均为短周期元素形成的单质,D、G、I为常见非金属气态单质。D元素的原子的最外层电子数是次外层电子数的3倍,C、G同周期,且原子最外层电子数相差4,它们的简单离子电子层结构不同。相互间有如下转化关系:
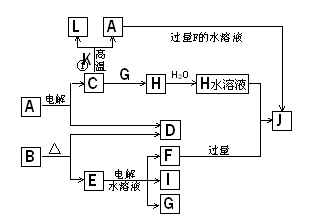
请填空:
(1) D与I能形成原子个数比为1:1的共价化合物,请写出其分子式:________;
(2)L是目前应用最广泛的金属,用碳棒作阳极,L作阴极,写出电解E水溶液的化学式:________。
(3)化合物K 中含有组成单质L的元素,且该元素的质量分数为70%。反应①的化学方程式是,引发该反应的操作是________
(4)写出A+F → J的离子方程式:________。
高二化学填空题困难题查看答案及解析