-
(12分)水是组成生命体的重要化学物质,没有水就没有生命。请回答下列问题:
(1)水分子自身作用生成含有相同电子数的阴、阳两种离子,写出此过程的方程式________;
(2)25℃时,在由水电离产生的c(H+)=1×10-14 mol·L-1的溶液中
①NH4+、Al3+、Br-、SO42- ② Na+、Mg2+、Cl-、NO3-
③K+、Ba2+、Cl-、NO3- ④K+、Na+、HCO3-、SO42-
四组离子中,一定可以大量共存的是________(填序号,下同),可能大量共存的是________,一定不能大量共存的是________;
(3)在下列反应中,水仅做氧化剂的是________(填字母,下同),水既不做氧化剂又不做还原剂的是________。
A.Cl2+H2O=HCl+HClO B.2Na2O2+2H2O=4NaOH+O2↑
C.CaH2+2H2O=Ca(OH)2+2H2↑ D.3Fe+4H2O(g) Fe3O4+4H2
Fe3O4+4H2
-
(8分)2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心。水是组成生命体的重要化学物质,有关水的反应有很多。
(1)两个水分子自身作用会生成阴、阳两种离子,其中阳离子的电子式是________。
(2)在下列反应中,水仅做氧化剂的是________ ________(填字母,下同),水既不做氧化剂又不做还原剂的是________ ________。
A.Cl2+H2O=HCl+HClO B.2Na2O2+2H2O=4NaOH+O2↑
C.CaH2+2H2O=Ca(OH)2+2H2↑ D.3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
(3)“神舟七号”飞船上的能量主要来自于太阳能和燃料电池,H2、O2和KOH的水溶液可形成氢氧燃料电池,负极的电极反应为 ,电极反应产生的水经冷凝后可作为航天员的饮用水,当得到1.8 L饮用水时,电池内转移的电子数约为________。
(4)右图是某品牌饮用矿泉水标签的部分内容。请认真阅读标签内容后计算。
①该矿泉水中镁离子的物质的量浓度的最大值是________;
②一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过________ mol。

-
(16分)2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心。水是组成生命体的重要化学物质,有关水的反应有很多。
(1)水分子自身作用会生成阴、阳两种离子,其中阳离子的电子式是________。
(2)在由水电离产生的c(H+)=1×10-14 mol·L-1的溶液中,①NH4+、Al3+、Br-、SO42-
② Na+、Mg2+、Cl-、NO3-③K+、Ba2+、Cl-、NO3- ④K+、Na+、HCO3-、SO42-四组离子中,一定可以大量共存的是(填序号,下同),可能大量共存的是________。
(3)在下列反应中,水仅做氧化剂的是________(填字母,下同),水既不做氧化剂又不做还原剂的是________。
A.Cl2+H2O=HCl+HClO
B.2Na2O2+2H2O=4NaOH+O2↑
C.CaH2+2H2O=Ca(OH)2+2H2↑
D.3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
(4)“神舟七号”飞船上的能量主要来自于太阳能和燃料电池,H2、O2和KOH的水溶液可形成氢氧燃料电池,负极的电极反应为 ,电极反应产生的水经冷凝后可作为航天员的饮用水,当得到1.8 L饮用水时,电池内转移的电子数约为________。
(5)右图是某品牌饮用矿泉水标签的部分内容。请认真阅读标签内容后计算。

①该矿泉水中镁离子的物质的量浓度的最大值是________;
②一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过________ mol。
-
水是组成生命体的重要化学物质,没有水就没有生命.2010年春,发生在滇、黔、桂、渝、川等省的严重旱情牵动了全国人民的心,再一次警示人们关注水资源.阅读下列有关水的问题并正确作答.
(1).水分子自身作用生成含有相同电子数的阴、阳两种离子,写出此过程的方程式______.
(2)25℃时,在由水电离产生的c(H+)=1×10-14 mol•L-1的溶液中,①NH4+、Al3+、Br-、SO42- ②Na+、Mg2+、Cl-、NO3-③K+、Ba2+、Cl-、NO3- ④K+、Na+、HCO3-、SO42-四组离子中,一定可以大量共存的是______(填序号,下同),可能大量共存的是______,一定不能大量共存的是______.
(3)在下列反应中,水仅做氧化剂的是______(填字母,下同),水既不做氧化剂又不做还原剂的是______.
A.Cl2+H2O=HCl+HClO B.2Na2O2+2H2O=4NaOH+O2↑
C.CaH2+2H2O=Ca(OH)2+2H2↑ D.3Fe+4H2O(g) Fe3O4+4H2.
Fe3O4+4H2.
-
(18分)水是组成生命体的重要化学物质,有关水的反应有很多。
(1)水分子的空间构型为___________;水分子自身作用会生成阴、阳两种离子,其中阴离子的电子式是___________

(2)如图是某品牌饮用矿泉水标签的部分内容。请计算一瓶合格的这种矿泉水中硫酸根离子的物质的量不能超过___________。
(3)标况下将a L氨气溶于1L水中,得到的溶液密度为b g·cm﹣3。用化学方程式表示氨气溶于水显碱性的原因___________该溶液的物质的量浓度为___________mol·L﹣1。
(4)已知M是生活中常见的一种金属,将44.8 g M完全溶于很稀的过量硝酸,向所得溶液中加入足量固体烧碱并加热,放出6.72 L(标准状况)气体。M溶于该很稀的硝酸的离子方程式为___________________。M与水在高温条件下,生成1g气体吸热a kJ,写出该反应的热化学方程式_________________________________。
(5)味精是常用的调味品,当前味精生产主要采用淀粉发酵法,其中第一步是使淀粉水解为单糖。
①淀粉发生水解反应的化学方程式是_________________________________
②实验室中检验淀粉水解产物应选用的试剂可以是___________ (填字母)·
A.NaOH溶液、氨水、AgNO3溶液 B.H2SO4溶液、氨水、AgNO3溶液
C.NaOH溶液、CuSO4溶液 D.H2SO4溶液、CuSO4溶液
-
[化学——选修3:物质结构与性质]碳是地球上组成生命的最基本的元素之一。根据要求回答下列问题:
(1)碳原子的价电子排布式______________,核外有_________种不同运动状态的电子。
(2)碳可以形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。
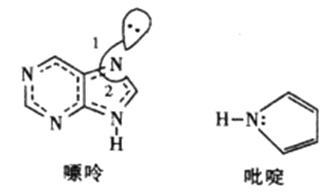
①嘌呤中所有元素的电负性由大到小的顺序__________________。
②嘌呤中轨道之间的夹角∠1比∠2大,解释原因__________________。
③吡啶结构中N原子的杂化方式__________________。
④分子中的大π键可用符号π 表示,m代表形成大π键的原子数,n代表参与形成大π键的电子数。则吡啶结构中的大π键表示为__________。
表示,m代表形成大π键的原子数,n代表参与形成大π键的电子数。则吡啶结构中的大π键表示为__________。
(3)碳元素能形成CO、CO2、H2CO3等多种无机化合物。
①二氧化碳的晶体叫做干冰,每个二氧化碳分子周围通常有__________个紧邻的分子。
②在CO转化成CO2的反应过程中,下列说法正确的是__________。
A.分子中孤电子对数不变 B.分子的极性发生变化
C.原子间成键方式发生改变 D.分子晶体的熔沸点升高
③H2CO3与H3PO4均有1个非羟基氧,H3PO4为中强酸,H2CO3为弱酸的原因_________。
(4)2017年,中外科学家团队共同合成了碳的一种新型同素异形体:T-碳。T-碳的结构是将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代形成碳的一种新型三维立方晶体结构,如下图。已知T碳晶胞参数为a pm,阿伏伽德罗常数为NA,则T碳的密度的表达式为__________g/cm3。(写出表达式即可)

-
(8分)水是生命之源,也是化学反应中的主角。试回答下列问题:
(1)写出水分子的结构式________。
(2)全部由短周期元素组成的A、B、C三种物质,是中学化学常见的有色物质,它们均 能与水发生氧化还原反应,但反应中水既不作氧化剂也不作还原剂。请写出A、B、C与水反应的化学方程式:
①A十 __________________ _______ __;
__________________ _______ __;
②B十 ________;
________;
③C十 ________。
________。
-
选做(12分)【化学——物质结构与性质】化学中的某些元素是与生命活动密不可分的元素,请回答下列问题。
(1)NH4NO3是一种重要的化学肥料,其中N原子的杂化方式是 。
(2)维生素C是一种水溶性维生素,水果和蔬菜中含量丰富,该物质结构简式如图所示。以下关于维生素C的说法正确的是 。
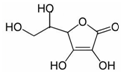
a.分子中既含有极性键又含有非极性键
b.1 mol 分子中含有4 mol π键
c.该物质的熔点可能高于NaCl
d.分子中所含元素电负性由大到小的顺序为O>C>H
(3)维生素C晶体溶于水的过程中要克服的微粒间作用力有 。
(4)KSCN溶液可用于Fe3+的检验,原因是铁离子外围有较多能量相近的空轨道,因此能与一些分子或离子形成配合物。Fe3+的价电子排布为 ,与之形成配合物的分子或离子中的配位原子应具备的结构特征是 。
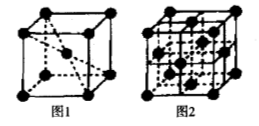
(5)1183K以下纯铁晶体的晶胞如图1所示,1183K以上则转变为图2所示晶胞,则图1和图2中,铁原子的配位数之比为 。
-
氮是生命物质的重要组成元素之一,含氮物质与人类的生活密切相关。
(1)氮原子最外层电子排布式为:_________;氮离子 核外有___种运动状态不同的电子;N4分子的空间结构如图:
核外有___种运动状态不同的电子;N4分子的空间结构如图: ,它是一种_____分子。(填“极性”或“非极性”)
,它是一种_____分子。(填“极性”或“非极性”)
(2)氨气是人工固氮的产物,它极易溶于水( ),生成NH3 · H2O。请设计实验证明NH3 · H2O是弱碱_______________________________。
),生成NH3 · H2O。请设计实验证明NH3 · H2O是弱碱_______________________________。
(3)向100mL 0.1mol/L的盐酸中通入0.02mol氨气,充分吸收后测得溶液呈碱性。则该溶液中NH3 · H2O、 、
、 三种微粒的物质的量浓度大小关系为____________。
三种微粒的物质的量浓度大小关系为____________。
(4)铵盐可用作氮肥,实验室检验铵盐中的 时,可取少量铵盐样品于试管中,加入强碱浓溶液,加热,若产生的气体能使________________________________,说明有
时,可取少量铵盐样品于试管中,加入强碱浓溶液,加热,若产生的气体能使________________________________,说明有 。
。
(5)NaN3可用于制造汽车安全气囊,当汽车遇到撞击时,NaN3能迅速分解产生Na和N2。请写出该反应的化学方程式_______________________,每生成3mol N2时,转移电子_____mol。
-
氮是生命物质的重要组成元素之一,氮的单质及其化合物性质多样,用途广泛。
(1)氮原子核外电子排布式为_________,其最外层电子共有_____种不同的伸展方向。
(2)N2分子是一种极具理论研究价值的分子,它的空间结构如图,是一种正四面体结构( ),则N4是一种_____________分子。(填“极性”或“非极性”)
),则N4是一种_____________分子。(填“极性”或“非极性”)
(3)科学家正在研究利用催化技术将超音速飞机尾气中的NO和CO转变为CO2和N2:2NO+2CO  2CO2 + N2+Q ( Q>0),该反应平衡常数K的表达式为___________;温度升高,K值________(选填“增 大”、“减小”、“不变”);若上述反应在密闭容器中发生,达到平衡时能提高NO转化率的措施之一是_____________________。
2CO2 + N2+Q ( Q>0),该反应平衡常数K的表达式为___________;温度升高,K值________(选填“增 大”、“减小”、“不变”);若上述反应在密闭容器中发生,达到平衡时能提高NO转化率的措施之一是_____________________。
(4)铁盐可用作氮肥,实验室检验铵盐中的 NH4+时,可取少量铵盐样品于试管中,加入强碱浓溶液,加热,若产生的气体能使___________________,说明有NH4+。
Fe3O4+4H2






