-
【加试题】实验室制取高纯NaI晶体(无色)可按下列步骤进行:按化学计量称取各原料,在三颈烧瓶中(如图)先加入适量的高纯水,然后按Na2CO3、I2和水合肼的投料顺序分批加入。
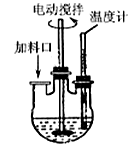
已知: I2 + Na2CO3 == NaI +NaIO +CO2↑; △H <0
3I2 + 3Na2CO3 == 5NaI +NaIO3 +3CO2↑; △H <0
I2(s) + I-(aq)  I3-(aq) ;
I3-(aq) ;
水合肼(N2H4·H2O)具有强还原性,可分别将IO-、IO3-和I2还原为I-,本身被氧化为N2(放热反应);100℃左右水合肼分解为氮气和氨气等。
(1)常温常压时,I2与Na2CO3溶液反应很慢,下列措施能够加快反应速率的是 (填字母)。
a.将碘块研成粉末 b.起始时加少量NaI
c.将溶液适当加热 d.加大高纯水的用量
(2)I2与Na2CO3溶液反应适宜温度为40~70℃,温度不宜超过70℃,除防止反应速率过快,另一个原因是 。
(3)写出水合肼氧化IO-的离子方程式 。
(4)所得溶液(偏黄,且含少量SO42-,极少量的K+和Cl-)进行脱色、提纯并结晶,可制得高纯NaI晶体。实验方案为:
①、将溶液在不断搅拌下依次加入稍过量的Ba(OH)2溶液、稍过量的Na2CO3溶液、过滤,在滤液中加少量活性炭煮沸后 (填操作名称),这样操作的目的是 。
②、溶液在不断搅拌下加入 (填试剂名称)至溶液的PH约为6,然后 (填操作名称),再次过滤,用 洗涤晶体2~3次,在真空干燥箱中干燥。
-
某小组以CoCl2·6H2O、过氧化氢、液氨、氯化铵固体为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验:
①氨的测定:精确称取wgX,加适量水溶解,注入圆底烧瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1mL c1mol·L-1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)用NaOH标准溶液滴定过剩的HCl时,应使用_______式滴定管,该滴定实验可使用的指示剂为_______,达到滴定终点的现象为____________________________
(2)样品中氨的质量分数表达式为__________________________
(3)滴定终点时,若溶液中c(Ag+)=2.0×10-5mol·L-1 ,c(CrO42-)为________mol·L-1。(已知:Ksp(Ag2CrO4)=1.12×10-12)。
-
Ⅰ、高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:在烧瓶中(装置见图)加入一定量MnO2 和水,搅拌,通入 SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤(已知MnO2+H2SO3=MnSO4+H2O)。
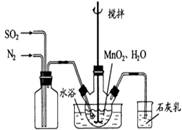
①石灰乳作用:________。
②若实验中将 换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是________。
换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如右图。导致溶液中Mn2+、SO42-浓度变化产生明显差异的原因是________。

(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿 时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH=7.7, 请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤:
[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]。
①________;
②________;
③检验SO42-是否被洗涤除去; ④用少量乙醇洗涤; ⑤低于100℃干燥。
Ⅱ、锌铝合金的主要成分有Zn、Al、Cu、Si等元素。实验室测定其中Cu含量的步骤如下:①称取该合金样品1.1g,用HCl和H2O2溶解后,煮沸除去过量H2O2,过滤,滤液定容于250mL容量瓶中。
②用移液管移取50.00mL滤液于250mL碘量瓶中,控制溶液的pH=3~4,加入过量KI溶液(生成CuI和I2)和指示剂,用0.01100mol×L-1Na2S2O3溶液滴定生成的I2至终点(反应:I2 + 2S2O32- = 2I- + S4O62-),消耗Na2S2O3溶液6.45mL。
(1)判断步骤②滴定终点的方法是。
(2)计算合金中Cu的质量分数________。
-
丙烯酸甲酯是一种重要的工业原料,某实验小组制取丙烯酸甲酯的装置如图所示。

Ⅰ.实验步骤如下:
①向三颈瓶中依次加入:10.0 mL丙烯酸(CH2=CHCOOH)、适量的浓硫酸、10.0 mL无水甲醇、2粒沸石,按图示装置连接好冷凝管,用搅拌棒搅拌,水浴加热。
②充分反应后,冷却,向混合液中加入5% Na2CO3溶液洗至中性。
③分液,取上层油状液体,再用无水Na2SO4干燥后蒸馏,收集70℃~90℃馏分。
可能用到的信息:
| 密度 | 沸点 | 溶解性 | |
| 丙烯酸 | 1.05 g/cm3 | 141℃ | 与水互溶,易溶于有机溶剂 | 有毒 |
| 甲醇 | 0.79 g/cm3 | 64.7℃ | 与水互溶,易溶于有机溶剂 | 易挥发,有毒 |
| 丙烯酸甲酯 | 0.95 g/cm3 | 80.5℃ | 难溶于水,易溶于有机溶剂 | 易挥发 |
请回答下列问题:
(1)仪器c的名称是______。
(2)混合液用5% Na2CO3溶液洗涤的作用是________。
(3)该实验中应采用的安全防护措施有_______。(1条即可)
Ⅱ.为测定上述反应中丙烯酸甲酯的产率,设计如下实验:
①将油状物质提纯后平均分成5份,取出1份置于锥形瓶中,加入2.5 mol/L的KOH溶液10.0 mL,加热使之完全水解。
②用酚酞做指示剂,向冷却后的溶液中滴加0.5 mol/L的HCl溶液,中和过量的KOH,滴到终点时共消耗盐酸20.00 mL。
(4)请写出(Ⅱ)操作①中发生的化学反应方程式____________。
(5)计算本次酯化反应丙烯酸甲酯的产率_______________。
-
Ⅰ.某小组以CoCl2·6H2O、过氧化氢、液氨、氯化铵固体为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进行如下实验:
①氨的测定:精确称取wgX,加适量水溶解,注入圆底烧瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1mL c1mol·L-1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L-1 NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不在消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)用NaOH标准溶液滴定过剩的HCl时,应使用___式滴定管,该滴定实验可使用的指示剂为___,达到滴定终点的现象为___。
(2)样品中氨的质量分数表达式为___。
(3)滴定终点时,若溶液中c(Ag+)=2.0×10-5mol·L-1 ,c(CrO42-)为___mol·L-1。(已知:Ksp(Ag2CrO4)=1.12×10-12)。
Ⅱ.已知
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
(4)则用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入稀硫酸和双氧水,溶解,铁变为___加入___调节pH为___(保留两位有效数字),铁刚好完全沉淀(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全)。
-
为了测定草酸晶体H2C2O4·xH2O中的x值,某实验小组进行实验,步骤如下:
①称取1.260 g草酸晶体,配成100 mL溶液。
②取25.00 mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000 mol/L的KMnO4溶液滴定H2C2O4溶液,当__________________时,滴定结束。
④记录数据,重复实验。整理数据如:
| 实验序号 | V(KMnO4溶液) |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 1 | 0.10 | 10.00 |
| 2 | 1.10 | 11.10 |
| 3 | 1.50 | 11.50 |
回答下列问题:
(1)步骤①需使用烧杯、量筒、玻璃棒,还缺少的玻璃仪器为______________(填名称);步骤③滴定过程中,盛装KMnO4溶液的仪器为_______________(填名称)。
(2)该反应原理的化学方程式为_____________________________________________。
(3)请将步骤③补充完整_____________________________________________________。
(4)根据数据,计算H2C2O4溶液的物质的量浓度为_________mol/L,x=________。
(5)若滴定终点读数时俯视KMnO4溶液液面,则x值会_________(填“偏大”“偏小”或“无影响”)。
-
为了测定草酸晶体H2C2O4·xH2O中的x值,某实验小组进行实验,步骤如下:
①称取1.260g草酸晶体,配成100mL溶液。
②取25.00mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000mol/L的KMnO4溶液滴定H2C2O4溶液,当 _____________时,滴定结束。
④记录数据,重复实验。整理数据如下:
| 实验序号 | V(KMnO4溶液) |
| 滴定前刻度/mL | 滴定后刻度/mL |
| 1 | 0.10 | 10.00 |
| 2 | 1.10 | 11.10 |
| 3 | 1.50 | 13.50 |
| 4 | 0.70 | 10.80 |
回答下列问题:
(1)步骤①需要使用烧杯、量筒、玻璃棒,还缺少的玻璃仪器为_______(填名称);步骤③滴定过程中,盛装KMnO4溶液的仪器为__________________(填名称)。
(2)该反应原理的离子方程式为___________________________________;
(3)请将步骤③补充完整_________________________________________;
(4)根据数据,计算H2C2O4溶液的物质的量浓度为______mol/L,x=____________;
(5)若滴定终点读数时俯视液面,则x值会________(填“偏大”、“偏小”或“无影响”)。
-
在苹果、香蕉等水果的果香中存在着乙酸正丁酯。某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯。实验步骤如下:
(一)乙酸正丁酯的制备
①在干燥的50mL圆底烧瓶中,加入13.5mL(0.15mol)正丁醇和7.2mL(0.125mol)冰醋酸,再加入3~4滴浓硫酸,摇匀,投入1~2粒沸石。
按下图所示安装带分水器的回流反应装置,并在分水器中预先加入水,使水面略低于分水器的支管口。
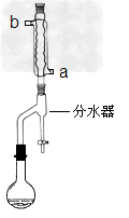
②打开冷凝水,圆底烧瓶在石棉网上用小火加热。在反应过程中,通过分水器下部的旋塞不断分出生成的水,注意保持分水器中水层液面原来的高度,使油层尽量回到圆底烧瓶中。反应达到终点后,停止加热,记录分出的水的体积。
(二)产品的精制
③将分水器分出的酯层和反应液一起倒入分液漏斗中,先用10 mL的水洗涤,
再继续用10 mL10%Na2CO3洗涤至中性,再用10 mL 的水洗涤,最后将
有机层转移至锥形瓶中,再用无水硫酸镁干燥。
④将干燥后的乙酸正丁酯滤入50 mL 烧瓶中,常压蒸馏,收集124~126℃的
馏分,得11.6g产品。
(1)写出该制备反应的化学方程式_______________。
(2)冷水应该从冷凝管___________(填a或b)管口通入。
(3)步骤②中不断从分水器下部分出生成的水的目的是__________________。步骤②中判断反应终点的依据是_______。
(4)产品的精制过程步骤③中,洗的目的是______________________。两次洗涤完成后将有机层从分液漏斗的__________置入锥形瓶中。
-
在苹果、香蕉等水果的果香中存在着乙酸正丁酯。某化学课外兴趣小组欲以乙酸和正丁醇为原料合成乙酸正丁酯。实验步骤如下:
(一)乙酸正丁酯的制备
①在50mL 圆底烧瓶中,加入0.15mol正丁醇和 0.12mol 冰醋酸,再加入3~4滴浓硫酸,摇匀,投入1~2粒沸石。按如图所示安装带分水器的回流反应装置, 并在分水器中预先加入水,使水面略低于分水器的支管口。
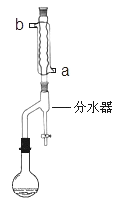
②打开冷凝水,圆底烧瓶在石棉网上用小火加热。在反应过程中,通过分水器下部的旋塞不断分出生成的水,注意保持分水器中水层液面原来的高度,使油层尽量回到圆底烧瓶中。反应达到终点后,停止加热,记录分出的水的体积。
(二)产品的精制
③将分水器分出的酯层和反应液一起倒入分液漏斗中,用 10 mL 的水洗涤。有机层继续用10 mL10% Na2CO3 洗涤至中性,再用 10 mL 的水洗涤,最后将有机层转移至锥形瓶中,再用无水硫酸镁干燥。
④将干燥后的乙酸正丁酯滤入50 mL 烧瓶中,常压蒸馏,收集 124~126 ℃的馏分,得11.6g产品。
(1)冷水应该从冷凝管_____(填 a 或 b)管口通入。
(2)步骤②中不断从分水器下部分出生成的水的目的是_____。
(3)下列关于分液漏斗的使用叙述正确的是_____。
a.分液漏斗使用前必须要检漏,只要分液漏斗的旋塞芯处不漏水即可使用
b.分液时乙酸正丁酯应从上口倒出
c.萃取振荡操作应如图所示
d.放出液体时,需将玻璃塞打开或使塞上的凹槽对准漏斗口上的小孔
(4)该实验过程中,生成乙酸正丁酯(相对分子质量 116)的产率是_____。
-
某化学实验小组以电镀废渣(Cr2O3、CuO、Fe2O3及CaO)为原料制取铜粉和K2Cr2O7。主要流程如图:

(1)加入适量Na2S溶液后生成的沉淀X为___,若加入的Na2S溶液过量,除生成X外还会发生反应的离子方程式为___。
(2)请配平[Cu(NH3)4]SO4·H2O加热发生分解反应的化学方程式。
___[Cu(NH3)4]SO4·H2O ___Cu+___NH3↑+___SO2↑+___N2↑+___H2O
___Cu+___NH3↑+___SO2↑+___N2↑+___H2O
(3)“沉CuNH4SO3”时可用如图装置(夹持、加热仪器略):
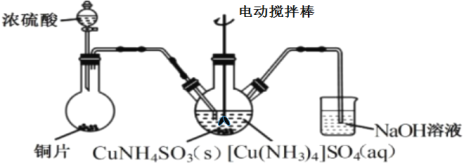
①“沉CuNH4SO3”时,反应温度需控制在45℃,合适的加热方式是___。
②NaOH溶液的作用是___。
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.0g配成250mL溶液,取出25.00mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000mol/L硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行三次实验。(已知Cr2O72-被还原为Cr3+)
①若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为20.00mL,则所得产品K2Cr2O7的纯度为___%。
②上述流程中K2Cr2O7发生氧化还原反应后所得溶液中除含有Cr3+,还含有一定浓度的Fe3+,可通过调pH的方法使两者转化为沉淀。假设两种离子初始浓度均为2×10-3mo/L,当溶液中刚开始析出Cr(OH)3沉淀时,c(Fe3+)=___mo/L。{已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31}

I3-(aq) ;







