-
(14分)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)
氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
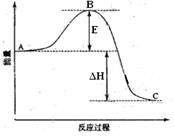
(1)图中A、C分别表示________、________,E的大小对该反应的反应热有无影响?________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________,理由是________;
(2)图中△H =________KJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,身被还原为四价钒化合物;四价钒化合物
再被氧气氧化。写出该催化循环机理的化学方程式________;
(4)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=________mol·L-1·min-1、υ(SO3)=________mol·L-1·min-1;
(5)已知单质硫的燃烧热为296 KJ·mol-1,则由S(s)生成3 molSO3(g)的△H = ________。
-
已知2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示.请回答下列问题:
2SO3(g)反应过程的能量变化如图所示.请回答下列问题:

(1)1molSO2(g)氧化为1molSO3(g)放出的热量为99.00kJ•mol﹣1,写出该反应的热化学方程式 .
(2)①在图中标出该反应的活化能E和反应热△H;
②该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低,请在图中画图表示出来,并进行必要的标注.
(3)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是 .
A.容器中气体总压强不变
B.容器中混合气体的密度不变
C.每生成1mol SO3的同时生成1molSO2
D.SO2、O2、SO3的物质的量之比为2:1:2
(4)在400℃,常压下,向体积为2L的密闭容器中充入2mol SO2(g)和1.92mol O2(g),充分反应后,测得还有0.08mol SO2剩余,求该反应的平衡常数(要求写出计算过程).
-
(共14分) 2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:
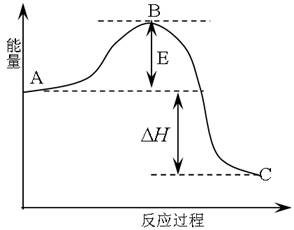
(1)图中A、C分别表示________、________,E的大小对该反应的反应热有无影响?(填“有影响”或“无影响”)________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________,理由是________;
(2)图中△H=________KJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式________;
(4)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)= ________ mol·L-1·min-1、υ(SO3)=________ mol·L-1·min-1;
(5)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H________ (要求计算过程)。
-
(15分)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH=-99kJ·mol-1.请回答下列问题:
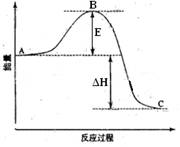
(1)图中A、C分别表示________、________,E的大小对该反应的反应热有无影响________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低________,理由是________;
(2)图中△H=________ KJ·mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式;
(4)如果反应速率υ(SO2)为0.05 mol·L-1·min-1,则υ(O2)=________mol·L-1·min-1
(5)已知单质硫的燃烧热为296 KJ·mol-1,计算由S(s)生成3 molSO3(g)的△H________(要求计算过程)。
-
(一)(6分)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH=-99kJ·mol-1.请回答下列问题:

(1)图中E的大小对该反应的反应热有无影响?________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________
 (2)已知单质硫16g燃烧放热为149 KJ写出硫燃烧热的热化学方程式: ________
(2)已知单质硫16g燃烧放热为149 KJ写出硫燃烧热的热化学方程式: ________
(3) 计算由S(s)生成3 molSO3(g)的△H
计算由S(s)生成3 molSO3(g)的△H
(二)(6分)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子。制取铁酸钠的化学方程式如下:
__Fe(NO3)3 +__ NaOH+ __Cl2 → __Na2FeO4+ __NaNO3 + __NaCl + __H2O
(1)配平上述反应,当生成3mol还原产物时,转移电子的总数为________mol;
(2)铁酸钠除了能消毒外,还可以用于净水,原因是
-
2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
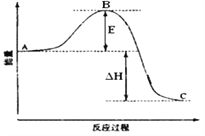
已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99kJ·mol-1。请回答下列问题:
(1)图中E的大小对该反应的反应热________(填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点___________ (填“升高”还是“降低”)。
(2)完成SO2氧化为SO3的热化学方程式______________________________________。
(3)铝元素在人体中积累可使人慢性中毒,1989年世界卫生组织正式将铝确定为食品污染源之一而加以控制。铝及其化合物在下列场合使用时必须严格加以控制的是________(填字母)
A.用明矾净水 B.制电线电缆 C.制包糖果用的铝箔 D.制防锈油漆
(4)铝在空气中会被氧化生成一层致密的氧化膜(氧化物)而对铝起保护作用,但这层氧化膜(氧化物)遇到强酸或强碱都会溶解,请写出氧化膜与氢氧化钠溶液反应的化学方程式:_____________________
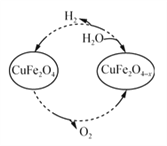
(5)用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O可制H2,其物质转化如图所示。写出其中氧缺位铁酸铜(CuFe2O4-x)与水反应的化学方程式:_____________。
-
2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3(g)的ΔH= —99kJ·mol-1。请回答下列问题:
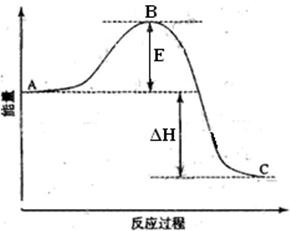
(1)图中A、C分别表示、,E的大小对该反应的反应热________(填“有”或“无”)影响。该反应通常用V2O5作催化剂,加V2O5会使图中B点(填“升高”还是“降低”),△H________(填“变大”、“变小”或“不变”),理由是。
(2)图中△H=________KJ·mol-1。
-
2SO2(g)+O2(g)⇌2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=-99kJ•mol-1.
请回答下列问题:
(1)图中A、C分别表示______、______,E的大小对该反应的反应热有无影响?______.该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?______,理由是______;
(2)图中△H=______kJ•mol-1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化.写出该催化循环机理的化学方程式______;
(4)如果反应速率υ(SO2)为0.05mol•L-1•min-1,则υ(O2)=______mol•L-1•min-1、υ(SO3)=______mol•L-1•min-1;
(5)已知单质硫的燃烧热为296kJ•mol-1,计算由S(s)生成3molSO3(g)的△H______(要求计算过程).

-
(16分)已知2SO2(g)十O2(g) 2SO3(g)反应过程的能量变化如图所示。
2SO3(g)反应过程的能量变化如图所示。
请回答下列问题:
(1)1mol SO2(g)氧化为1mol SO3(g)放出的热量为99.00kJ·mol-1,写出该反应的热化学方程式 。
(2)①在图中标出该反应的活化能E和反应热△H;
②该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低,请在图中画图表示出来,并进行必要的标注。
(3)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是 。
A.容器中气体总压强不变 B.容器中混合气体的密度不变
C.每生成1mol SO3的同时生成1molSO2 D.SO2、O2、SO3的物质的量之比为2∶1∶2
(4)在400℃,常压下,向体积为2L的密闭容器中充入2mol SO2(g)和1.92mol O2(g),充分反应后,测得还有0.08mol SO2剩余,求该反应的平衡常数(要求写出计算过程)。
-
(12分)2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH= —99kJ·mol—1.请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1mol SO3的ΔH= —99kJ·mol—1.请回答下列问题:
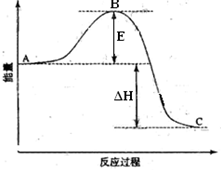
(1)图中A点表示________ 。E的大小对该反应的反应热有无影响?________。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?________,理由是________;
(2)图中△H=________KJ·mol—1;
(3)V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化。写出该催化循环机理的化学方程式
________,________ 。










