-
纯碱(Na2CO3)在生产生活中具有广泛的用途。
Ⅰ.以下是实验室模拟制碱原理制取Na2CO3的流程图。
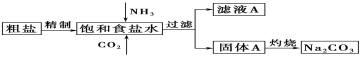
下表是四种物质在100g水中不同温度的溶解度
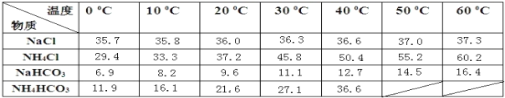
(1)粗盐中含有的杂质离子有Ca2+、Mg2+、SO42-等。精制除杂的步骤顺序是a→________→________→________→b(填字母编号)。
a.粗盐溶解,滤去沉渣 b.加入盐酸调pH c.加入Ba(OH)2溶液
d.加入Na2CO3溶液 e.过滤
(2)向饱和食盐水中先通入_______,后通入________,生成固体A的化学方程式为____
Ⅱ.制得的碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案.请回答下列有关问题:
方案一:把6g样品溶解后加入过量的CaCl2溶液,将所得沉淀过滤、洗涤、烘干后得到5g固体。
(3)洗涤沉淀的具体操作是_____________________________。
(4)根据实验中测得的有关数据,计算纯碱样品Na2CO3的质量分数为___________(结果保留小数点后一位)。
方案二:利用下图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去)。
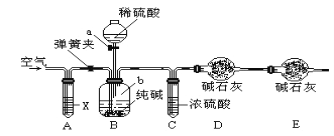
已知:碱石灰为氢氧化钠和氧化钙的混合物。
(5)实验开始前应进行的操作是______________________________。
(6)仪器a的名称为___________________,装置A中试剂X应选用_________________。
(7)装置E的作用是_________________________________。
-
NaCl在生活、生产和科研中都有广泛的用途。
I. 从海水中提取的粗盐含有Ca2+、Mg2+、SO4-等离子,为制备精盐可使用以下四种试剂:①Na2CO3溶液 ②BaCl2溶液 ③NaOH溶液 ④盐酸(用于沉淀的试剂均稍过量)。
(1)加入试剂的合理顺序是________(填选项)。
a. ①②③④ b. ③①②④ c. ②①③④ d. ③②①④
(2)加入过量Na2CO3溶液的作用是________________。
II. 实验室要配制100 mL 0.2 mol·L-1 NaCl溶液。
(1)用托盘天平称氯化钠固体的质量是________g。
(2)配制溶液需要使用的主要玻璃仪器有烧杯、玻璃棒、胶头滴管和________。
(3)下列操作中,可能造成所配制溶液的浓度偏低的是________(填选项)。
a. 没有洗涤烧杯和玻璃棒 b. 定容时,俯视刻度线
c. 洗涤后的容量瓶中残留少量蒸馏水
-
NaCl在生活、生产和科研中都有广泛的用途。
I.从海水中提取的粗盐含有Ca2+、Mg2+、SO42-等离子,为制备精盐可使用以下四种试剂:①Na2CO3溶液②BaCl2溶液③NaOH溶液④盐酸(用于沉淀的试剂均稍过量)。加入试剂的合理顺序是__________(填选项)。
A.①②③④ B.③①②④ C.②①③④ D.③②①④
II.实验室要配制100 mL 0.2 mol/L NaCl溶液。
(1)用托盘天平称氯化钠固体的质量是________g。
(2)配制溶液需要使用的主要玻璃仪器有烧杯、玻璃棒、胶头滴管和___________。
(3)下列操作中,可能造成所配制溶液的浓度偏低的是________(填选项)
a.没有洗涤烧杯和玻璃棒b.定容时,俯视刻度线
c.洗涤后的容量瓶中残留少量蒸馏水
-
硫酸在生产生活中有广泛的用途,试回答下列回题:
(1)用浓硫酸在竹简表面“刻字”是利用浓硫酸的________性。
(2)工业上制取硫酸铜常采用铜与稀硫酸混合,通入空气并进行加热,请写出该反应的化学方程式_____________________;不采用铜跟浓硫酸反应来制取硫酸铜的原因是__________________________________。
(3)一定量的锌与含 a mol H2SO4的浓溶液充分反应后,锌完全溶解,同时收集到SO2与H2的混合气体bL(标准状况)。将反应后的溶液稀释至1L,测得溶液中c(H+)为 c mol/L,则混合物中SO2物质的量为______mol。
-
金属及其化合物在生产中用途广泛。
I.CuSO4·5H2O的制取
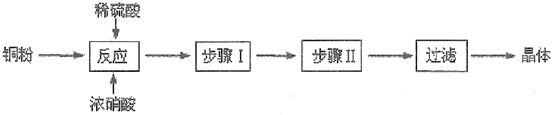
(1)向含铜粉的稀硫酸中滴加少量稀硝酸(可加热),铜粉溶解时可以观察到的实验现象:____。
(2)根据反应原理,硝酸与硫酸的理论配比(物质的量之比)为__________。
(3)步骤I、步骤II的操作名称分别是____、_____。
II.利用生产硼砂的废渣硼镁泥(主要成分为MgCO3、SiO2,还含有少量Fe2O3、MnO等)为主要原料制取轻质碳酸镁[MgCO3·Mg(OH)2·2H2O]的工业流程如下:
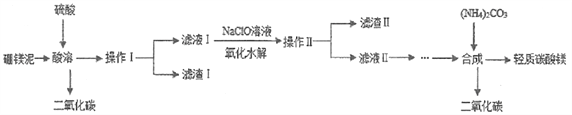
(4)实验室进行操作I、操作II所需的玻璃仪器有烧杯、______。滤渣I的成分是_____。
(5)写出“酸溶”一步中,MgCO3和硫酸反应的离子方程式__________。
(6)滤渣2的主要成分有MnO2和Fe(OH)3,写出生成MnO2的离子方程式_________。
(7)“合成”时需通蒸汽至80℃,边加热边搅拌,温度不能超80℃的原因是_________。
-
硫酸铝是一种具有广泛用途的重要化工产品,以高岭土(含SiO2、A12O3、少量Fe2O3 等)为原料制备硫酸铝晶体[Al2(SO4)3·18H2O]的实验流程如图所示。
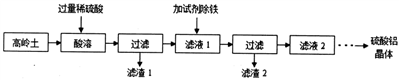
回答以下问题
(1)高岭土需进行粉粹,粉粹的目的是_____________________。
(2)滤渣1经过处理可作为制备水玻璃(Na2SiO3水溶液)的原料,写出滤渣1与烧碱溶液反应的化学方程式____________________________________。
(3)加入试剂除铁前,滤液1中的阳离子除了Al3+、Fe3+外还有的阳离子是__________(填离子符号)。滤渣2主要成分为Fe(OH)3,由于条件控制不当,常使Fe(OH)3 中混有Al(OH)3影响其回收利用,用离子方程式表示除去A1(OH)3的原理____________________________________________。
(4)检验滤液2中是否含有Fe3+的实验方法是(要求写出实验步骤和现象):__________________。
(5)要从滤液2获取硫酸铝晶体需要经过多步处理,其中从溶液中得到晶体的方法是__________(填标号)。
a.蒸发结晶 b.蒸发浓缩、冷却结晶
(6)某兴趣小组为了测定晶体中Al2(SO4)3·18H2O(M=666g·mol-1)的质量分数,进行如下实验:
①准确称取l.00g晶体样品,溶于一定量水中;
②滴入0.100 mol·L-1 EDTA溶液,与Al3+反应所消耗EDTA溶液的体积25.00 mL。 (已知:EDTA与Al3+以物质的量之比1∶1反应,假设杂质不与EDTA反应)则晶体中Al2(SO4)3·18H2O的质量分数是__________;若样品中的杂质离子能与EDTA反应,所测定质量分数将会__________(填“偏高”、“偏低”或“无影响”)。
-
NaHCO3和Na2CO3是常见的钠盐,下列对它们的俗名、分类和用途描述不正确的是( )
A.NaHCO3可做治疗胃酸过多的药剂 B.Na2CO3俗名纯碱,属于碱
C.Na2CO3可用于清洗餐具上的油污 D.NaHCO3可用于泡沫灭火器
-
化学在生活中应用广泛,下列物质性质与对应用途错误的是
A. 明矾易水解生成胶体,可用作净水剂
B. 晶体硅熔点高硬度大,可用作芯片
C. NaClO具有强氧化性,可作织物漂白剂
D. 硅胶具有优良的吸附性,且无毒,可作袋装食品和瓶装药品的干燥剂
-
硅及其化合物在生产生活中具有广泛的用途。
(1)工业生产粗硅的化学反应方程式为:SiO2+2C Si(粗硅)+2CO↑。该反应中,被还原的元素是___,还原剂是___(填化学式),若转移1mol电子则生成的CO在标准状况下的体积为___L。
Si(粗硅)+2CO↑。该反应中,被还原的元素是___,还原剂是___(填化学式),若转移1mol电子则生成的CO在标准状况下的体积为___L。
(2)由粗硅制纯硅的过程为:
Ⅰ.粗硅与氯气反应生成四氯化硅(SiCl4);
Ⅱ.在高温下用氢气还原四氯化硅得到纯硅。Ⅱ所发生反应的化学方程式为___。
-
化学在生活中应用广泛,下列物质性质与对应用途错误的是
A.明矾易水解生成胶体,可用作净水剂
B.晶体硅熔点高硬度大,可用作芯片
C.NaClO具有强氧化性,可作织物漂白剂
D.硅胶具有优良的吸附性,且无毒,可作袋装食品和瓶装药品的干燥剂





