-
(1)某反应中反应物与生成物有:FeSO4、Fe2(SO4)3、CuSO4、Cu。将上述反应设计成的原电池如图(1)所示,请回答下列问题:
①溶液X是____________溶液;
②Cu电极上发生的电极反应式为__________________________________________;
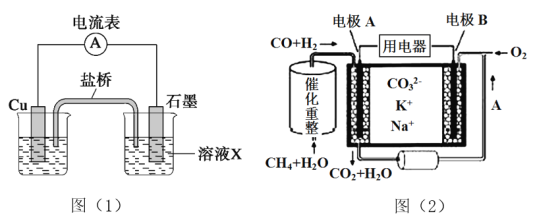
(2)一种熔融碳酸盐燃料电池原理示意如图(2)。
①电极A上CO参与的电极反应式为______________________________。
②电极B处除了通O2外,还需通入的物质A为__________。
③电池工作时,电池内部CO32-的物质的量__________(填“增大”、“减少”或“不变”)。
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O Na2FeO4+3H2↑。高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为_______________________________________。
Na2FeO4+3H2↑。高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为_______________________________________。
-
某合作学习小组的同学利用下列氧化还原反应设计 原电池:2KMnO4 + 10FeSO4 + 8H2SO4=2MnSO4 + 5Fe2(SO4)3+K2SO4+8H2O,盐桥中装有饱和K2SO4溶液。下列叙述中正确的是
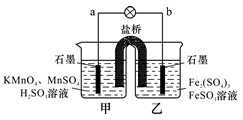
A.乙烧杯中发生还原反应
B.甲烧杯中溶液的pH逐渐减小
C.电池工作时,盐桥中的SO42-移向甲烧杯
D.外电路的电流方向是从a到b
-
根据反应KMnO4+FeSO4+H2SO4→MnSO4+Fe2(SO4)3+K2SO4+H2O(未配平)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。下列说法不正确的是( )
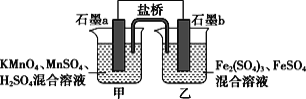
A.石墨b是原电池的负极,发生氧化反应
B.忽略溶液体积变化,Fe2(SO4)3浓度变为1.5 mol/L,则反应中转移的电子为0.1 mol
C.甲烧杯中的电极反应式:MnO4-+5e-+8H+=Mn2++4H2O
D.电池工作时,盐桥中的K+向甲烧杯中移动
-
工业上,常用Fe2(SO4)3溶液作腐蚀液,腐蚀铜质电路板得到废液主要成分是FeSO4和CuSO4,含少量Fe2(SO4)3。某小组设计装置从废液中提取铜,如图:

已知:Fe2+失电子能力比OH-强。下列说法正确的是
A. 电解初期阴极没有铜析出,原因是2H+ + 2e- = H2↑
B. 石墨极的电极反应式为2H2O + 4e- = 4H+ + O2↑
C. 若将废液2充入阳极室时可再生腐蚀液(硫酸铁溶液)
D. 若电路中转移2mol电子,理论上有2molM从交换膜左侧向右侧迁移
-
工业上,常用Fe2(SO4)3溶液作腐蚀液,腐蚀铜质电路板得到废液主要成分是FeSO4和CuSO4,含少量Fe2(SO4)3。某学习小组设计装置从废液中提取铜,如图所示。已知:Fe2+失电子能力比OH- 强。下列说法正确的是

A. 电解初期阴极没有铜析出,原因是2H++2e-=H2↑
B. 石墨极的电极反应式为2H2O+4e-=4H++O2↑
C. 若电路中转移2mol电子,理论上有2molM从交换膜左侧向右侧迁移
D. 若将废液2充入阳极室时可再生腐蚀液(硫酸铁溶液)
-
工业上,常用Fe2(SO4)3溶液作腐蚀液,腐蚀铜质电路板得到废液主要成分是FeSO4和CuSO4,含少量Fe2(SO4)3。某学习小组设计装置从废液中提取铜,如图所示。已知:Fe2+失电子能力比OH- 强。下列说法正确的是

A. 电解初期阴极没有铜析出,原因是2H++2e-=H2↑
B. 石墨极的电极反应式为2H2O+4e-=4H++O2↑
C. 若电路中转移2mol电子,理论上有2molM从交换膜左侧向右侧迁移
D. 若将废液2充入阳极室时可再生腐蚀液(硫酸铁溶液)
-
在氧化还原反应中,氧化过程和还原过程是同时发生的两个半反应.Cu2O-2e-+2H+═2Cu2++H2O是一个半反应式.下列五种物质FeSO4、Fe2(SO4)3、CuSO4、Na2CO3、KI中的一种能使上述半反应顺利发生.
(1)写出并配平该氧化还原反应的离子方程式:________.
(2)向(1)中反应后的溶液里加入酸性高锰酸钾溶液,得还原产物Mn2+(无色),反应的离子方程式为________;判断Cu2+、MnO-、Fe3+的氧化性由强到弱的顺序是________(用离子符号表示).
(3)某同学用上述原理测定一种含Cu2O的矿石中Cu2O的质量分数:称量5.0g矿石溶于足量的硫酸铁和硫酸的混合溶液中,充分反应后,用酸性高锰酸钾溶液滴定,消耗0.100 0mol•L-1的高锰酸钾溶液的体积为100.00mL.
①滴定时,滴定终点的颜色为________.
②该同学测得矿石样品中Cu2O的质量分数为________.
③下列情况使测定结果一定偏高的是________.
A.开始和终点都是仰视读数
B.没有用待装液润洗滴定管
C.称量时,砝码与样品放反了
D.样品中含有较强还原性杂质
E.高锰酸钾溶液中含有
F.用酸性高锰酸钾溶液润洗锥形瓶.
-
请根据:Fe+CuSO4=FeSO4+Cu设计成一个原电池.
(1)该电池的负极材料为________,其电极反应式为________.
(2)正极发生________反应(填“氧化”或“还原”),其电极反应式为________.
(3)如果开始的时候两个电极的质量相等,如果过一段时间后两电极的质量相差1.2g,那么该电路中通过的电子的物质的量为________mol.
-
某同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如图所示原电池,盐桥中装有饱和K2SO4溶液。下列说法正确的是
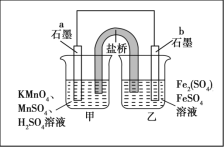
A.b电极上发生还原反应
B.外电路电子的流向是从a到b
C.电池工作时,盐桥中的SO42-移向甲烧杯
D.a电极上发生的反应为MnO4-+8H++5e-=Mn2++4H2O
-
某一反应体系中有反应物和生成物共6种:HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe2(SO4)3,已知反应前在溶液中滴加KSCN溶液呈血红色,反应后红色消失。则该反应中的氧化剂和氧化产物分别是
A.SnCl4、Fe2(SO4)3 B.Fe2(SO4)3、SnCl4
C.SnCl2、FeSO4 D.HCl、H2SO4

Na2FeO4+3H2↑。高铁酸钠生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为_______________________________________。





