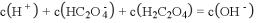-
草酸( )广泛存在于食品中,人们对其及相关产品进行了深入研究。
)广泛存在于食品中,人们对其及相关产品进行了深入研究。
(1)已知 时,
时, :
: ,
, 溶液显酸性。解释
溶液显酸性。解释 溶液显酸性的原因:______;(用化学用语并配以必要文字说明)
溶液显酸性的原因:______;(用化学用语并配以必要文字说明)
(2)已知反应: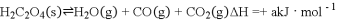 ,为了使草酸分解,通过
,为了使草酸分解,通过 燃烧反应提供能量:
燃烧反应提供能量: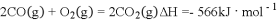 ,已知分解的草酸与所需空气(其中氧气的体分数为
,已知分解的草酸与所需空气(其中氧气的体分数为 )的物质的量之比为
)的物质的量之比为 ,则
,则 ______
______
(3)草酸分解生成的 燃料燃烧不足以提供足够的能量,还可通过甲烷来制备
燃料燃烧不足以提供足够的能量,还可通过甲烷来制备 。在密闭容器中通入物质的量浓度均为
。在密闭容器中通入物质的量浓度均为 的
的 和
和 ;在一定条件下发生反应
;在一定条件下发生反应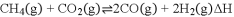 ,测得
,测得 的平衡转化率与温度、压强的关系如下图1所示。
的平衡转化率与温度、压强的关系如下图1所示。
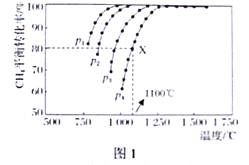
①由图判断压强 、
、 、
、 、
、 由小到大的顺序为:______;该反应的
由小到大的顺序为:______;该反应的 ______0(填“<”“>”“=”):
______0(填“<”“>”“=”):
② 该反应的平衡常数为______(结果保留两位小数)
该反应的平衡常数为______(结果保留两位小数)
(4)常温下,向 的
的 溶液中逐滴加入
溶液中逐滴加入
 溶液,所得滴定曲线如图所示。下列说法正确的是______
溶液,所得滴定曲线如图所示。下列说法正确的是______

① 点时:
点时: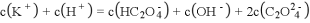
② 点时:
点时:
③ 点时:
点时: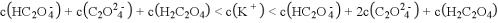
④ 点时:
点时: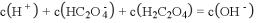
-
“中和滴定原理在实际生产生活中应用广泛某化学学习小组同学的研究课题是:探究测定草酸晶体(H2C2O4·xH2O)中的x值。通过查阅资和网络查寻,得知草酸易溶于水,其水溶液可以用酸性KMnO4溶液进行滴定,反应原理为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
回答下列问题:
(1)该滴定实验所需的玻璃仪器有______。
A.酸式滴定管(50mL) B.碱式滴定管(50mL) C.量筒(50mL) D.锥形瓶 E.烧杯
(2)滴定终点的现象为_____________________________________________________。
(3)某学生根据3次实验分别记录有关数据如下表:
| 滴定次数 | 待测H2C2O4溶液的体积/mL | 0.100mol·L-1KMnO4的体积/mL |
| 滴定前刻度 | 滴定后刻度 | 滴液体积/mL |
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据上表数据列式计算该H2C2O4溶液的物质的量浓度______________。(计算结果保留四位有效数字)
(4)讨论:若滴定到终点时俯视滴定管刻度线读数,则由此测得的x值会______________(填“偏大”、“偏小”或“不变”)。
-
向草酸(H2C2O4)溶液中逐滴加入酸性高锰酸钾溶液时,溶液褪色总是先慢后快。对其原因,某研究性学习小组结合化学反应原理提出猜想与假设,并设计了一系列实验进行探究:
实验(1):在两支试管中分别加入10mL等浓度的草酸溶液,在②号试管中加入少量硫酸锰固体。然后在两支试管中分别加入5滴0.1 mol·L-1的硫酸酸化高锰酸钾溶液。现象如下(表1)
| ①号试管 | ②号试管 |
| 加入药品 | 草酸溶液 硫酸酸化高锰酸钾溶液 | 草酸溶液 硫酸酸化高锰酸钾溶液 硫酸锰固体 |
| 实验现象(褪色时间) | 溶液褪色很慢(30s) | 溶液褪色很快(2s) |
实验(2):在两支试管中分别加入5 mL等浓度的草酸溶液,在②号试管中再滴加10滴稀硫酸,然后各加入5滴0.1 mol·L-1的高锰酸钾溶液。现象如下(表2)
| 编号 | ①号试管 | ②号试管 |
| 褪色时间 现象 | 100 s | 90 s |
| 均有气泡产生;②号试管的溶液褪色比①号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
实验(3):取3支试管分别加入5 mL等浓度草酸溶液,然后在①、②、③号试管中依次加入10滴、1 mL、2 mL稀硫酸溶液,各加入5滴0.1 mol·L-1的高锰酸钾溶液,然后置于温度为65℃的水浴中加热。观察现象(表3)。
| 编号 | ①号试管 | ②号试管 | ③号试管 |
| 褪色时间 实验现象 | 80 s | 100 s | 120 s |
| 均有气泡产生;①号试管的溶液褪色比②、③号试管的溶液快,它们颜色变化如下:紫红色→红色→橙红色→橙色→黄色→无色。 |
(1) 该研究性学习小组的实验目的是________。
(2)该研究性学习小组进行实验时所用的方法是科学实验中常用的一种方法,该方法叫________法;
(3)实验(1)得出的结论是________。
(4)由实验(2)和实验(3)得出的结论是(写三点)
_________________________,_____________________,_______________;
(5)据有关现象写出草酸溶液与酸性高锰酸钾溶液反应的离子方程式:
________H2C2O4+________MnO4—+ ________ ________=________Mn2++ ________ ________+ ________H2O
-
某同学进行影响草酸与酸性高锰酸钾溶液反应速率因素的研究。草酸与酸性高锰酸钾的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。室温下,实验数据如下:
| 实验序号 | ① | ② | ③ |
| 加入试剂 | 0.01mol/L KMnO4 0.1mol/L H2C2O4 | 0.01mol/L KMnO4 0.1mol/L H2C2O4 MnSO4固体 | 0.01mol/L KMnO4 0.1mol/L H2C2O4 Na2SO4固体 |
| 褪色时间/s | 116 | 6 | 117 |
请回答:
(1)该实验结论是________。
(2)还可以控制变量,研究哪些因素对该反应速率的影响________。
(3)进行上述三个实验后,该同学进行反思,认为实验①的现象可以证明上述结论。请你写出实验①的现象并分析产生该现象的原因________。
(4)实验②选用MnSO4固体而不是MnCl2固体的原因是_________。
-
结合所学内容,回答下列问题:
Ⅰ.某同学进行影响草酸与酸性高锰酸钾溶液反应速率因素的研究。草酸与酸性高锰酸钾的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。室温下,两支试管分别编号①和②,实验数据如下:
| 实验序号 | ① | ② |
| 加入试剂 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的MnSO4固体 |
| 褪色时间/s | 116 | 6 |
试管①中KMnO4溶液褪色的速率开始十分缓慢,一段时间后突然加快。
请回答:
(1)该实验结论是___________________________________________________________。
(2)实验②选用MnSO4固体而不是MnCl2固体的原因是____________________________。
(3)该同学为使实验更加严密,在试管③中做了如下实验,请预测褪色时间约为_____。
| 实验序号 | ③ |
| 加入试剂 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的Na2SO4固体 |
| 褪色时间/s | |
Ⅱ.滴定法是一种重要的定量分析方法,应用范围很广。某地市场上销售的一种食用精制盐包装袋上有如下部分说明:
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾(KIO3)、抗结剂 |
| 碘含量(以I计) | 20~50 mg·kg-1 |
已知:IO3-+5I-+6H+ = 3I2+3H2O,I2+2S2O32- = 2I-+S4O62-某学生拟测定食用精制盐的碘含量,其步骤为
a.准确称取W g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.加入指示剂,逐滴加入物质的量浓度为2.0×10-3 mol·L-1的Na2S2O3溶液10.0 mL,恰好反应完全
(4)c中加入的指示剂可选用_________,恰好完全反应时的现象是_______________。
(5)若操作b在空气中振荡时间过长,则最终测定的测定食用精制盐中的的碘含量会__________(填“偏高”、“偏低”或“没有影响”)。
(6)根据以上实验和包装说明,算得所测食用精制盐的碘含量是(以含W的代数式表示)________mg·kg-1(计算结果保留整数即可)。
-
结合所学内容,回答下列问题:
Ⅰ.某同学进行影响草酸与酸性高锰酸钾溶液反应速率因素的研究。草酸与酸性高锰酸钾的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。室温下,两支试管分别编号①和②,实验数据如下:
| 实验序号 | ① | ② |
| 加入试剂 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的MnSO4固体 |
| 褪色时间/s | 116 | 6 |
试管①中KMnO4溶液褪色的速率开始十分缓慢,一段时间后突然加快。
请回答:
(1)该实验结论是___________________________________________________________。
(2)实验②选用MnSO4固体而不是MnCl2固体的原因是____________________________。
(3)该同学为使实验更加严密,在试管③中做了如下实验,请预测褪色时间约为_____。
| 实验序号 | ③ |
| 加入试剂 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的Na2SO4固体 |
| 褪色时间/s | |
Ⅱ.滴定法是一种重要的定量分析方法,应用范围很广。某地市场上销售的一种食用精制盐包装袋上有如下部分说明:
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾(KIO3)、抗结剂 |
| 碘含量(以I计) | 20~50 mg·kg-1 |
已知:IO3-+5I-+6H+ = 3I2+3H2O,I2+2S2O32- = 2I-+S4O62-某学生拟测定食用精制盐的碘含量,其步骤为
a.准确称取W g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.加入指示剂,逐滴加入物质的量浓度为2.0×10-3 mol·L-1的Na2S2O3溶液10.0 mL,恰好反应完全
(4)c中加入的指示剂可选用_________,恰好完全反应时的现象是_______________。
(5)若操作b在空气中振荡时间过长,则最终测定的测定食用精制盐中的的碘含量会__________(填“偏高”、“偏低”或“没有影响”)。
(6)根据以上实验和包装说明,算得所测食用精制盐的碘含量是(以含W的代数式表示)________mg·kg-1(计算结果保留整数即可)。
-
结合所学内容,回答下列问题:
Ⅰ.某同学进行影响草酸与酸性高锰酸钾溶液反应速率因素的研究。草酸与酸性高锰酸钾的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。室温下,两支试管分别编号①和②,实验数据如下:
| 实验序号 | ① | ② |
| 加入试剂 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的MnSO4固体 |
| 褪色时间/s | 116 | 6 |
试管①中KMnO4溶液褪色的速率开始十分缓慢,一段时间后突然加快。
请回答:
(1)该实验结论是___________________________________________________________。
(2)实验②选用MnSO4固体而不是MnCl2固体的原因是____________________________。
(3)该同学为使实验更加严密,在试管③中做了如下实验,请预测褪色时间约为_____。
| 实验序号 | ③ |
| 加入试剂 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的Na2SO4固体 |
| 褪色时间/s | |
Ⅱ.滴定法是一种重要的定量分析方法,应用范围很广。某地市场上销售的一种食用精制盐包装袋上有如下部分说明:
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾(KIO3)、抗结剂 |
| 碘含量(以I计) | 20~50 mg·kg-1 |
已知:IO3-+5I-+6H+ = 3I2+3H2O,I2+2S2O32- = 2I-+S4O62-某学生拟测定食用精制盐的碘含量,其步骤为
a.准确称取W g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.加入指示剂,逐滴加入物质的量浓度为2.0×10-3 mol·L-1的Na2S2O3溶液10.0 mL,恰好反应完全
(4)c中加入的指示剂可选用_________,恰好完全反应时的现象是_______________。
(5)若操作b在空气中振荡时间过长,则最终测定的测定食用精制盐中的的碘含量会__________(填“偏高”、“偏低”或“没有影响”)。
(6)根据以上实验和包装说明,算得所测食用精制盐的碘含量是(以含W的代数式表示)________mg·kg-1(计算结果保留整数即可)。
-
某化学学习小组的研究课题是:探究测定草酸晶体(H2C2O4•xH2O)中x的值。该组同学通过查阅资料查寻得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
学习小组的同学设计了滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③用浓度为0.1000 mol/L的酸性KMnO4标准溶液进行滴定,达到终点时消耗了10.00mL。
请回答下列问题:
(1)配制100.00 mL待测液时,使用的玻璃仪器除烧杯、玻璃棒及胶头滴管外,还需要 。
(2)滴定时,将酸性KMnO4标准液装在如图中的 (填“甲”或“乙”)滴定管中。本实验滴定达到终点的标志是 。

(3)通过上述数据,求得x= 。
(4)讨论:
①若滴定终点时俯视滴定管,则由此测得的x值会 (填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会 。
-
结合所学内容,回答下列问题:
Ⅰ.某同学进行影响草酸与酸性高锰酸钾溶液反应速率因素的研究。室温下,两支试管分别编号①和②,实验数据如下:
| 实验序号 | ① | ② | ③ |
| 加入试剂 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的MnSO4固体 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的Na2SO4固体 |
| 褪色时间/s | 116 | 6 | |
试管①中KMnO4溶液褪色的速率开始十分缓慢,一段时间后突然加快。
请回答:
(1)草酸与酸性高锰酸钾的反应的离子方程式为:__________________________________
(2)实验①②结论是___________________________________________________________。
(3)实验②选用MnSO4固体而不是MnCl2固体的原因是____________________________。
(4)该同学为使实验更加严密,在试管③中做了如下实验,请预测褪色时间约为________。
Ⅱ.滴定法是一种重要的定量分析方法,应用范围很广。某地市场上销售的一种食用精制盐包装袋上有如下部分说明:
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾(KIO3)、抗结剂 |
| 碘含量(以I计) | 20~50 mg·kg-1 |
已知:IO3-+5I-+6H+ = 3I2+3H2O,I2+2S2O32- = 2I-+S4O62-某学生拟测定食用精制盐的碘含量,其步骤为
a.准确称取W g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.加入指示剂,逐滴加入物质的量浓度为2.0×10-3 mol·L-1的Na2S2O3溶液10.0 mL,恰好反应完全
(5)c中加入的指示剂可选用_________,恰好完全反应时的现象是_______________。
(6))若操作b在空气中振荡时间过长,则最终测定的测定食用精制盐中的的碘含量会__________(填“偏高”、“偏低”或“没有影响”)。
(7)根据以上实验和包装说明,算得所测食用精制盐的碘含量是(以含W的代数式表示)_____mg·kg-1(计算结果保留整数即可)。
-
某小组同学的研究课题是测定草酸晶体(H2C2O4·xH2O)中的x 值。查阅资料得,草酸[M(H2C2O4)=90g/mol] 易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2 ↑+8H2O。学习小组同学设计滴定法测定x值。
①称取1.260g纯草酸晶体,将其配制成100mL水溶液的待测液。
②取25mL 待测液放入锥形瓶中,再加入适量的稀硫酸。
③用浓度为0.100mol/L的KMnO4标准液进行滴定,达到终点时消耗10.00mL。
(1)滴定时,将酸性KMnO4溶液装在_______ (酸式或碱式) 漓定管中。
(2)本实验滴定达到终点的标志是_________________。
(3)通过上述数据,求得x=___________________。
讨论:
①滴定终点时俯视滴定管刻度,则由此测得的x值会______(填“偏大”“偏小”“不变”,下同。)
②若滴定时所用的酸性高锰酸钾溶液因久置而导致浓度变小,则由此测得的x值会___________。
)广泛存在于食品中,人们对其及相关产品进行了深入研究。
时,
:
,
溶液显酸性。解释
溶液显酸性的原因:______;(用化学用语并配以必要文字说明)
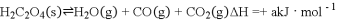 ,为了使草酸分解,通过
,为了使草酸分解,通过燃烧反应提供能量:
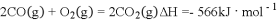 ,已知分解的草酸与所需空气(其中氧气的体分数为
,已知分解的草酸与所需空气(其中氧气的体分数为)的物质的量之比为
,则
______
燃料燃烧不足以提供足够的能量,还可通过甲烷来制备
。在密闭容器中通入物质的量浓度均为
的
和
;在一定条件下发生反应
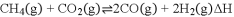 ,测得
,测得的平衡转化率与温度、压强的关系如下图1所示。

、
、
、
由小到大的顺序为:______;该反应的
______0(填“<”“>”“=”):
该反应的平衡常数为______(结果保留两位小数)
的
溶液中逐滴加入
溶液,所得滴定曲线如图所示。下列说法正确的是______
点时:
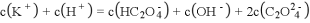
点时:

点时:
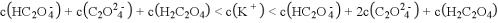
点时: