-
工业上常通过高温分解FeSO4的方法制备较为纯净的Fe2O3,其反应方程式为:2FeSO4  Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
为了检验FeSO4高温分解的产物,进行如下实验:
①取少量FeSO4高温分解得到的固体,先加入一定量稀盐酸使固体完全溶解,再向所得溶液中适量的KSCN溶液,观察溶液颜色的变化以检验Fe3+是否存在。
②将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2 和SO3
请回答下列问题:
(1)写出能说明FeSO4发生分解的现象__________________________________;
(2)写出KSCN溶液与Fe3+反应的离子方程式:_________________;
(3)实验②中,气体通过BaCl2时可以观察到的现象__________________________,产生该现象所对应的化学反应为___________________________________(用一个化学反应方程式表示);
(4)实验②中最后要将通过品红溶液的气体通入NaOH溶液中,其目的是________________________。

-
(1)工业上通过高温分解FeSO4的方法制备Fe2O3,化学方程式为:2FeSO4  Fe2O3+ SO3↑ + SO2↑为检验FeSO4高温分解的产物,进行如下实验:
Fe2O3+ SO3↑ + SO2↑为检验FeSO4高温分解的产物,进行如下实验:
检验FeSO4高温分解产生的气体,将FeSO4高温分解产生的气体通入下图装置中。

① 装置A试管可选用的试剂是_________(填标号)。
a. 水 b. BaCl2溶液 c. Ba(NO3)2溶液 d. Ba(OH)2溶液
② 装置C的作用是防止尾气污染环境,试管中应加入的试剂是_________________。
③ 若装置B试管中溶液改为酸性KMnO4溶液,可以观察到溶液紫色褪去,反应的离子方程式为__________________________ 。
(2)工业上在一定温度和催化剂条件下用NH3将NO2还原生成N2,某同学在实验室中对NH3与NO2反应进行了探究。

①实验室可以用A、B或C装置制取氨气,如果用C装置,则该装置中烧瓶所盛放的试剂为________(写名称);反应的化学方程式是_____________________;
② 预收集一瓶干燥的氨气,选择下图中的装置,其气体收集和尾气处理装置连接顺序依次为:发生装置→_____________________(用字母表示)

③ 将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按下图装置进行实验。打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中,Y管观察到的实验现象是____________________ ,反应的化学方程式为 ______________________________。

-
工业上常通过高温分解FeSO4的方法制备Fe2O3,其化学方程式为:2FeSO4 Fe2O3+SO2↑+SO3↑为检验FeSO4高温分解的产物,进行如下实验
Fe2O3+SO2↑+SO3↑为检验FeSO4高温分解的产物,进行如下实验
(1)检验产物Fe2O3取少量FeSO4高温分解得到的固体,加入一定量__________溶解,再向该溶液中加入适量的__________溶液,如有____________现象产生,则证明产物中存在Fe2O3
(2)检验气体产物:将FeSO4高温分解产生的气体通入下图三个装置中,以检验产生的气体中是否含有SO2、SO3。
①三个装量的连接序为_______________(填装置序号)
②实验中如观察到装置A中品红溶液______,装置B BaCl2溶液中__________,则可证明FeSO4高温分解产生的气体中含有SO2、SO3。
③装置C中NaOH溶液的作用是_______________(用离子方程式表示〕。

-
工业上常通过高温分解FeSO4的方法制备Fe2O3,其化学方程式为:2FeSO4 Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的产物,进行如下实验:
Fe2O3+SO2↑+SO3↑。为检验FeSO4高温分解的产物,进行如下实验:
①取少量FeSO4高温分解得到的固体,加一定量稀盐酸溶解,向该溶液中加入适量的KSCN溶液,观察溶液颜色的变化以检验Fe3+是否存在。
②将FeSO4高温分解产生的气体通入如图所示的装置中,以检验产生的气体中是否含有SO2、SO3。
请回答下列问题:

(1)写出KSCN溶液与Fe3+反应的离子方程式:____。
(2)操作②中观察到的现象和结论是____;_____。
(3)操作②中最后要将通过品红溶液的气体通入NaOH溶液中的原因是___,有关反应的离子方程式____。
-
工业上常通过高温分解FeSO4的方法制备Fe2O3,其化学方程式为:2FeSO4 Fe2O3+ SO2↑+SO3↑为检验FeSO4高温分解的产物,进行如下实验:
Fe2O3+ SO2↑+SO3↑为检验FeSO4高温分解的产物,进行如下实验:
(1)取少量分解得到的固体加入稀盐酸溶解,为检验溶液中是否有Fe3+,下列试剂或药品中最合适的是 (填序号),加入该试剂后可观察的现象为 。
A.稀盐酸 B.氯气 C.KSCN溶液 D.氯化铜溶液
(2)将高温分解产生的气体通入下图所示装置中,以检验产生的气体成分。
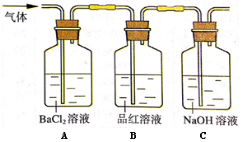
请回答下列问题:
①若在装置A中,观察到有白色沉淀生成,则该沉淀为 ,表明有 气体存在。
②装置C中的NaOH溶液的作用是 。
-
工业上常通过高温分解FeSO4的方法制备Fe2O3,其化学方程式为:2FeSO4 Fe2O3+ SO2↑+SO3↑为检验FeSO4高温分解的产物,进行如下实验:
Fe2O3+ SO2↑+SO3↑为检验FeSO4高温分解的产物,进行如下实验:
(1)取少量分解得到的固体加入稀盐酸溶解,为检验溶液中是否有Fe3+,下列试剂或药品中最合适的是 (填序号),加入该试剂后可观察的现象为 。
A.稀盐酸 B.氯气 C.KSCN溶液 D.氯化铜溶液
(2)将高温分解产生的气体通入下图所示装置中,以检验产生的气体成分。
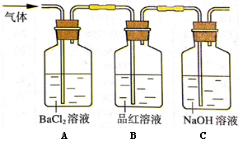
请回答下列问题:
①若在装置A中,观察到有白色沉淀生成,则该沉淀为 ,表明有 气体存在。
②装置C中的NaOH溶液的作用是 。
-
硫酸亚铁在高温下分解的方程式为:2FeSO4  Fe2O3+SO2↑+SO3↑。若将反应所得的气体混合物通入BaCl2溶液(已知SO3+ H2O ═H2SO4),将得到
Fe2O3+SO2↑+SO3↑。若将反应所得的气体混合物通入BaCl2溶液(已知SO3+ H2O ═H2SO4),将得到
A.BaSO3与BaSO4沉淀 B. BaSO3沉淀
C.BaSO4沉淀 D.无法得到沉淀物
-
工业上用固体硫酸亚铁制取颜料铁红(Fe2O3),反应原理是:
2FeSO4 Fe2O3 + SO2↑+SO3↑,某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、(II)x溶液、(III)NaOH溶液的三个装置。则下列对该方案的评价中正确的是( )
A.(I)中会生成BaSO3、BaSO4两种沉淀
B.可将(I)中的BaCl2溶液改为Ba(NO3)2溶液
C.(III)的作用是检验生成的SO2气体
D.(II)所盛x应为品红溶液
-
高温下硫酸亚铁发生反应2FeSO4  Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀是
Fe2O3+SO2↑+SO3↑,若将生成的气体通入氯化钡溶液中,得到的沉淀是
A. BaS B. BaSO3 C. BaSO4 D. BaSO3和BaSO4
-
绿矾在高温下易分解,用右图装置检验绿矾的分解产物(加热装置已略去)。化学方程式为:2FeSO4·7H2O Fe2O3+SO2↑+SO3↑+14H2O。二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃。其中b为干燥的试管。下列有关说法不正确的是
Fe2O3+SO2↑+SO3↑+14H2O。二氧化硫的沸点为-10℃,三氧化硫的沸点为44.8℃。其中b为干燥的试管。下列有关说法不正确的是
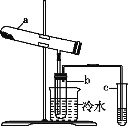
A. SO2是还原产物,Fe2O3是氧化产物
B. b中所得到的硫酸的质量分数理论上为29.5%
C. 将反应后的气体通入氯化钡溶液中,产生的沉淀为BaSO3、BaSO4
D. 将反应后的气体通入硝酸钡溶液中,产生的沉淀为只有BaSO4
Fe2O3+SO2↑+SO3↑









