铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+Fe2++Cr3+。下列说法一定正确的是
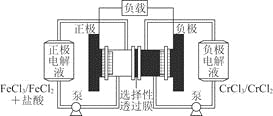
A. 充电时,阴极的电极反应式为Cr3++e-=Cr2+
B. 电池放电时,负极的电极反应式为Fe2+-e-=Fe3+
C. 电池放电时,Cl-从负极室穿过选择性透过膜移向正极室
D. 放电时,电路中每流过0.1 mol电子,Fe3+浓度降低0.1 mol·L-1
高二化学单选题中等难度题
铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+Fe2++Cr3+。下列说法一定正确的是

A. 充电时,阴极的电极反应式为Cr3++e-=Cr2+
B. 电池放电时,负极的电极反应式为Fe2+-e-=Fe3+
C. 电池放电时,Cl-从负极室穿过选择性透过膜移向正极室
D. 放电时,电路中每流过0.1 mol电子,Fe3+浓度降低0.1 mol·L-1
高二化学单选题中等难度题
铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+Fe2++Cr3+。下列说法一定正确的是

A. 充电时,阴极的电极反应式为Cr3++e-=Cr2+
B. 电池放电时,负极的电极反应式为Fe2+-e-=Fe3+
C. 电池放电时,Cl-从负极室穿过选择性透过膜移向正极室
D. 放电时,电路中每流过0.1 mol电子,Fe3+浓度降低0.1 mol·L-1
高二化学单选题中等难度题查看答案及解析
铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+Fe2++Cr3+。下列说法正确的是
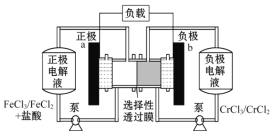
A. 电池充电时,b极的电极反应式为Cr3++e-=Cr2+
B. 电池充电时,Cl-从a极穿过选择性透过膜移向b极
C. 电池放电时,a极的电极反应式为Fe3++3e-=Fe
D. 电池放电时,电路中每通过0. 1 mol电子,Fe3+浓度降低0. 1 mol·L-1
高二化学单选题中等难度题查看答案及解析
铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+Fe2++Cr3+。下列说法正确的是( )
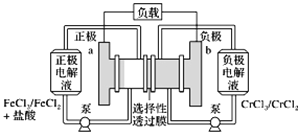
A. 电池放电时,a极的电极反应式为Fe3++3e−===Fe
B. 电池放电时,电路中每通过0.1 mol电子,Fe3+浓度降低0.1 mol·L−1
C. 电池充电时,Cl−从a极穿过选择性透过膜移向b极
D. 电池充电时,b极的电极反应式为Cr3++e−===Cr2+
高二化学单选题中等难度题查看答案及解析
铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如下图所示,工作原理为: 。下列说法正确的是
。下列说法正确的是

A. 电池放电时,电路中每通过电子,
浓度降低
B. 电池充电时,从a极穿过选择性透过膜移向b极
C. 电池放电时,a极的电极反应式为
D. 电池充电时,b极的电极反应式为
高二化学单选题中等难度题查看答案及解析
铁氧体(Fe3O4)法是处理含废铬水的常用方法,其原理是用FeSO4把废水中Cr2O还原为Cr3+,并通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或Fe2O3•FeO)的复合氧化物(
)。CrxFe2-xO3•FeO处理含1molCr2O
废水至少需要加入amolFeSO4•7H2O。下列结论正确的是( )
A.x=0.5,a=10 B.x=1,a=5 C.x=2,a=l0 D.x=0.5,a=8
高二化学单选题中等难度题查看答案及解析
(1)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的Fe2+含量,请写出酸性条件下K2Cr2O7与Fe2+反应的离子方程式_________(K2Cr2O7被还原为Cr3+)。
(2)若需配制浓度为0.010 00 mol·L-1的K2Cr2O7标准溶液250 mL,应准确称取K2Cr2O7________ g(保留四位有效数字,已知M(K2Cr2O7)=294.0 g·mol-1)。配制该标准溶液时,下列仪器一定不会用到的有________。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤250mL容量瓶 ⑥胶头滴管 ⑦托盘天平
(3)若配制K2Cr2O7标准溶液时,俯视刻度线,则测定结果________(填“偏大”、“偏小”或“不变”,下同);滴定操作中,若滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则滴定结果将____________________________。
(4)用0.010 00 mol·L-1的K2Cr2O7溶液滴定20.00 mL未知浓度的含Fe2+的溶液。恰好完全反应时消耗10.00 mL K2Cr2O7溶液,则溶液中Fe2+的物质的量浓度是多少?_________________。
高二化学实验题中等难度题查看答案及解析
铁氧体(Fe3O4)法是处理含铬废水的常用方法。其原理是用FeSO4把废水中Cr2O72-离子还原为Cr3+离子,并通过调节废水pH,使生成物组成符合类似于铁氧体(Fe3O4或FeO·Fe2O3)的复合氧化物·
。若处理含1 mol Cr2O72-的废水至少需要加入10mol FeSO4·7H2O,则
A.x=1,y=4,z=6 B.x=0.5,y=1.5,z=8.5
C.x=2,y=4,z=6 D.x=2,y=6,z=4
高二化学选择题简单题查看答案及解析
将3.48克Fe3O4完全溶解在100mL1mol/LH2SO4中,然后加入K2Cr2O7溶液25mL,恰好使溶液中Fe2+全部转化为成Fe3+, Cr2O72-离子全部还原为Cr3+。则K2Cr2O7溶液的摩尔浓度为
A.0.05mol/L B.1.0mol/L C.0.2mol/L D.0.3mol/L
高二化学选择题中等难度题查看答案及解析
全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如图所示。下列说法不正确的是


A.放电过程中右槽溶液颜色逐渐由紫色变为绿色
B.放电过程中氢离子的作用之一是参与正极反应
C.充电过程中左槽溶液逐渐由蓝变黄
D.充电时若转移的电子数为3.011023个,左槽溶液中n(H+)的变化量为1mol
高二化学单选题中等难度题查看答案及解析
微生物燃料电池可净化废水,同时还能获得能源或有价值的化学产品,图1为其工作原理,图2为废水中Cr2O72-离子浓度与去除率的关系。下列说法正确的是
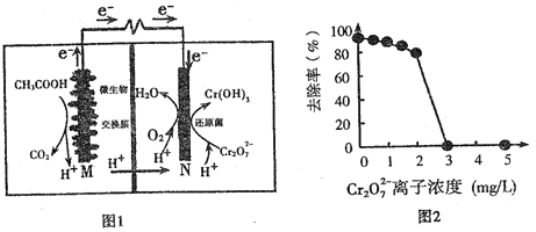
A.M为电池正极,CH3COOH被还原
B.外电路转移4mol电子时,M 极产生22.4LCO2
C.反应一段时间后,N极附近的溶液pH下降
D.Cr2O72-离子浓度较大时,可能会造成还原菌失活
高二化学单选题中等难度题查看答案及解析