-
反应2A⇌B+D在四种不同条件下进行,B、D起始浓度为零,A的浓度(mol•L-1)随反应时间(min)的变化情况如下表:
| 实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
下列说法正确的是
A.在实验1,反应在10至20分钟时间内物质A的平均速率为0.013mol/(L•min)
B.在实验2,A的初始浓度c2>1.0mol•L-1
C.设实验3的反应速率为v3,实验1的反应速率为v1,则v3<v1
D.实验4中,该反应在30min后才达到平衡状态
-
某化学反应2A(g)  B(g) + D(g)在四种不同的条件下进行,B、D起始浓度为0,反应物A的浓度随反应时间的变化情况如下表:
B(g) + D(g)在四种不同的条件下进行,B、D起始浓度为0,反应物A的浓度随反应时间的变化情况如下表:
| 实验序号 | | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| (1) | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| (2) | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| (3) | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| (4) | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,下列说法错误的是
A. 在(1)中,反应在10~20 min内A的平均速率为0.013 mol/(L·min)
B. 在(2)中,A的初始浓度c2<1.0 mol/L
C. 设(3)的反应速率为υ3,(1)的反应速率为υ1,则υ3 > υ1
D. 比较(1)和(4),可推测该反应的正反应是吸热反应
-
在一恒容密闭容器中发生某化学反应2A(g) B(g)+C(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,B、C的起始浓度都为0,反应物A的浓度(mol·L-1)随时间(min)的变化如图所示:
B(g)+C(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,B、C的起始浓度都为0,反应物A的浓度(mol·L-1)随时间(min)的变化如图所示:

试回答下列问题:
(1)在实验Ⅰ中,反应在20min至40min内A的平均反应速率为___________mol·L-1min-1。
(2)实验Ⅱ和实验I相比,可能隐含的反应条件是_____________________________。
(3)根据实验Ⅲ和实验Ⅰ的比较,可推测该反应降低温度,平衡向_____(填“正”或“逆”)反应方向移动,该正反应是_________(填“放热”或“吸热”)反应。
(4)与实验Ⅰ相比,若实验Ⅰ中的A的起始浓度改为0.8 mol·L-1,其它条件不变,则达到平衡时所需用的时间___________实验Ⅰ(填写“大于”、“等于”或“小于”)。
-
化学反应 在四个不同条件下进行。B、D起始为0,反应物A的浓度
在四个不同条件下进行。B、D起始为0,反应物A的浓度 随反应时间
随反应时间 变化情况如下表:
变化情况如下表:
| 实验序号 | 时间 浓度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.8 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | 
| 0.8 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | 
| 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
下列说法不正确的是( )
A.实验1,反应在10至 内
内
B.实验2,A的初始浓度 ,还隐含的条件是加入了催化剂
,还隐含的条件是加入了催化剂
C.实验3的反应速率v3<实验1的反应速率v1
D.比较实验4和实验1,可推测该反应为吸热反应
-
在不同条件下进行化学反应 ,B、D起始浓度均为0,反应物A的浓度
,B、D起始浓度均为0,反应物A的浓度 随反应时间的变化情况如下表:下列说法不正确的是( )
随反应时间的变化情况如下表:下列说法不正确的是( )
| 序号 | 时间 温度 | 0 | 20 | 40 | 50 |
| ① | 800 | 
| 
| 
| 
|
| ② | 800 | x | 
| 
| 
|
| ③ | 800 | y | 
| 
| 
|
| ④ | 820 | 
| 
| 
| 
|
A.①中B在 min平均反应速率为
min平均反应速率为

B.②中 ,可能使用了催化剂
,可能使用了催化剂
C.③中

D.比较①④可知,该反应为吸热反应
-
在不同条件下进行化学反应 ,B、D起始浓度均为0,反应物A的浓度
,B、D起始浓度均为0,反应物A的浓度 随反应时间的变化情况如下表:下列说法不正确的是( )
随反应时间的变化情况如下表:下列说法不正确的是( )
| 序号 | 时间 温度 | 0 | 20 | 40 | 50 |
| ① | 800 | 
| 
| 
| 
|
| ② | 800 | x | 
| 
| 
|
| ③ | 800 | y | 
| 
| 
|
| ④ | 820 | 
| 
| 
| 
|
A.①中B在 min平均反应速率为
min平均反应速率为

B.②中 ,可能使用了催化剂
,可能使用了催化剂
C.③中

D.比较①④可知,该反应为吸热反应
-
(8分)(2011·泰州模拟)某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
| 实验 序号 | 时间 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800 | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1中,反应在10 min~20 min时间内平均速率为________mol·L-1·min-1。
(2)在实验2中,A的初始浓度c2=________mol·L-1,反应经20 min就达到平衡,可推测实验2中还隐含的条件是________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3________v1,且c3________1.0 mol/L(填“=”、“>”或“<”)
(4)比较实验4和实验1,可推测该反应是________反应(填“吸热”或“放热”),理由是________________________________________________________________________。
-
某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
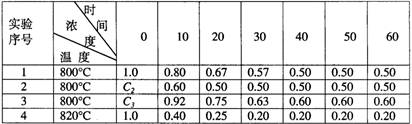
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为________mol/(L·min)。
(2)在实验2,A的初始浓度c2=________mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3________v1(填>、=、<),且c3________1.0mol/L(填>、=、<)
(4)比较实验4和实验1,可推测该反应是________反应(选填吸热、放热)。理由是________。
-
某化学反应2A B+D在四种不同条件下进行。B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行。B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
| 实验序号 | | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1中,反应在10至20分钟内平均速率为。
(2)在实验2中,A的初始浓度c2=__________________,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是__________________。
(3)设实验3中的反应速率为v3,实验1的反应速率为v1,则v3__________v1(填“>”、“=”或“<”),且c3__________1.0mol·L-1(填“<”、“=”或“>”)。
(4)比较实验4和实验1,可推测该反应是__________反应(填“吸热”或“放热”)。
-
某化学反应2A B+D在四种不同条件下进行,B,D起始浓度为0,反应物A的的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B,D起始浓度为0,反应物A的的浓度(mol/L)随反应时间(min)的变化情况如下表:
| 实验 序号 | 
| 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | c2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为_________mol/(L·min)。
(2)在实验2,A的初始浓度c2=_________mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是____________。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3_______________v1(填>、=、<),且c3___________1.0 mol/L(填>、=、<)。
(4)比较实验4和实验1,可推测该反应速率快的是________,理由是______________________。
B(g) + D(g)在四种不同的条件下进行,B、D起始浓度为0,反应物A的浓度随反应时间的变化情况如下表:

