-
天然气是一种清洁的化石燃料,也是引起温室效应的一种物质。天然气的综合利用对节能减排、高效利用能源、减少二氧化碳排放有重大意义。作为化工原料,合成甲醇是天然气综合利用的重要途径。
CH4(g)+ CO2(g) 2CO(g)+ 2H2(g)△H=+247.3 kJ·mol—1 ①
2CO(g)+ 2H2(g)△H=+247.3 kJ·mol—1 ①
CH4(g)+H2O(g) CO(g)+3H2(g) △H=+206.2 kJ·mol—1 ②
CO(g)+3H2(g) △H=+206.2 kJ·mol—1 ②
Ⅰ、合成甲醇的主要反应为:2H2(g)+ CO(g) CH3OH(g) △H=-90.8 kJ·mol—1
CH3OH(g) △H=-90.8 kJ·mol—1
(1)该反应熵变△S________0(填“>、=或<”),该反应在______(填“高温”或“低温”)条件下能自发进行。
(2)生产过程中,合成气要循环,其目的是:________________________________。
(3)T℃下此反应的平衡常数为160。某时刻测得各组分的浓度如下,比较此时正、逆反应速率的大小:υ(正)________υ(逆)(填“>”“<”或“=”)
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol·L—1) | 0.20 | 0.10 | 0.40 |
(4)在恒温恒容条件下,充入一定量的H2和CO,发生上述反应,则该反应达到平衡状态的标志有(__________________)
A.混合气体的密度保持不变 B.混合气体的总压强保持不变
C.甲醇的浓度保持不变 D.υ正(H2)= υ逆(CH3OH)
(5)在恒温恒容条件下,要提高反应2H2(g)+ CO(g) CH3OH(g)中CO的转化率,可以采取的措施是(______________)
CH3OH(g)中CO的转化率,可以采取的措施是(______________)
A.升温 B.加入催化剂 C.增加CO的浓度
D.增加H2的浓度 E.充入惰性气体 F.分离出甲醇
Ⅱ、合成甲醇的另一反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-akJ·mol-1(a>0)。
CH3OH(g)+H2O(g) △H=-akJ·mol-1(a>0)。
在一定温度下的2L固定容积的密闭容器中,通入2 molCO2和3mol H2,发生上述反应,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
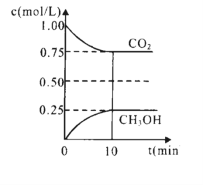
(6)下列措施中能使n(CH3OH )/n(CO2 )增大的是______(填编号)。
A.升高温度
B.恒温恒容下充入He(g)
C.将H2O(g)从体系中分离
D.恒温恒容再充入2 mol CO2和3 mol H2
(7)经计算该温度下此反应的平衡常数K=0.20 L2·mol—2。若改变条件_________(填选项),可使K=1。
A.增大压强 B.增大反应物浓度 C.降低温度
D.升高温度 E.加入催化剂
(8)10min内,用H2表示的该反应的化学反应速率为=_________mol·L—1·min—1
-
(12分) 二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放。
(1)在一定温度下的2L固定容积的密闭容器中,通入2 molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H =-akJ·mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如下图所示。
CH3OH(g)+H2O(g) △H =-akJ·mol-1(a>0),测得CO2(g)和CH3OH(g)的浓度随时间变化如下图所示。

①能说明该反应已达平衡状态的是________
A.CO2的体积分数在混合气体中保持不变
B.混合气体的密度不随时间的变化而变化
C.单位时间内每消耗1.2mol H2,同时生成0.4molH2O
D.反应中H2O与CH3OH的物质的量浓度之比为1:1, 且保持不变
②下列措施中能使 增大的是________ (选填编号)。
增大的是________ (选填编号)。
A.升高温度
B.恒温恒容下充入He(g)
C.将H2O(g)从体系中分离
D.恒温恒容再充入2 mol CO2和3 mol H2
③计算该温度下此反应的平衡常数K=___________ , 若改变条件 (填选项),可使K=1。
A增大压强 B增大反应物浓度 C.降低温度
D.升高温度 E.加入催化剂
 (2)某甲醇燃料电池原理如图1所示:M区发生反应的电极反应式为_______________________________。
(2)某甲醇燃料电池原理如图1所示:M区发生反应的电极反应式为_______________________________。

-
二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放。在一定温度下的2L固定容积的密闭容器中,通入2 molCO2和3mol H2,发生的反应为:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),△H=-a kJ·mol-1(a>0), 测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),△H=-a kJ·mol-1(a>0), 测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。
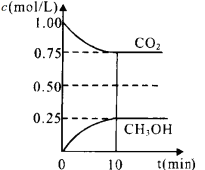
①能说明该反应已达平衡状态的是__________(填编号)
A.CO2的体积分数在混合气体中保持不变
B.混合气体的平均相对分子质量不随时间的变化而变化
C.单位时间内每消耗1.2mol H2,同时生成0.4molH2O
D.该体系中H2O与CH3OH的物质的量浓度之比为1:1,且保持不变
②计算该温度下此反应的平衡常数K=_________。(保留两位有效数字)。若改变条件 (填选项),可使K=1。
A.增大压强
B.增大反应物浓度
C.降低温度
D.升高温度
E.加入催化剂
-
下列说法中错误的是
A.推广使用新能源,可以减少二氧化碳等温室气体的排放
B.发电厂的燃煤在燃烧时加入适量石灰石,可减少二氧化硫排放
C.石油、煤、天然气均属于可再生的化石燃料
D.太阳能、氢能、风能属于清洁能源
-
下列说法中错误的是
A.推广使用新能源,可以减少二氧化碳等温室气体的排放
B.发电厂的燃煤在燃烧时加入适量石灰石,可减少二氧化硫排放
C.石油、煤、天然气均属于可再生的化石燃料
D.太阳能、氢能、风能属于清洁能源
-
“低碳经济,节能减排”是21世纪世界经济发展的新思路。下列与之相悖的是( )
A.开发水能、风能、太阳能、地热能、核能等新能源,减少使用煤、石油等化石燃料
B.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
C.大力开采煤、石油和天然气,以满足经济发展的需要
D.大力发展新能源汽车,如混合动力汽车、电动汽车等,以减少碳、氮氧化物的排放
-
化学与生活、社会密切相关,“低碳经济,节能减排”是今后经济发展的新思路。下列说法不正确的是
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.将废弃的秸秆转化为清洁高效的能源
C.大量开采煤、石油和天然气,以满足经济发展的需要
D.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
-
化学与生活、生产密切相关.下列说法不正确的是( )
A.低碳生活就是节能减排,使用太阳能等代替化石燃料,可减少温室气体的排放
B.新能源的优点主要是资源丰富、可再生、没有或很少有污染
C.氢能的优点热值高、资源丰富、燃烧产物无污染;缺点是储存和运输困难
D.高纯度的硅单质广泛用于制作光导纤维
-
化学已经渗透到人类生活的各个方面,下列有关说法不正确的是( )
A.低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,减少温室气体的排放。
B.“光化学烟雾”、“臭氧空洞”、“硝酸酸雨”的形成都与氮氧化合物有关。
C.高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路”。
D.禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染。
-
我国正在大力执行“节能减排”的政策.“节能”,要求节约能源;“减排”,要求降低“三废”的排放.下列废气大量排放能引起“温室效应”的是( )
A.SO2
B.NO
C.CO2
D.CO
2CO(g)+ 2H2(g)△H=+247.3 kJ·mol—1 ①
CO(g)+3H2(g) △H=+206.2 kJ·mol—1 ②
CH3OH(g) △H=-90.8 kJ·mol—1
CH3OH(g)中CO的转化率,可以采取的措施是(______________)
CH3OH(g)+H2O(g) △H=-akJ·mol-1(a>0)。



