-
A、B、C、D、E五种短周期元素,其中A是地壳中含量最多的元素;C元素的单质存在于火山喷发口附近或地壳的岩层里;E原子的电子总数等于其电子层数的3倍;D的一种原子核中没有中子;A、B、C三种元素的族序数之和为16。下列说法错误的是
A. D与E可形成既含极性键又含非极性键的分子
B. B的最高价氧化物为酸性氧化物,不能与任何酸反应
C. B、C、E三种元素的最高价氧化物对应的水化物中,B的酸性最弱
D. A、C、D中两种或三种元素形成的钠盐溶液可显酸性、中性或碱性
高三化学单选题中等难度题查看答案及解析
-
短周期主族元素R、X、Y、Z、M的原子序数依次增大,它们分别位于三个周期。Y和M同主族,火山喷口附近或地壳的岩层中存在游离态的M, X元素的最高价氧化物对应的水化物与其气态氢化物相遇会有白烟。这五种元素组成一种离子化合物Q,取一定量Q溶于蒸馏水得到溶液,向此溶液中滴加稀氢氧化钠溶液,产生沉淀的物质的量与氢氧化钠溶液体积的关系如图所示。下列说法不正确的是( )

A. 简单氢化物的沸点:Y>X
B. 简单离子的半径:M>Y>Z
C. R与除Z以外的其他3种元素均能形成共价化合物
D. Y与其他4种元素均可形成至少两种二元化合物
高三化学单选题简单题查看答案及解析
-
A、D、E、M、L是原子序数依次增大的五种短周期元素.已知A是元素周期表中原子半径最小的元素;D的某种单质是天然存在的最硬物质;E是地壳中含量最多的元素;M与A位于同一主族;L与M能够形成ML型离子化合物.回答下列问题:
(1)元素D在元素周期表中的位置是______.
(2)L的单质与M的最高价氧化物对应水化物反应的离子方程式为______.
(3)25℃时,物质的量浓度相同的MEA、MADE3、MLE三种溶液,水的电离程度由大到小的顺序为______.(填化学式)
(4)设化合物甲、乙、丙分别为DA3EA、DA3EDA3、A2E.
ⅰ:已知:(1)丙(g)═丙(l)△H=-Q1 kJ•mol-1
(2)2甲(l)+3E2(g)═2DE2(g)+4丙(g)△H=-Q2 kJ•mol-1
Q1、Q2均大于0.若要使32g液态甲完全燃烧并恢复到室温,放出的热量为______.
ⅱ:已知:2甲(g)=乙(g)+丙(g).在某温度下,在1L密闭容器中加入甲,反应到10分钟时达到平衡,此时测得各组分的浓度如下:
①该温度下反应的平衡常数为______.物 质 甲 乙 丙 浓度/mol•L-1 0.01 0.2 0.2
②10min内平均反应速率v(甲)=______.
ⅲ:如图是乙为燃料的绿色电源工作原理示意图.若b电极的反应式为:3O2+12e-+12H+═6H2O,则a电极的反应式为:______.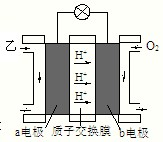
高三化学解答题中等难度题查看答案及解析
-
短周期元素W、X、Y、Z、Q的原子序数依次增大,W的阴离子的核外电子数与氦相同。X的一种核素在考古时常用来鉴定一些文物的年代,Y在地壳中含量最多,Z原子半径为短周期中最大,Q存在由多原子分子构成的单质。下列说法错误的是
A. W与X可形成3种以上化合物
B. W、X、Y只能形成1种二元酸
C. Y与Z可形成既含共价键又含离子键的化合物
D. X、Q的最高价氧化物对应水化物的酸性:Q>X
高三化学单选题中等难度题查看答案及解析
-
X、Y、Z、W四种短周期元素,原子序数依次增大。元素X的最高正价与最低负价代数和为零,Z元素最外层电子数是内层电子数的3倍,W是地壳中含量最高的金属元素。下列说法不正确的是
A. X、Z的单质均存在同素异形体
B. 原子半径大小顺序为:W>X>Y>Z
C. W的氢氧化物既可易溶于Y的气态氢化物的水溶液,又可溶于Y的最高价含氧酸
D. Y、Z、W三种元素,可以形成既含离子键又含共价键的离子化合物
高三化学单选题中等难度题查看答案及解析
-
短周期元素X、Y、Z、M、R的原子序数依次增大。Y、R同主族且均为植物生长所必需的营养元素,X的某种单质能导电,X、Y、Z的化合物存在如下反应:2XZ + 2YZ=Y2 + 2XZ2, M为地壳中含量最高的金属元素。下列说法正确的是
A. 原子半径:R>M>X>Y>Z B. 元素的非金属性X<Y<Z
C. 工业上通过电解M的氯化物来制取M单质 D. RCl3水解会生成两种强酸
高三化学null中等难度题查看答案及解析
-
X、Y、Z、W是元素周期表前四周期的常见元素,其相关信息如下表:
X
X的一种核素的质子数为56,中子数为30
Y
海水中元素含量最高的金属元素
Z
常温常压下,Z单质是淡黄色固体,常在火山口附近沉积
W
价电子的排布式为3s23p3
(1)Z元素在元素周期表中的位置为,Z的电负性比W的________(填“大”或“小”)。
(2)X元索的基态原子电子排布式是 _________,其有___种运动状态不同的电子。该元素的白色氧氧化物在空气中会迅速变成灰绿色。最后变成红褐色、其反应的化学方程式为________。
(3)Y的单质在工业上用途广泛,工业上以YW制取Y单质的化学方程式为________。
(4)设计实验验证Z和W的非金属性的强弱:________。
高三化学填空题困难题查看答案及解析
-
已知
、
、
、
为原子序数依次增大的短周期元素,
为地壳中含量最高的过渡金属元素,
与
同主族,
与
同周期,且
与
的原子序数之和为20,
单质能与无色无味液体
反应置换出
单质,
单质也能与
反应置换出
单质,
、
、
均能与
形成离子化合物,下列说法不正确的是( )
A.
、
两元素的形成的化合物都为黑色固体
B.
、
形成的离子化合物可能含有其价键
C.
的单质只有还原性,没有氧化性
D. 工业上可以用铝热法制取金属
用于野外焊接铁轨
高三化学单选题困难题查看答案及解析
-
【化学-选修3:物质结构与性质】
已知A、B、C、D、E、F是周期表前四周期的元素,原子序数依次增大。A的基态原子2p能级有2个单电子;C占整个地壳质量的48.6%,是地壳中含量最多的元素;E的单质常温常压下为黄绿色气体,化学性质十分活泼,具有毒性;F位于ds区,最外能层有单电子, 是热和电最佳导体之一,是唯一的能大量天然产出的金属;D与F不同周期,但最外能层电子数相等。
(1)写出基态D原子的价电子排布式 。
(2)A、B、C三种元素第一电离能最大的是 (用元素符号表示)
其原因是 。
(3)A、C两元素形成的化合物AC2的分子空间构型 _ _。 与 AC2互为等电子体的粒子的化学式_ , __ _(分子和离子各写一种)。
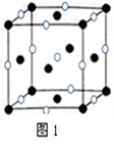
(4)D、E形成的一种离子化合物,在图1晶胞结构图中黑球表示E的位置,白球表示D的位置,已知该晶胞的边长为n cm,阿伏加德罗常数为NA,求:
晶胞的密度ρ= g/cm3(用含a、NA的计算式表示)。
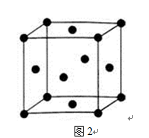
(5)由F原子形成的晶胞结构如图2,F原子的半径为r,列式表示E原子在晶胞中的空间利用率 (不要求计算结果)。
高三化学推断题困难题查看答案及解析
-
元素组成物质,下列说法不正确的是( )
A.构成地壳基本骨架的非金属元素的是O、Si
B.蛋白质中均含C、H、O、N四种元素
C.海水中的钠元素经过物理变化就可形成钠单质
D.火山喷发形成的物质中通常含有硫元素高三化学选择题中等难度题查看答案及解析