下列过程不属于放热反应的是( )
A. 木材燃烧
B. N2(g)+3H2(g) 2NH3(g)
C. H20(g)=H20(l)
D. 盐酸和氢氧化钠反应
高二化学单选题简单题
下列过程不属于放热反应的是( )
A. 木材燃烧
B. N2(g)+3H2(g) 2NH3(g)
C. H20(g)=H20(l)
D. 盐酸和氢氧化钠反应
高二化学单选题简单题
下列过程不属于放热反应的是( )
A. 木材燃烧
B. N2(g)+3H2(g) 2NH3(g)
C. H20(g)=H20(l)
D. 盐酸和氢氧化钠反应
高二化学单选题简单题查看答案及解析
下列过程不属于放热反应的是( )
A. 木材燃烧
B. N2(g)+3H2(g) 2NH3(g)
C. H20(g)=H20(l)
D. 盐酸和氢氧化钠反应
高二化学单选题简单题查看答案及解析
合成氨工业发生反应:N2 + 3H2 2NH3 ,下列措施不属于加快反应速率的是
A. 温度控制在500℃ B. 铁触媒作为催化剂
C. 压强控制在20MPa ~ 50MPa D. 混合气体中分离出液态氨
高二化学单选题简单题查看答案及解析
(17分)氨的合成原理为:N2(g)+3H2(g)2NH3(g) ;△H= —92.4 KJ·mol—1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如图。
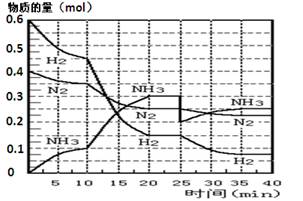
回答下列问题:
(1)10 min内以NH3表示的平均反应速率________;
(2)在10 ~20 min内:NH3浓度变化的原因可能是 ________;
A.加了催化剂 B.缩小容器体积 C.降低温度 D.增加NH3物质的量
(3)第1次平衡的时间范围为:________,第2次平衡的时间范围为:________,
第1次平衡:平衡常数K1 = ________(带数据的表达式),第2次平衡时NH3的体积分数 ________;
(4)在反应进行至25 min时:
① 曲线发生变化的原因:________
② 达第二次平衡时,新平衡的平衡常数K2 ________ K1(填“大于”、“等于”、“小于”);
(5)在25~40 min时,计算合成氨过程中的反应热△H= ________。
(6)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:
N2(g) + 3H2O(1) 2NH3(g) +
O2(g) ;△H = a kJ·mol—1
进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
①此合成反应的a________0;ΔS________0,(填“>”、“<”或“=”)
②已知:N2(g) + 3H2(g)2NH3(g) ΔH= -92 .4kJ·mol—1
2H2(g) + O2(g) = 2H2O(l) = -571.6kJ·mol—1
则常温下氮气与水反应生成氨气与氧气的热化学方程式为:________
高二化学填空题简单题查看答案及解析
(16分)氨的合成原理为:N2(g)+3H2(g)2NH3(g) ;△H= —92.4 KJ·mol—1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如下图。回答下列问题:
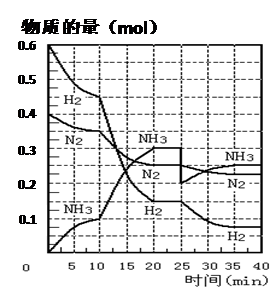
(1)10 min内以NH3表示的平均反应速率________;
(2)在10 ~20 min内:NH3浓度变化的原因可能是 ________;
A.加了催化剂 B.缩小容器体积
C.降低温度 D.增加NH3物质的量
(3)第1次平衡的时间范围为:________,第2次平衡的时间范围为:________,第1次平衡:平衡常数K1 = ________(带数据的表达式),第2次平衡时NH3的体积分数 ________;
(4)在反应进行至25 min时:① 曲线发生变化的原因:________② 达第二次平衡时,新平衡的平衡常数K2 ________ K1(填“大于”、“等于”、“小于”)
高二化学填空题简单题查看答案及解析
(27分)氨的合成原理为:N2(g)+3H2(g)2NH3(g) ;△H= —92.4 KJ·mol—1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如下图。回答下列问题:
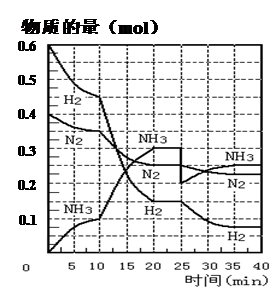
(1)10 min内以NH3表示的平均反应速率________;
(2)在10 ~20 min内:NH3浓度变化的原因可能是 ________;
A.加了催化剂 B.缩小容器体积
C.降低温度 D.增加NH3物质的量
(3)第1次平衡的时间范围为:________,
第2次平衡的时间范围为:________,
第1次平衡:平衡常数K1 = ________(带数据的表达式),
第2次平衡时NH3的体积分数 ________;
(4)在反应进行至25 min时:
① 曲线发生变化的原因:________
② 达第二次平衡时,新平衡的平衡常数
K2 ________ K1(填“大于”、“等于”、“小于”);
(5)在25~40 min时,计算合成氨过程中的反应热△H= ________。
(6)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:
N2(g) + 3H2O(1) 2NH3(g) +
O2(g) ;△H = a kJ·mol—1
进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
①此合成反应的a________0;ΔS________0,(填“>”、“<”或“=”)
②已知:N2(g) + 3H2(g)2NH3(g) ΔH= -92 .4kJ·mol—1
2H2(g) + O2(g) = 2H2O(l) = -571.6kJ·mol—1
则常温下氮气与水反应生成氨气与氧气的热化学方程式为:
高二化学实验题简单题查看答案及解析
氨是重要的氮肥,合成原理为: N2(g)+3H2(g)2NH3(g) △H= —92.4 kJ/mol。在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各种物质的量变化如图,回答下列问题:
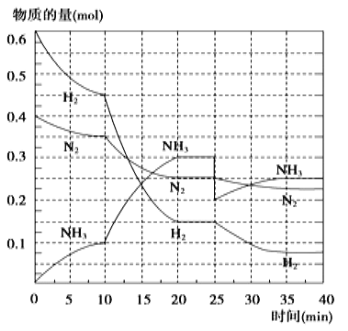
(1)10 min内以NH3表示的平均反应速率:______;
(2)在10 ~20 min内:NH3浓度变化的原因可能是______________
A.加了催化剂 B.缩小容器体积 C.降低温度 D.增加NH3物质的量
(3)第1次平衡的平衡常数K1 = _________________(带数据的表达式),第2次平衡时NH3的体积分数=___________(小数点后保留一位);
(4)在反应进行至25 min时:①曲线发生变化的原因______________,② 达第二次平衡时,新平衡的平衡常数K2 ____ K1(填“大于”“等于”或“小于”)。
高二化学填空题中等难度题查看答案及解析
氨是重要的氮肥,合成原理为: N2(g)+3H2(g)2NH3(g) △H= —92.4 kJ/mol。在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各种物质的量变化如图,回答下列问题:
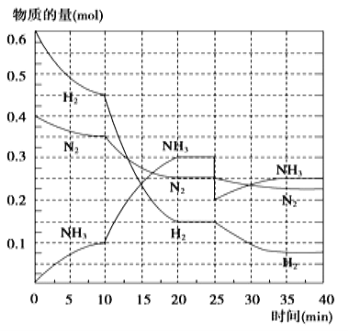
(1)10 min内以NH3表示的平均反应速率:______;
(2)在10 ~20 min内:NH3浓度变化的原因可能是______________
A.加了催化剂 B.缩小容器体积 C.降低温度 D.增加NH3物质的量
(3)第1次平衡的平衡常数K1 = _________________(带数据的表达式),第2次平衡时NH3的体积分数=___________(小数点后保留一位);
(4)在反应进行至25 min时:①曲线发生变化的原因______________,② 达第二次平衡时,新平衡的平衡常数K2 ____ K1(填“大于”“等于”或“小于”)。
高二化学填空题中等难度题查看答案及解析
氨的合成原理为:N2(g)+3H2(g)2NH3(g) ;△H= —92.4 KJ·mol—1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如右图。回答下列问题:
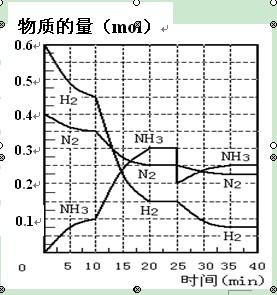
(1)10 min内以NH3表示的平均反应速率________;
(2)在10 ~20 min内:NH3浓度变化的原因可能是 ________;
A.加了催化剂 B.缩小容器体积 C.降低温度 D.增加NH3物质的量
(3)第1次平衡的时间范围为:________平衡常数K1 ="_____________" ________(表达式),第2次平衡时NH3的体积分数 ________;
(4)在反应进行至25 min时, 曲线发生变化的原因:________
高二化学填空题中等难度题查看答案及解析
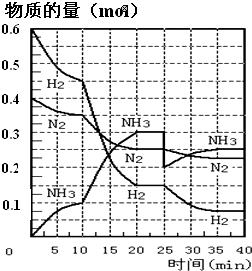
高二化学解答题中等难度题查看答案及解析