-
(1)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(l)+3/2O2(g)===CO2(g)+2H2O(g)ΔH=-a kJ/mol,则 a___238.6(填“>”、“<”或“=”)。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:_________________________________。
(3)反应mA(g)+nB(g) pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
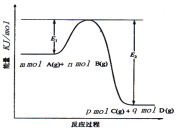
该反应△H =____(用含E1、E2式子表示);在反应体系中加入催化剂,E1___,E2___,(填增大、减小、不变)。
(4)已知:CO (g) +H2O (g) H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
回答下列问题:
①该反应的ΔH=__________填“>”、“=”或“<”)。
②已知在一定温度下,C(s) +CO2 (g) 2CO(g)平衡常数K1;C (s) +H2O (g)
2CO(g)平衡常数K1;C (s) +H2O (g) CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是__________________________。
CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是__________________________。
-
(1)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,
CH3OH(l)+3/2O2(g)===CO2(g)+2H2O(g)ΔH=-a kJ/mol,则 a___238.6(填“>”、“<”或“=”)。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ 热量,写出该反应的热化学方程式:_________________________________
(3)反应mA(g)+nB(g) pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。

该反应△H =____kJ/mol(用含E1、E2式子表示); 在反应体系中加入催化剂,E1___,E2___,(填增大、减小、不变)。
(4)已知:
CO (g) +H2O (g) H2 (g) +CO2 (g)平衡常数K
H2 (g) +CO2 (g)平衡常数K
C(s) +CO2 (g) 2CO(g)平衡常数K1
2CO(g)平衡常数K1
C (s) +H2O (g) CO(g) +H2 (g)平衡常数K2
CO(g) +H2 (g)平衡常数K2
则K、K1 、K2之间的关系是 ___________________________________
-
碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)已知CH3OH(l)的燃烧热△H为-238.6kJ·mol-1
CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g) △H=-QkJ·mol-1(Q>0)
则Q__________(填“>”“<”或“ =”)238.6。
(2)使Cl2和H2O(g))通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式:________________ .
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煆烧,所得物质可作耐高温材料:4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) △H=-1176kJ·mol-1,则反应过程中,每转移1mol电子放出的热量为__________。
-
(1)已知:①CO(g)+ O2(g)=CO2(g)△H=-283.0kJ•mol-1
O2(g)=CO2(g)△H=-283.0kJ•mol-1
②CH3OH(l)+ O2(g)=CO2(g)+2H2O(l)△H=-726.5kJ•mol-1
O2(g)=CO2(g)+2H2O(l)△H=-726.5kJ•mol-1
请写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: ______。
(2)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似.已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,则1molN4气体转化为2molN2时的△H= ______ 。

-
碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)已知CH3OH(l)的燃烧热为726.51kJ/mol,CH3OH(l) + 1/2O2(g)=CO2(g) + 2H2O(g) ΔH=-a kJ/mol,则a______(填“>”“<”或“=”)726.51。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1mol Cl2参与反应时释放出145kJ热量,写出该反应的热化学方程式___________________。
(3)火箭和导弹表面的薄层是耐高温的物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,反应的热化学方程式为:4Al(s) + 3TiO2(s) + 3C(s)=2Al2O3(s) + 3TiC(s) ΔH=-1176kJ/mol,则反应过程中,每转移1mol电子放出的热量为__________。
-
在25℃、101kPa下,0.1mol甲醇燃烧生成CO2和液态时放出72.58kJ,下列热化学方程式正确的是
A.CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l);△H=+725.8kJ/mol
B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g);△H=-1451.6kJ/mol
C.CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l);△H=-725.8kJ/mol
D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g);△H=+1451.6kJ/mol
-
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+ O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ/mol
O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ/mol
B.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ/mol
C.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-725.8kJ/mol
D.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=+1452kJ/mol
-
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+ O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ/mol
O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ/mol
B.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ/mol
C.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-725.8kJ/mol
D.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=+1452kJ/mol
-
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+ O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ/mol
O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ/mol
B.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ/mol
C.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-725.8kJ/mol
D.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=+1452kJ/mol
-
在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+ O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ/mol
O2(g)═CO2(g)+2H2O(l)△H=+725.8kJ/mol
B.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452kJ/mol
C.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-725.8kJ/mol
D.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=+1452kJ/mol
pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。

H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
2CO(g)平衡常数K1;C (s) +H2O (g)
CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是__________________________。
