-
(12分)某粗氧化铜样品中含少量氧化亚铁及不溶于酸的杂质,某化学兴趣小组利用该样品制取胆矾晶体,测定胆矾晶体中结晶水的含量,并计算样品中氧化铜的含量,设计了如下方案进行实验。
查阅资料知Fe3+、Cu2+、Fe2+在水溶液中形成氢氧化物沉淀的pH范围如下:
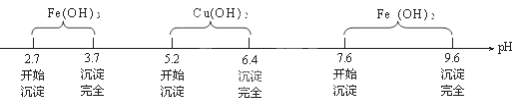
请回答下列问题:
(1)在整个实验过程中,下列仪器中不可能用到的是__________(填编号)。
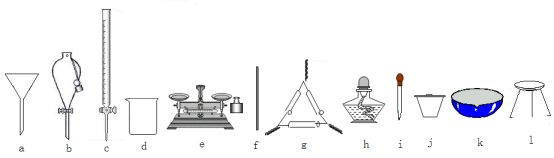
(2)物质X应选用_________(填字母)。
a.氢氧化钠 b.双氧水 c.铁粉 d.高锰酸钾
(3)为保证沉淀Ⅱ沉淀完全,操作③中溶液pH的调节范围为 。
(4)操作④的步骤有 、冷却结晶、 、自然干燥。
(5)在测定所得胆矾(CuSO4·xH2O)中结晶水x值的实验过程中:称量操作至少进行__ 次若测定结果x值偏大,可能的原因是_______________。
a.加热温度过高
b.胆矾晶体的颗粒较大
c.加热后放在空气中冷却
d.加热胆矾晶体时有晶体从坩埚中溅出
(6)该小组一位同学根据实验结果求出样品中CuO的质量分数为 ,另一位同学不同意,其原因是 。
,另一位同学不同意,其原因是 。
-
为测定粗氧化铜(其中含少量氧化亚铁及不溶于酸的杂质)中CuO的质量分数,并制取无水硫酸铜,某化学活动小组进行了下列实验:
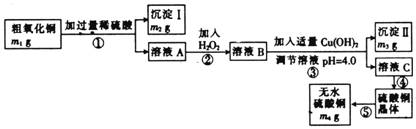
已知Fe3+、Cu2+、Fe2+三种离子在溶液中形成氢氧化物沉淀的pH范围如下:
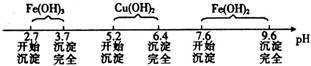
请回答下列问题:
(1)在整个实验过程中,下列实验装置不可能用到的是________(填字母),装置d中仪器A和B的名称分别为。
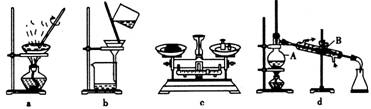
(2)溶液A中所含溶质的化学式为________。
(3)步骤②发生反应的离子方程式为________。
(4)沉淀II的化学式为________。
(5)粗氧化铜样品中CuO的质量分数为________。(列出计算式)
-
为测定粗氧化铜(其中含少量氧化亚铁及不溶于酸的杂质)中CuO的质量分数,并制取无水硫酸铜,某化学活动小组进行了下列实验:
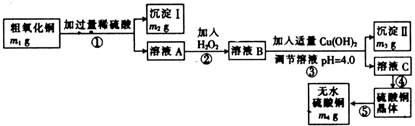
已知Fe3+、Cu2+、Fe2+三种离子在溶液中形成氢氧化物沉淀的pH范围如下:
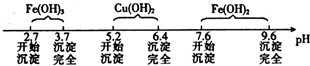
请回答下列问题:
(1)在整个实验过程中,下列实验装置不可能用到的是______(填字母),装置d中仪器A和B的名称分别为______.
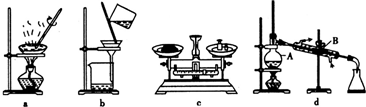
(2)溶液A中所含溶质的化学式为______.
(3)步骤②发生反应的离子方程式为______.
(4)沉淀II的化学式为______.
(5)粗氧化铜样品中CuO的质量分数为______.(列出计算式)
-
某化学兴趣小组用含有铝、铁、铜的合金制取纯净的氯化铝溶液、绿矾晶体(七水合硫酸亚铁)和胆矾晶体,以探索工业废料的再利用.其实验方案如下:试回答下列问题:
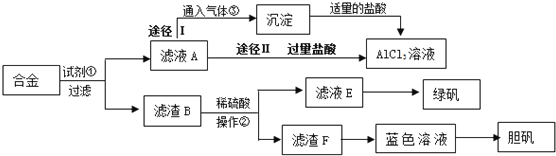
(1)写出合金溶于试剂①溶液时相关反应的离子方程式 ____________________________,操作②的名称是 ______________ 。
(2)滤液A中通入过量气体的离子反应方程式为_______________________________,由滤液A制AlCl3溶液有途径I和途径II两种,与途径I相比,途径II存在着明显的缺陷是: _________________________________________________________。
(3)溶液E中的主要溶质为 _____________________ ;如何检验滤液E是否已被氧化(写出操作过程、现象和结论) _______________________________________________。
(4)按环保要求,写出用滤渣F制备硫酸铜溶液的各步反应的化学方程式 ________。
-
(14分)某化学小组拟利用下列流程测定某草酸亚铁样品(含有少量草酸,不含结晶水和其他杂质)中FeC2O4的含量。
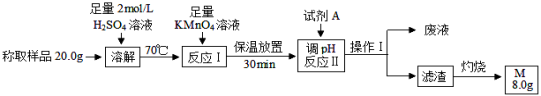
已知几种氢氧化物开始沉淀和完全沉淀的pH如下表所示
| Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
试回答下列问题:
(1)用2 mol/L H2SO4溶液溶解草酸亚铁样品而不用蒸馏水直接溶解的原因是 ,加热至70℃左右,立即用KMnO4溶液滴定至终点。发生反应的离子方程式为2MnO4- + 5H2C2O4 +6H+ =2Mn2+ + 10CO2↑+ 8H2O和 。
(2)保温放置30min的目的是 。
(3)证明反应Ⅰ完全的实验操作或现象为 。
(4)已知常温下Fe(OH)3的Ksp=1.1×10-36,废液中c(Fe3+)= mol·L-1。
(5)灼烧充分的标志是 。
(6)样品中FeC2O4的含量为 。
-
硫酸亚铁是一种重要的食品和饲料添加剂,某课外兴趣小组在实验室用废铁屑与稀硫酸在加热条件下制取FeSO4•X H2O,并测定该晶体中结晶水含量.请回答下列问题:
(1)铁屑表面少量的铁锈对制取硫酸亚铁有无影响______(填“有”或“无”.其原因是______,该步实验的关键是保证______过量(填“硫酸”或“铁屑”);
(2)FeSO4在不同温度下溶解度如下表所示:
| 温度/℃ | | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g/100g水 | 18.5 | 20.8 | 26.3 | 32.8 | 40.1 | 48.4 | 52.4 | 50.9 | 43.7 |
由于铁屑中含有C、Si等杂质,为了使FeSO4 溶液的浓度增大,便于反应后分离溶液和残渣.该小组实验时采取了水浴加热和趁热过滤的方法,这样做的主要目的是为了防止______.你认为实验时的水浴温度最好控制在______℃左右.从滤液中获得FeSO4•xH2O,下列操作中不需要的是______;
(A)冷却 (B)蒸发
(C)结晶 (D)洗涤 (E)过滤
(3)以下是测定FeSO4•xH2O中结晶水含量的实验流程.(称量仪器为电子天平)
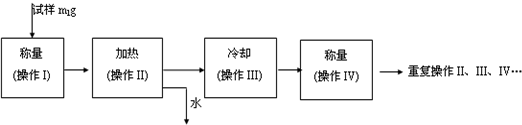
①其加热装置正确的是______
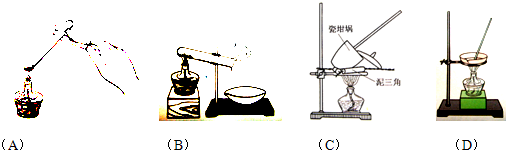
②重复操作II、III、IV,直到连续两次称量结果相差不超过______g;
③操作III必须要在______中(填仪器名称)进行.
(4)以下结晶水含量测定操作正确的是______;
A、加热时,晶体溅出坩埚,再加些FeSO4•xH2O
B、加热时,先用小火,后用大火加热至最后
C、加热时,不断用玻璃棒搅拌
D、恒重操作是指加热、冷却、称量这一过程重复两次
(5)实验中出现下列情况时,将对X值有何影响(填“偏大”、“偏小”或“无影响”):灼烧时有黑色固体出现______;在冷却过程中,无水硫酸亚铁又吸收了空气中的水蒸气______.
-
硫酸铜晶体俗称“胆矾”,在无机化工及生产生活中有广泛的应用。某课外研究小组的同学用粗铜粉(含有碳等杂质)设计了两种制备胆矾的途径,并测定了其中结晶水的含量。设计的流程如下:
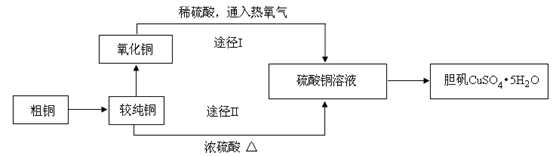
(1)“较纯铜”转化为氧化铜时,应将其置于________内进行灼烧(填写仪器名称)。“粗铜”表面的油脂可以用热碱溶液洗去,原因是________。若灼烧“粗铜”,获得的产物是混有少量铜的氧化铜。存在少量铜的可能原因是________。
a.灼烧过程中部分氧化铜被还原 b.该条件下铜无法被氧气氧化
c.氧化铜在加热过程中分解生成铜 d.灼烧不充分铜未被完全氧化
(2)通过途径I实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤是:酸溶、加热通氧气、过滤、________、冷却结晶、________、自然干燥。比较由粗制氧化铜制取胆矾的两种途径,途径Ⅰ有明显的两个优点:
① ________ ________。
②________。
(3)测定胆矾晶体里结晶水的含量时,若测定的相对误差大于零,则产生误差的原因可能是___________。
a.加热后容器未放入干燥器中冷却
b.最后两次加热后的质量相差较大
c.加热前称量时容器未完全干燥
d.加热过程中有少量溅失
(4)利用下图装置加热无水硫酸铜粉末直至完全分解,A的试管中剩余黑色粉末,用带火星的木条伸入集气瓶D,发现木条能复燃。反应前后各装置的质量见图下方的表格所示。
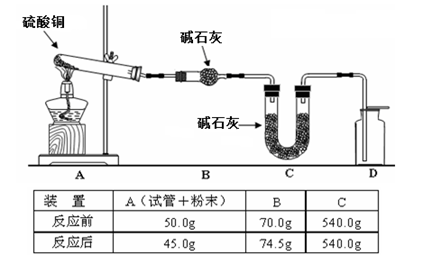
请通过计算,推断该实验条件下硫酸铜分解的化学方程式:________。
-
某化学小组用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜,其实验流程如下所示:
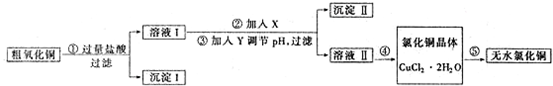
(1)步骤①中氧化铜与盐酸反应的离子方程式是______.
(2)步骤①、③的过滤操作中,除用到铁架台(带铁圈)外,还需要使用的玻璃仪器是______.
(3)已知:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| 提供的试剂:a.NaOH b.H2O2c.Na2CO3d.CuO |
参照表中给出的数据和试剂,请回答:
步骤②的目的是______,反应的离子方程式是______.步骤③中调节溶液pH的范围是______,试剂Y是______(填字母).
(4)步骤⑤要得到无水氯化铜,需要在干燥的HCl气流中加热CuCl2•2H2O,其原因是______.
-
(14分)
某化学小组用粗氧化铜(含少量氧化亚铁及不溶于酸的杂质)制取无水氯化铜,其实验流程如下所示:
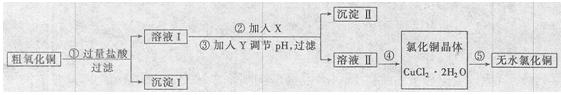
(1)步骤①中氧化铜与盐酸反应的离子方程式是________。
(2)步骤①、③的过滤操作中,除用到铁架台(带铁圈)外,还需要使用的玻璃仪器是
________。
(3)已知:
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH |
| Fe3+ | 1.9 | 3.2 |
| Fe2+| | 7.0 | 9.0 |
| Cu2+ | 4.7 | 6.7 |
| 提供的试剂:a. NaOH b. H2O2 c. Na2CO3 d. CuO |
参照表中给出的数据和试剂,请回答:
步骤②的目的是________,反应的离子方程式是________。步骤③中调节溶液pH的范围是________,试剂Y是________(填字母)。
(4)步骤⑤要得到无水氯化铜,需要在干燥的HCl气流中加热CuCl2·2H2O,其原因是________。
-
黄铁矿是工业上制取硫酸的主要原料,其主要成分为FeS2,含少量杂质(杂质不含S元素,且高温下不反应)。某化学兴趣小组用下列装置测定黄铁矿中硫元素的质量分数。
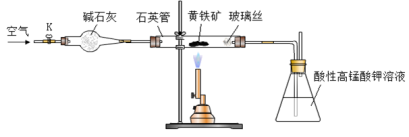
称取2.0g研细的黄铁矿样品,将样品放入石英管中,缓慢鼓入空气,再加热石英管至800~850℃;锥形瓶中盛装100 mL 0.2mol/L酸性KMnO4溶液用于吸收SO2(忽略SO2、H2SO3与氧气反应);反应结束后,每次从锥形瓶中取出25.00 mL溶液,用0.23mol/L标准H2C2O4溶液滴定,重复三次。
已知:4FeS2+11O2 2Fe2O3+8SO2;
2Fe2O3+8SO2;
2KMnO4+5SO2+2H2O K2SO4+2MnSO4+2H2SO4
K2SO4+2MnSO4+2H2SO4
请回答下列问题:
(1)连接好装置,检查装置气密性的操作是 。
(2)通入空气的作用是 。
(3)若实验过程中鼓入空气的速率过快,则测得的硫元素的质量分数 (填“偏高”、“偏低”或“不变”)。
(4)滴定时,应选择图中的 (填字母序号)盛装标准H2C2O4溶液,根据 现象来判断滴定已经达到终点。

(5)滴定过程中发生反应的离子方程式是 。
(6)如果黄铁矿中的硫全部转化为SO2,且被酸性KMnO4溶液完全吸收,滴定操作中,平均耗用0.23mol/L标准H2C2O4溶液21.73mL,则黄铁矿样品中硫元素的质量分数是 (保留到小数点后1位)。



,另一位同学不同意,其原因是 。















