-
a(g)镁和足量稀硫酸反应,镁完全反应后,测得氢气在常温时的体积为V(L),则常温下l mol氢气的体积为_________________L。
高二化学填空题简单题查看答案及解析
-
(10分)在常温常压下,可利用下列装置来测定气体体积,抽气装置E用以调节装置中的气压差,减小实验误差。
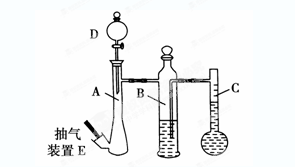
(1)若称取0.113g镁带与10.00 mL稀硫酸(足量)完全反应制取氢气,并测定1mol H2的体积(在常温常压下测定)。反应结束时C中的液面刻度为128.00 mL(A中未加硫酸时C中无液体),则得此条件下1mol H2的体积为________L(精确到0.001)。
(2)上述测出1mol H2的体积比该温度和压强下的理论值偏高的原因是(假设操作和装置都无问题)________(选填编号,下同)
A.未冷却到室温 B.反应太快
C.装置气密性不好 D.B装置漏气
(3)若利用上述装置测定CO2的气体摩尔体积。
①B中所盛放的液体应为________。
A.饱和Na2CO3溶液 B.饱和NaHCO3溶液
C.水 D.澄清石灰水
②仪器A、D中盛放的试剂应为________。
A.大理石,浓盐酸 B.纯碳酸钠,稀硫酸
C.纯碳酸钙,稀硫酸 D.纯碳酸钠,稀盐酸
(4)用以上装置测出的气体摩尔体积均比理论值大,你认为减小实验误差可行的措施是_______。
A.把A装置浸入盛水(常温)的水槽中
B.减小酸的浓度
C.把A装置浸入盛热水的水槽中
D.增大酸的浓度
高二化学实验题困难题查看答案及解析
-
下列测定常温下1mo1氢气体积的操作中,使结果偏大的是
A.镁带中混有与酸不反应的杂质 B.装置接口连接处有气体泄漏
C.液体量瓶刻度读数未扣去硫酸的体积 D.硫酸注入量不足,镁带未反应完全
高二化学选择题中等难度题查看答案及解析
-
常温时,用1.0mol/L NaOH溶液中和某浓度硫酸溶液时,其pH 和所加NaOH溶液的体积关系如图所示。原硫酸溶液的物质的量浓度和完全反应后溶液的总体积是
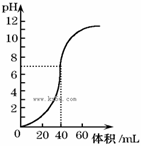
A.1 mol/L 60mL B.0.5 mol/L 80mL
C.0.5 mol/L 40mL D.1 mol/L 80mL
高二化学选择题中等难度题查看答案及解析
-
(6分)(1)常温下100mL0.05 mol·L-1的氢氧化钡溶液中滴加硫酸钠溶液,当两者恰好完全反应时,测得溶液的pH为12。则加入硫酸钠溶液的体积是____________ ml。(溶液混合时体积的变化不计,下同)
(2)常温下,若100体积的某强酸溶液与1体积的某强碱溶液混合后溶液呈中性,则混合之前,该强酸的PH(用a表示)与强碱的PH(用b表示)之间应满足的关系是________。
(3)已知100℃ KW=1×10-12 ,0.1mol/LNaOH溶液,由水电离出的OH-物质的量的浓度为________,PH=________。
高二化学计算题简单题查看答案及解析
-
利用如图装置可以测定常温下1mol氢气的体积,某同学的实验数据以及计算结果如下:
温度:10℃压强:1atm
(1)写出镁与硫酸反应的化学方程式:______实验次数 镁带质量(g) 硫酸体积(ml) C装置中液体的体积(ml) 最后抽气的体积(ml) 氢气的体积(ml) 计算1mol氢气的体积(L) ① 0.125 10 128.5 3.0 121.5 23.34 ② 0.133 10 135.5 3.0 128.5 23.19 ③ 0.127 10 129.7 3.0 122.7 23.19
(2)写出仪器名称:A______B______C______
(3)有同学认为上述实验中的第______次实验明显造假,其理由是______.
(4)此条件下1mol氢气的体积是(平均)=______L(保留2位小数)
(5)实验误差=______%(已知在此条件下1mol氢气的体积理论值为23.15L,保留2位小数).
(6)造成误差的可能原因有______
A、镁条表面的氧化物没有除 B、实验以后没有抽气
C、液体量瓶读数时俯视 D、镁带中含有少量的铝.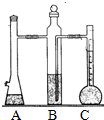
高二化学解答题中等难度题查看答案及解析
-
下列反应中,产生氢气速度最快的是( )
A.常温下铝与6mol/L的硝酸 B.常温下镁与3mol/L的醋酸
C.常温下铁与3mol/L的盐酸 D.常温下镁与3mol/L的硫酸
高二化学选择题简单题查看答案及解析
-
实验室用锌粒与2mol/L硫酸溶液制取氢气,下列措施不能增大化学反应速率的是( )
A.用锌粉代替锌粒 B.改用3mol/L硫酸溶液
C.改用热的确2mol/L硫酸溶液 D.向该硫酸溶液中加入等体积的水
高二化学选择题简单题查看答案及解析
-
(1)
碳与适量水蒸气反应生成CO和H2,需吸收
热量,此反应的热化学方程式为_________________
(2)已知
;
;
;
常温下,取体积比4:1的甲烷和氢气的混合气体
(标准状况下),经完全燃烧后恢复至室温,则放出的热量为___________
高二化学填空题简单题查看答案及解析
-
一定条件下,一种反应物过量,另一种反应物仍不能完全反应的是( )
A. 过量的氢气与氮气 B. 过量的浓盐酸与二氧化锰
C. 过量的铜与浓硫酸 D. 过量的锌与18 mol/L硫酸
高二化学多选题中等难度题查看答案及解析