-
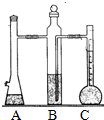
利用如图装置可以测定常温下1mol氢气的体积,某同学的实验数据以及计算结果如下:
温度:10℃压强:1atm
| 实验次数 | 镁带质量(g) | 硫酸体积(ml) | C装置中液体的体积(ml) | 最后抽气的体积(ml) | 氢气的体积(ml) | 计算1mol氢气的体积(L) |
| ① | 0.125 | 10 | 128.5 | 3.0 | 121.5 | 23.34 |
| ② | 0.133 | 10 | 135.5 | 3.0 | 128.5 | 23.19 |
| ③ | 0.127 | 10 | 129.7 | 3.0 | 122.7 | 23.19 |
(1)写出镁与硫酸反应的化学方程式:______
(2)写出仪器名称:A______B______C______
(3)有同学认为上述实验中的第______次实验明显造假,其理由是______.
(4)此条件下1mol氢气的体积是(平均)=______L(保留2位小数)
(5)实验误差=______%(已知在此条件下1mol氢气的体积理论值为23.15L,保留2位小数).
(6)造成误差的可能原因有______
A、镁条表面的氧化物没有除 B、实验以后没有抽气
C、液体量瓶读数时俯视 D、镁带中含有少量的铝.
-
利用镁和稀硫酸反应,不仅可以测定1mol氢气的体积,装置如下左图,也可以测定镁带中镁的质量分数(杂质与酸反应不产生气体),装置如图。
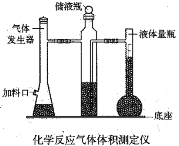
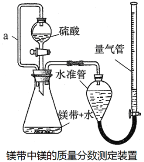
(1)用离子方程式表示测定实验的反应原理____________________________________。
(2)硫酸必须过量的目的是__________________________________________________。
(3)用“化学反应气体体积测定仪”测定1mol氢气的体积时,要三次用到注射器,其中两次是抽气调压,还有一次是___________________________________________。
(4)a(g)镁和足量稀硫酸反应,镁完全反应后,测得氢气在常温时的体积为V(L),则常温下l mol氢气的体积为_________________L。
(5)某学生在测定1molH2体积时,镁中混有少量铝,测定结果将_______________(填:偏大、偏小或没有变化)。
(6)若用“化学反应气体体积测定仪”也可以测定1mol二氧化碳气体的体积,那么储液瓶中应盛放________________________溶液。
(7)在“镁带中镁的质量分数测定装置”中,导管a的作用是______________________。
(8)“镁带中镁的质量分数测定”中,读取量气管的读数时,要使装置内外压强保持一致,具体操作为_________________________________________________________。
(9)在“镁带中镁的质量分数测定”中,如果实验的测定结果偏高,可能的原因是____________(选填编号)。
a.装置漏气 b.未冷却至室温即读数
c.镁带中含有氧化镁 d.末读数时量气管的液面低于水准管
-
(本题共10分)
利用镁和稀硫酸反应,不仅可以测定1mol氢气的体积,装置如下左图,也可以测定镁带中镁的质量分数(杂质与酸反应不产生气体),装置如下右图。
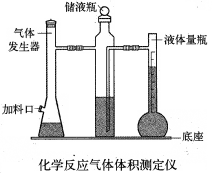
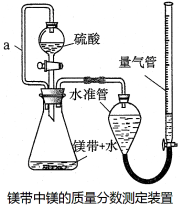
32.用离子方程式表示测定实验的反应原理 。
-
(10分)在常温常压下,可利用下列装置来测定气体体积,抽气装置E用以调节装置中的气压差,减小实验误差。
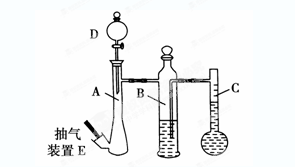
(1)若称取0.113g镁带与10.00 mL稀硫酸(足量)完全反应制取氢气,并测定1mol H2的体积(在常温常压下测定)。反应结束时C中的液面刻度为128.00 mL(A中未加硫酸时C中无液体),则得此条件下1mol H2的体积为________L(精确到0.001)。
(2)上述测出1mol H2的体积比该温度和压强下的理论值偏高的原因是(假设操作和装置都无问题)________(选填编号,下同)
A.未冷却到室温 B.反应太快
C.装置气密性不好 D.B装置漏气
(3)若利用上述装置测定CO2的气体摩尔体积。
①B中所盛放的液体应为________。
A.饱和Na2CO3溶液 B.饱和NaHCO3溶液
C.水 D.澄清石灰水
②仪器A、D中盛放的试剂应为________。
A.大理石,浓盐酸 B.纯碳酸钠,稀硫酸
C.纯碳酸钙,稀硫酸 D.纯碳酸钠,稀盐酸
(4)用以上装置测出的气体摩尔体积均比理论值大,你认为减小实验误差可行的措施是_______。
A.把A装置浸入盛水(常温)的水槽中
B.减小酸的浓度
C.把A装置浸入盛热水的水槽中
D.增大酸的浓度
-
某同学利用如图所示实验装置测定常温常压下的气体摩尔体积。
根据下列步骤完成实验:
①装配好装置,检查气密性
②用砂纸擦去镁带表面的氧化物,然后取0.0480g的镁带加入仪器a中,分液漏斗内加入足量1mol/L硫酸溶液
③量气装置中加入适量水,记录量气管读数(读数为0.10mL)
④通过分液漏斗向仪器a中加入适量硫酸溶液,使镁带与硫酸充分反应
⑤当镁带完全反应后,再次记录量气管读数(读数为49.60mL)。
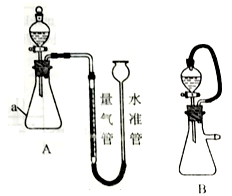
完成下列填空:
(1)仪器a的名称_______,通过分液漏斗向仪器a中加入硫酸溶液的操作是_______。
(2)在记录量气管读数时,应注意将_______,再________,视线与量气管内凹液面相切,水平读数。
(3)该同学测出此条件下气体摩尔体积为__________,测定结果比理论值偏大,可能的原因是(填字母代号)__________。
a.镁带中氧化膜未除尽 b.镁带含有杂质铝
c.③记录量气管读数时俯视读数 d.镁带完全反应后有残留的未溶固体
(4)与原方案装置相比,有同学设想用装置B代替装置A,实验精确度更高。请说明理由____________________。
-
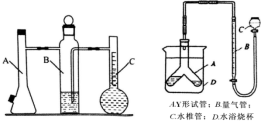
利用下左图所示实验装置可以测定常温常压下气体的摩尔体积。
 c
c
甲同学利用如上左图装置,根据下列步骤完成实验:
① 装配好装置,作气密性检查。
②用砂纸擦去镁带表面的氧化物,然后取0.108g的镁带。
③取下A瓶加料口的橡皮塞,用小烧杯加入20mL水,再把已称量的镁带加到A瓶的底部,用橡皮塞塞紧加料口。
④用注射器从A瓶加料口处抽气,使B瓶导管内外液面持平。
⑤用注射器吸取10mL3mol·L-1硫酸溶液,用针头扎进A瓶加料口橡皮塞,将硫酸注入A瓶,注入后迅速拔出针头。
⑥当镁带完全反应后,读取C瓶中液体的体积,记录数据。⑦用注射器从A瓶加料口处抽出8.0mL气体,使B瓶中导管内外液面持平。⑧读出C瓶中液体体积是115.0mL。
完成下列填空:
(1) 在常温常压下气体摩尔体积理论值约为24.5L/mol,甲同学测出此条件下lmol气体的体积为______,计算此次实验的相对误差为________%〈保留2位有效数字)。引起该误差的可能原因是______。
a.镁带中含铝; b.没有除去镁带表面的氧化物; c.反应放热; d.所用硫酸的量不足
(2) 丙同学提出可用如上右图装置完成该实验。该装置气密性的检查方法是:_____________。
(3) 与原方案装置相比,丙同学使用的装置实验精度更高。请说明理由(回答两条)____________________________________,_____________________________________。
-
甲、乙两个实验小组利用 酸性溶液与
酸性溶液与 溶液反应研究影响反应速率的因素。
溶液反应研究影响反应速率的因素。
设计实验方案如下 实验中所用
实验中所用 溶液均已加入
溶液均已加入 :
:
甲组:通过测定单位时间内生成 气体体积的大小来比较化学反应速率的大小某同学进行实验,实验装置如图.其中A、B的成分见表
气体体积的大小来比较化学反应速率的大小某同学进行实验,实验装置如图.其中A、B的成分见表
| 序号 | A溶液 | B溶液 |
| ① |  溶液 溶液
|  溶液 溶液
|
| ② |  溶液 溶液
|  溶液 溶液
|
| ③ |  溶液 溶液
|  溶液和少量 溶液和少量
|
 该反应的离子方程式为 ______
该反应的离子方程式为 ______
 实验开始前需要检查气密性.分液漏斗中A溶液应该 ______ 加入
实验开始前需要检查气密性.分液漏斗中A溶液应该 ______ 加入 填“一次性”或“逐滴滴加”
填“一次性”或“逐滴滴加”
 完成该实验还需要 ______
完成该实验还需要 ______  填仪器名称
填仪器名称 ,实验结束后读数前需要移动量气管,使两个量气管的液面相平.
,实验结束后读数前需要移动量气管,使两个量气管的液面相平.
乙组:通过测定 溶液褪色所需时间的多少来比较化学反应速率为了探究
溶液褪色所需时间的多少来比较化学反应速率为了探究 与
与 浓度对反应速率的影响,某同学在室温下完成以下实验
浓度对反应速率的影响,某同学在室温下完成以下实验
| 实验编号 | 1 | 2 | 3 | 4 |
| 水 | 10 | 5 | 0 | X |
| 
| 5 | 10 | 10 | 5 |
| 
| 5 | 5 | 10 | 10 |
| 时间 | 40 | 20 | 10 | --- |
 ______ ,4号实验中始终没有观察到溶液褪色,你认为可能的原因是 ______ 。
______ ,4号实验中始终没有观察到溶液褪色,你认为可能的原因是 ______ 。
 号反应中,
号反应中, 的反应速率为 ______。
的反应速率为 ______。
 在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.某同学认为是放热导致溶液温度升高所致,重做3号实验,测定过程中溶液不同时间的温度,结果如表:
在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.某同学认为是放热导致溶液温度升高所致,重做3号实验,测定过程中溶液不同时间的温度,结果如表:
| 时间 | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 温度℃ | 25 | 26 | 26 | 26 | 
| 27 | 27 |
结合实验目的与表中数据,你得出的结论是 ______。
 从影响化学反应速率的因素看,你的猜想还可能是 ______ 的影响。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是 ______
从影响化学反应速率的因素看,你的猜想还可能是 ______ 的影响。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是 ______  填字母
填字母 。
。
A 硫酸钾  水
水  二氧化锰
二氧化锰  硫酸锰。
硫酸锰。
-
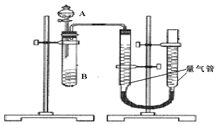
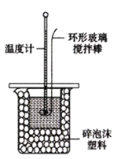
实验室用50mL 0.50mol/L盐酸、50mL0.55mol/L NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:
| 实验次数 | 起始温度/℃ | 终止温度/℃ |
| 盐酸 | NaOH溶液 |
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
完成下列问题:
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是___。实验中使用环形玻璃搅拌棒的操作方法是____;
(2)在操作正确的前提下,提高中和热测定准确性的关键是_____;
(3)根据表中所测数据进行计算,则该实验测得的中和热 =_____ [盐酸和NaOH溶液的密度按1
=_____ [盐酸和NaOH溶液的密度按1 计算,反应后混合溶液的比热容(c)按4.18
计算,反应后混合溶液的比热容(c)按4.18 计算]。如果用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的中和热将______ (填“偏大”“偏小”或“不变”)。
计算]。如果用0.5mol/L的盐酸与NaOH固体进行实验,则实验中测得的中和热将______ (填“偏大”“偏小”或“不变”)。
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热数值偏低,请你分析可能的原因是__________;
A.测量盐酸的温度后,温度计没有用水冲洗干净 B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓 C.做本实验的当天室温较高 D.在量取盐酸时仰视读数 E.大烧杯的盖板中间小孔太大
-
实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到下表中的数据:

| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ |
| 盐酸 | NaOH溶液 |
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
| | | |
完成下列问题:
(1)实验时不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是 。
(2)在操作正确的前提下,提高中和热测定准确性的关键是 。
(3)根据上表中所测数据进行计算,则该实验测得的中和热ΔH= [盐酸和NaOH溶液的密度按1 g·cm-3计算,反应后混合溶液的比热容(c)按4.18 J·(g·℃)-1计算]。如果用0.5 mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将 (填“偏大”、“偏小”或“不变”)。
(4)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是 。
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.在量取盐酸时仰视读数
E.大烧杯的盖板中间小孔太大
-
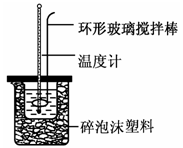
实验室用50 mL 0.50 mol·L-1盐酸、50 mL 0.55 mol·L-1 NaOH溶液和如图所示装置,进行测定中和热的实验,得到表中的数据:
| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ |
| 盐酸 | NaOH溶液 |
| 1 | 20.2 | 20.3 | 23.7 |
| 2 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
| | | |
完成下列问题:
(1)不能用铜丝搅拌棒代替环形玻璃搅拌棒的理由是_ 。
(2)在操作正确的前提下,提高中和热测定准确性的关键是_____________。大烧杯如不盖硬纸板,求得的中和热数值将 (填“偏大”、“偏小”或“无影响”)。结合日常生活实际该实验在 中(家用产品)效果更好。
(3)根据上表中所测数据进行计算,则该实验测得的中和热ΔH=___ [盐酸和NaOH溶液的密度按1 g·cm-3计算,反应后混合溶液的比热容(c)按4.18 J·(g·℃)-1计算]。
(4)如用0.5 mol/L的盐酸与NaOH固体进行实验,则实验中测得的“中和热”数值将___ _(填“偏大”、“偏小”、“不变”)。如改用60 mL0.5 mol/L的盐酸与50 mL 0.55 mol·L-1 的NaOH 溶液进行反应,与上述实验相比,所放出的热量 (填“相等”或“不相等”),所求中和热 (填“相等”或“不相等”)。
(5)若某同学利用上述装置做实验,有些操作不规范,造成测得中和热的数值偏低,请你分析可能的原因是 。
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.在量取盐酸时仰视计数
F.大烧杯的盖板中间小孔太大







 c
c


